Clear Sky Science · ar
التوجيه بالذكاء الاصطناعي للتثبيت التنافسي للفحص الافتراضي وتنبؤ فعالية المركبات
بحث أذكى عن أدوية جديدة
العثور على أدوية جديدة يشبه إلى حد ما البحث عن إبرة في كومة قش تتكون من ملايين الجزيئات. تُظهر هذه الدراسة كيف يمكن للتقدّم الحديث في الذكاء الاصطناعي أن يجعل هذا البحث أسرع وأرخص من خلال مساعدة العلماء على التنبؤ بأي الجزيئات من المرجح أن تلتصق ببروتين مرتبط بالمرض وتعمل فعليًا كدواء. بدلاً من اختبار مركب كيميائي واحد في المختبر في كل مرة، يستخدم المؤلفون نماذج ذكاء اصطناعي لإجراء مسابقات افتراضية بين الجزيئات ويتركون الفائزين يتصدّرون القائمة.
كيف يتعلّم الذكاء الاصطناعي رؤية توافق القفل والمفتاح الجزيئي
تعمل العديد من الأدوية الحديثة من خلال الانسجام مع جيوب صغيرة على البروتينات، تمامًا كما يلائم المفتاح القفل. تقليديًا، حاولت برامج الحاسوب التنبؤ بهذا التوافق باستخدام معادلات فيزيائية تقدّر القوى بين الذرات. في السنوات القليلة الماضية، مع ذلك، تعلّمت أنظمة ذكاء اصطناعي جديدة تُعرف بنماذج الطي المشترك المعتمدة على الانتشار—مثل AlphaFold3 وBoltz—من عدد هائل من البُنى المعروفة للبروتين-الجزيء. تستطيع هذه الأنظمة الآن «تخيّل» كيف قد يطوى البروتين والدواء المحتمل معًا في ثلاثة أبعاد، حتى عندما لا توجد بنية تجريبية. السؤال المركزي الذي يتعامل معه المؤلفون هو ما إذا كانت هذه الأدوات قادرة على أكثر من رسم صور معقولة—هل يمكنها أيضًا تمييز الأدوية الجيدة من غيرها؟
الرابطون الحقيقيون مقابل المتنكرين
اختبر الفريق أولًا 16 بروتينًا مدروسًا جيدًا بالإضافة إلى إنزيم بكتيري أكثر تعقيدًا يسمى دنا جيراز. لكل بروتين، طلبوا من نماذج الذكاء الاصطناعي وضع كل من المثبطات النشطة المعروفة ومجموعة من الجزيئات «خارج الهدف» غير المرتبطة في نفس موقع الارتباط. بدلًا من الوثوق بتنبؤ واحد، نظروا في مدى اتساق وضع كل جزيء عبر عدة محاولات. كان المثبطون الحقيقيون يميلون إلى العودة إلى نفس الموقع والاتجاه مرارًا وتكرارًا، متجمعين ضمن نطاقات ضئيلة جدًّا من المسافة. في المقابل، كانت الجزيئات غير النشطة تتجول على نطاق أوسع وغالبًا ما تكون أبعد عن الجيب. هذه الفكرة البسيطة—تقارب الوضعيات—تبين أنها إشارة قوية على أن المركب يناسب هدف البروتين فعليًا.
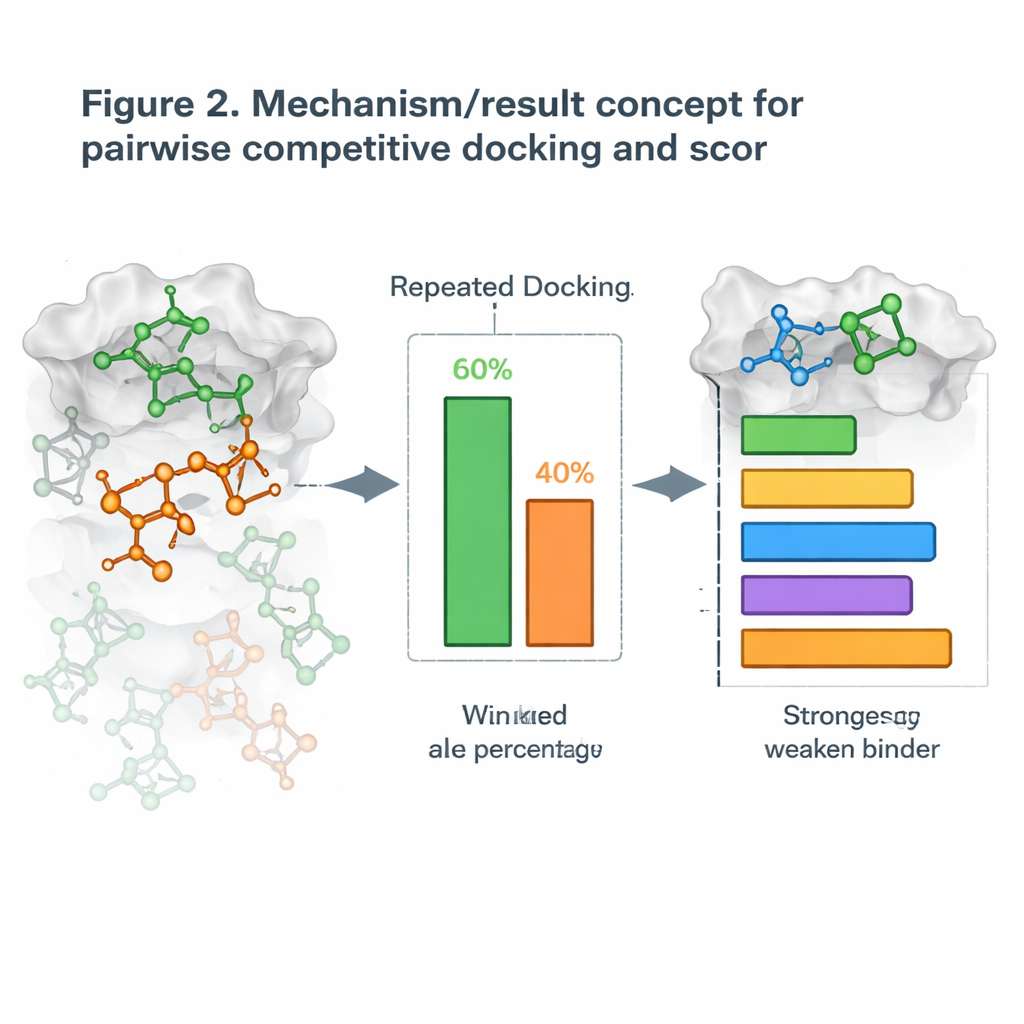
تحويل الترسيب إلى منافسة وجهًا لوجه
استنادًا إلى ذلك، قدم المؤلفون استراتيجية جديدة يسمونها الترسيب التنافسي الزوجي. بدلًا من ترسيب جزيء واحد في كل مرة، يقومون بترسيب مرشحين اثنين مع البروتين ويدعونهما «يتنافسان» على نفس الجيب. بعد العديد من المحاولات المتكررة، يُعلَن فوز الجزيء الذي يشغل الموقع في أغلب الأحيان في تلك المباراة. من خلال تشغيل كل التزاوجات الممكنة، يبنون جدولًا للفوز-الخسارة ويحسِبون درجة الترسيب التنافسي لكل جزيء، على غرار ترتيب اللاعبين في دورة روبن-راوند. عندما قورنت هذه الدرجات بقياسات العالم الحقيقي لمدى قدرة الجزيئات على حجب أهدافها، تطابقت الترتيبات غالبًا بشكل جيد، مع بعض نظم البروتين التي أظهرت اتفاقًا يكاد يكون تامًا.
من الشاشات الافتراضية إلى تصميم مضادات حيوية أفضل
كان دنا جيراز، وهو إنزيم أساسي للبكتيريا، حالة اختبار مفصّلة. يحتوي هذا البروتين على عدة جيوب دوائية تستهدفها فئات مختلفة من المضادات الحيوية، بما في ذلك الفلوركينولونات المستخدمة على نطاق واسع. استطاعت نماذج الذكاء الاصطناعي عادة وضع كل فئة دوائية في جيبها الصحيح، وتبعت درجات الترسيب التنافسي تقريبًا قوتها المقاسة. ثم وسّع المؤلفون العمل إلى فحص افتراضي لأكثر من 3000 دواء معتمد، سائِلين أي الجزيئات تنافس أفضل على موقع الفلوركينولون. استراتيجيتهما ذات المرحلتين—أولًا استخدام منافسة «الكل دفعة واحدة» لاختيار الفائزين المحتملين، ثم التصفية بحسب مدى تكتّلهم داخل الجيب—عزّزت بشكل كبير وجود الفلوركينولونات الحقيقية بينما استبعدت المرشحين الأضعف. أخيرًا، استخدموا مولد جزيئات مدفوعًا بالذكاء الاصطناعي لاقتراح هياكل جديدة شبيهة بالفلوركينولون وطبقوا الترسيب التنافسي ليجدوا عددًا قليلًا ذات ارتباط متوقع أفضل وخصائص مناسبة كأدوية.
الوعود والحدود وما يعنيه ذلك للمرضى
تُظهر الدراسة أن نماذج الذكاء الاصطناعي الحديثة قادرة على أكثر من رسم هياكل محتملة للبروتين-الدواء: عندما تُشغل في إطار تنافسي، يمكنها المساعدة في ترتيب المركبات بطريقة غالبًا ما تعكس بيانات تجريبية حقيقية. هذا لا يستبدل العمل المخبري—الأداء ما زال يعتمد بقوة على البروتين المعين، بعض الجيوب يتم التنبؤ بها خطأً، ونماذج الذكاء الاصطناعي قد تفشل مع جزيئات كبيرة جدًا أو غير عادية. لكن مع تحسّن هذه النماذج وبيانات تدريبها، قد تجعل أساليب مثل الترسيب التنافسي الزوجي اكتشاف الأدوية المبكر أكثر كفاءة بكثير. بالنسبة للمرضى، قد يترجم ذلك في نهاية المطاف إلى تطوير أسرع لأدوية موجهة، بما في ذلك مضادات حيوية جديدة تواكب البكتيريا المقاومة.
الاستشهاد: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
الكلمات المفتاحية: اكتشاف الأدوية بالذكاء الاصطناعي, الفحص الافتراضي, الترسيب الجزيئي, ارتباط البروتين-الرابط, تصميم المضادات الحيوية