Clear Sky Science · ar
استنتاج اختلالات مسارات الإشارة من صور الأنسجة المرضية عبر رسم بياني معرفي غير متجانس للجينات-المسارات مقيد بالمنطق
رؤية إشارات الخلايا الخفية في شرائح السرطان
عندما يفحص الأطباء السرطان تحت المجهر، فإنهم يرون في الغالب الأشكال والألوان، لا المحادثات الجزيئية المعقدة الجارية داخل الخلايا. ومع ذلك، غالبًا ما تحدد هذه «المحادثات» غير المرئية للإشارات بين الجينات والمسارات كيفية نمو الورم وكيف قد يستجيب للعلاج. تقدم هذه الدراسة نظام ذكاء اصطناعي جديدًا يقرأ صور الباثولوجيا الروتينية ويستنتج أي مسارات الاتصال الخلوية — أو أي المسارات — هي التي تتعرض للخلل، موفِّرًا وسيلة لإلقاء نظرة على السلوك الجزيئي دون اختبارات مخبرية إضافية.
من دلائل الجين الفردي إلى الصورة الأكبر
تحاول الطرق التقليدية التنبؤ بحالة الجينات الفردية من صور الأنسجة: هل جين معين متحور أم لا؟ هذا مفيد، لكن السرطان نادرًا ما يعتمد على جين واحد معطل فقط. بدلاً من ذلك، تعمل مجموعات من الجينات معًا لتعطيل مسارات إشارات كاملة تتحكم في النمو والبقاء والمناعة. يجادل المؤلفون بأن التركيز على الجينات الفردية يفوّت هذا السلوك التعاوني وقد يفشل في تفسير لماذا تبدو الأورام وتتصرّف كما هي تحت المجهر.
بناء خريطة بين الصور والجينات والمسارات
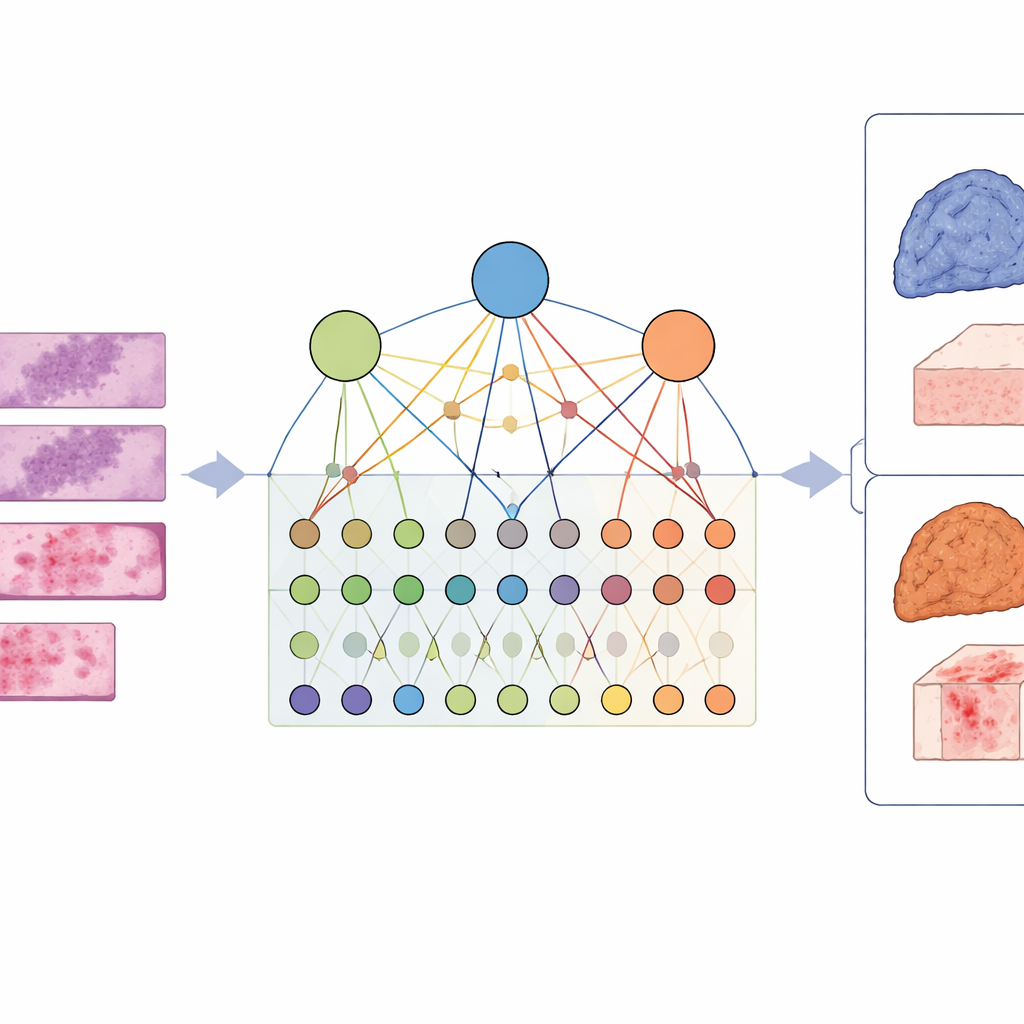
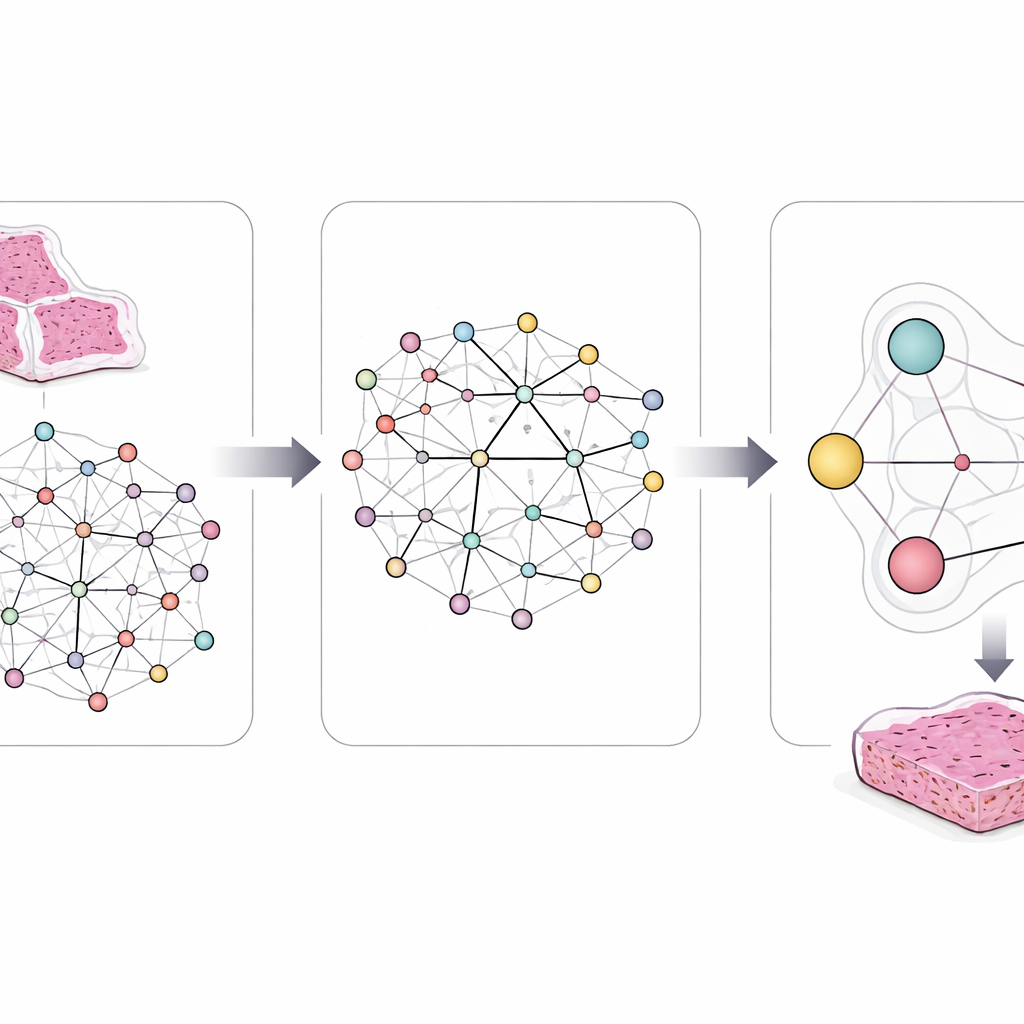
لالتقاط هذا التعقيد، صمّم الباحثون إطار عمل اسمه LCG-HGNN يربط بين ثلاث طبقات من المعلومات. أولاً، يقسمون كل شريحة كاملة من صور سرطان غدي الرئة إلى رقع صغيرة عديدة ويمثلون هذه الرقع على شكل رسم بياني، حيث تُربط المناطق القريبة أو المتشابهة المظهر. ثانيًا، يربطون علامات الجينات بالمسارات الإشارية باستخدام قواعد بيانات بيولوجية معتمدة، وبذلك يبنون رسمًا بيانيًا ثانيًا يُشفِّر أي الجينات تنتمي لأي مسارات. أخيرًا، يسمحون لنموذج ذكاء اصطناعي بتمرير المعلومات عبر هذا الرسم البياني المدمج، بحيث تؤثر أنماط الصور والجينات والمسارات في بعضها البعض بدلاً من التعامل معها بشكل منعزل.
تعليم النظام البيولوجيا المعروفة
الابتكار الرئيسي هو أن النموذج لا يُسمح له بالتعلّم بحرية دون توجيه. يضمّن المؤلفون بيانات صريحة على شكل قوانين مشتقة من عقود من أبحاث السرطان. على سبيل المثال، بعض الطفرات نادرًا ما تظهر معًا في نفس الورم، وبعض المسارات تقع أسفل أو أعلى مسارات أخرى. يقومون بترميز مثل هذه القواعد كقيود منطقية توجه بلطف الاتصالات الداخلية وتنبؤات الذكاء الاصطناعي. إذا اقترح النموذج مجموعة من تغييرات الجينات والمسارات تتعارض مع البيولوجيا المعروفة أو مع تشابه شرائح المرضى، فإن هذه القواعد تدفعه نحو بدائل أكثر واقعية.
اختبار الدقة مقابل الطرق القائمة
قيّم الفريق نظامه باستخدام أكثر من 1600 شريحة سرطانية للرئة مرتبطة ببيانات جينية. قارنوه مع نماذج تعلم عميق قياسية تركز على جينات فردية ومع طرق أكثر تقدمًا تتعامل مع العديد من الجينات مرة واحدة لكنها تتجاهل بنية المسارات. عبر عدة مسارات مهمة، بما في ذلك تلك المرتبطة بإشارات نمو الخلايا والهياكل الداعمة للنسج، تنبأ النموذج الجديد بتغيرات مجموعات الجينات واختلالات المسارات بدقة أعلى. كما أنتج رقع صور كان مظهرها متطابقًا إلى حد كبير مع أمثلة سريرية حقيقية معروفة بأنها مرتبطة بطفرات محددة، مما يوحي بأنه كان يركّز على أنماط مجهرية ذات مغزى بدلًا من عيوب عشوائية في الصور.
لماذا هذا مهم للمرضى
بالنسبة لغير المتخصص، النتيجة الأساسية هي أن هذا النهج يحوّل شريحة باثولوجيا روتينية إلى مصدر غني للرؤى الجزيئية. بدلاً من طلب اختبارات جينية منفصلة وغالبًا مكلفة لكل هدف محتمل، قد يتمكن الأطباء في المستقبل من استخدام مثل هذه النماذج لفحص المسارات المتعطلة مباشرة من الصور التي يجمعونها بالفعل. وبينما لا يزال الأسلوب بحاجة إلى تحقق أوسع في العالم الحقيقي ولا يحل بعد محل الاختبارات الجينية، إلا أنه يشير إلى مستقبل حيث يصبح منظر المجهر نافذة على البنية الداخلية للورم — مساعدًا في توجيه رعاية سرطانية أدق وأكثر استنادا إلى البيولوجيا.
الاستشهاد: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
الكلمات المفتاحية: مسارات السرطان, الذكاء الاصطناعي في علم الأمراض النسيجي, شبكات الرسم البياني العصبية, سرطان غدي رئة, الباثولوجيا الرقمية