Clear Sky Science · ar
نماذج مخبرية ثلاثية الأبعاد حيوية التكوين كمنهجيات نهجية جديدة بديلة للحيوانات
إعادة التفكير في كيفية اختبار الأدوية الجديدة
لمدة تقارب القرن، كان يُختبر معظم الأدوية الجديدة على الحيوانات قبل الوصول إلى التجارب البشرية. ومع ذلك، فإن أكثر من 9 من كل 10 مرشحين دوائيين يبدون آمنين في الحيوانات يفشلون لاحقًا في البشر. تستعرض هذه المقالة كيف يمكن لجيل جديد من الأنسجة البشرية «المطبوعة حيويًا» ثلاثية الأبعاد أن يغير هذه القصة — مقدماً طرقاً أدق وأكثر إنسانية لتوقع كيفية استجابة أجسامنا للأدوية، وربما مسرّعاً لوصول علاجات أكثر أماناً إلى المرضى.

من حيوانات المختبر إلى الاختبارات المتمحورة حول الإنسان
ألغت تشريعات أمريكية حديثة، تُعرف باسم قانون تحديث إدارة الغذاء والدواء 2.0، المطلب التلقائي لاختبار كل دواء جديد على الحيوانات. وبدلاً من ذلك، يمكن للجهات المنظمة الآن قبول «منهجيات النهج الجديدة» — أنظمة اختبار ذات صلة بالإنسان مصممة لتوقع استجابات المرضى الحقيقية بشكل أفضل. ومن بين هذه النهج تبرز الطباعة الحيوية ثلاثية الأبعاد. تستخدم طابعات متخصصة لوضع خلايا بشرية حية ومواد طرية شبيهة بالجِلّ في أشكال معقدة تحاكي الأنسجة الحقيقية والأعضاء المصغرة. تبدأ العملية غالباً بصور طبية مثل مسح الكمبيوتر المقطعي أو الرنين المغناطيسي، التي توفر مخططاً. ثم يختار العلماء المواد الحيوية المناسبة، ويخلطون أنواع الخلايا الملائمة لصنع «حبر حيوي» قابل للطباعة، ويطبعون هياكل طبقية أو حجمية تنضج لاحقاً إلى نماذج نسيجية وظيفية داخل المفاعل الحيوي.
كيف تبني الطباعة الحيوية ثلاثية الأبعاد أنسجة حية
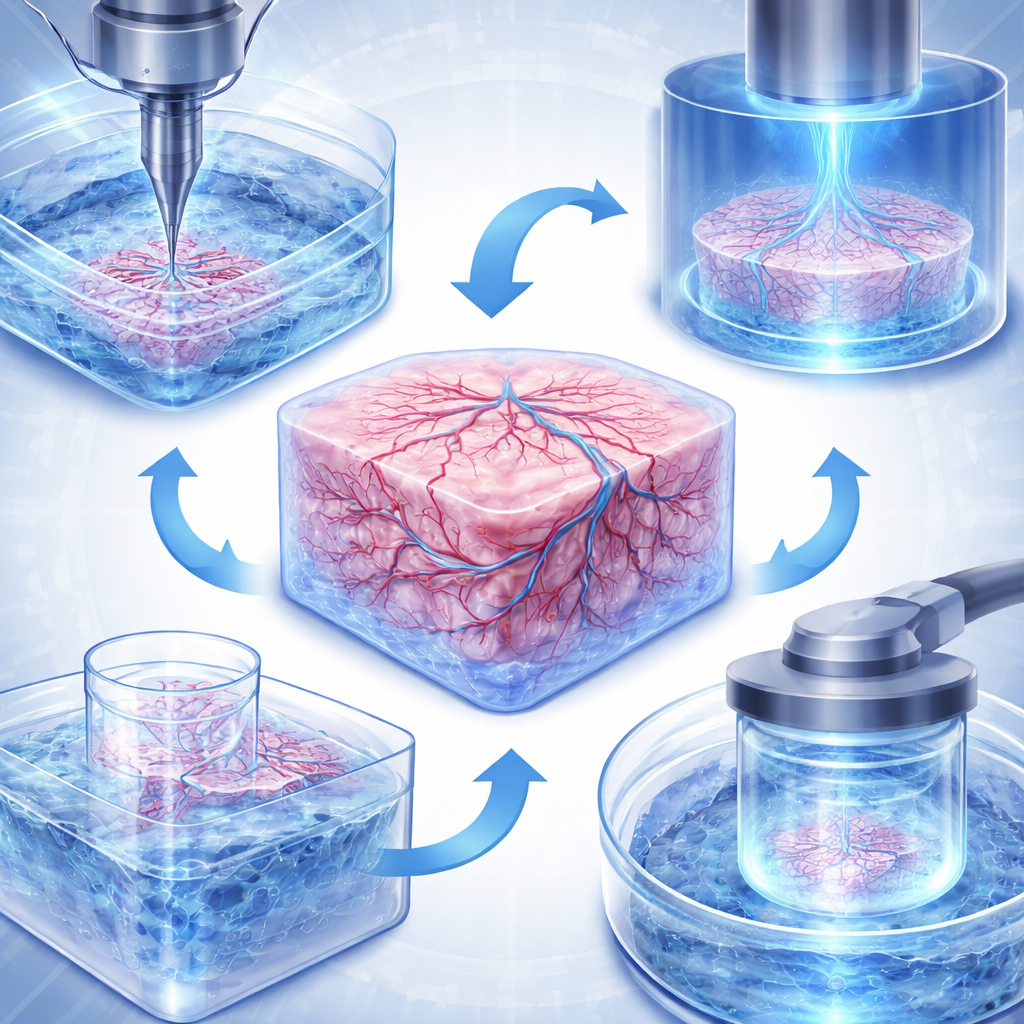
الطباعة الحيوية ليست تقنية واحدة بل عائلة من الأساليب. تطلق الطابعات ذات طراز نفاث الحبر قطرات صغيرة من سائل يحتوي خلايا لبناء طبقات رقيقة ذات تفاصيل دقيقة، مما يجعلها مفيدة للأنسجة المصغرة مثل رقع الجلد أو حواجز الرئة. تضغط طابعات البثق خيوطاً مستمرة من أحبار حيوية أكثر كثافة، قد تشمل كثيراً من الخلايا والألياف الداعمة، ما يمكّن من بناء هياكل أكبر وأكثر صلابة مثل صمامات القلب، نماذج أورام الكبد، أو شبكات الأوعية الدموية. فئة أحدث، تُدعى التصليد الضوئي في الحوض، تسلط ضوءاً مُنقّطاً داخل سائل لتصلّب أشكال معقدة دون إجبار الخلايا على المرور عبر فوهات. يمكن لأنماط من هذه الطريقة نحت ميزات على مقياس الميكرون، أو طباعة عضو صغير كامل في ثوانٍ، أو حتى تشكيل أنسجة داخل حمام شفاف، كل ذلك مع الحفاظ على حيوية الخلايا.
استبدال وصقل اختبارات الأدوية
تُستخدم هذه الأنسجة المطبوعة بالفعل لإعادة التفكير في خط أنابيب الأدوية. في مرحلة الاكتشاف المبكر، تتيح التركيبات المخصّصة للمريض أو للمرض — مثل نماذج الأورام المطبوعة حيوياً — للباحثين اختبار العديد من المرشحين الدوائيين في بيئات ثلاثية الأبعاد واقعية تشبه المرض البشري أفضل من الطبقات الخلوية المسطحة في الصحن. في الاختبارات قبل السريرية، تثبت أنسجة الجلد والرئة والكبد المطبوعة دقتها أكثر من الحيوانات في الكشف عن السمية أو الآثار الجانبية الخاصة بالبشر. تذهب بعض الدراسات أبعد من ذلك بطباعة «تجارب سريرية على شريحة»، حيث تتعرض أنسجة مأخوذة من خلايا متبرعين مختلفين لدواء بالتوازي، كاشفةً من قد يستفيد أو يتعرض للضرر. تشجع الجهات المنظمة الآن الشركات على تقديم بيانات من هذه النماذج إلى جانب دراسات الحيوانات، لبناء الأدلة اللازمة للاعتراف الأوسع.
هندسة الأعضاء دون جسد
على الرغم من التقدم السريع، تبقى عدة عقبات قبل أن تحل الأنسجة المطبوعة مكان اختبارات الحيوانات بشكل روتيني. تحدٍ رئيسي هو الإمداد الدموي: تحتوي الأعضاء الحقيقية على شبكات وعائية تتدرج من شرايين كبيرة إلى شعيرات دموية رفيعة جداً، بينما يجب على التركيبات المطبوعة التغلب على حد طبيعي لمسافة انتشار الأكسجين والمغذيات. يعالج الباحثون ذلك باستراتيجيات طباعة جديدة تخلق قنوات متفرعة، وبحمامات داعمة تثبت الأنسجة الطرية أثناء تشكيل الأوعية الدقيقة، وبطابعات حجمية فائقة السرعة تصنع هياكل كثيفة الخلايا قبل أن تبدأ الخلايا بالتدهور. تحدٍ آخر هو الواقعية: الأنسجة الحية مزيج من أنواع خلوية متعددة مغمورة في إشارات كيميائية معقدة وغالباً تتأثر بالميكروبيوم والأعضاء البعيدة. تجمع النماذج المتقدمة الآن بين مجموعات خلوية متعددة، وتدرجات محكمة للأكسجين ودرجة الحموضة، وحتى أنظمة «متعددة الأعضاء» الموصولة التي تربط الأمعاء والكبد والجهاز المناعي والدماغ عبر تيار سائل لمحاكاة استجابات الجسم ككل.
مستقبل إنساني وتنبؤي لتطوير الأدوية
تشير هذه التطورات مجتمعة إلى مستقبل تصبح فيه نماذج الأنسجة البشرية عالية الدقة مركزية في طريقة تقييمنا للأدوية. وتخلص المقالة إلى أن الطباعة الحيوية ثلاثية الأبعاد تنتقل من تقنية مختبرية متخصصة إلى أداة أساسية لبناء أنظمة اختبار موحدة وجاهزة للجهات المنظمة. ولتحقيق هذا الوعد بالكامل، يجب على العلماء والجهات المنظمة الاتفاق على متى وكيف تُستخدم هذه النماذج، وإثبات أنها تتنبأ بنتائج البشر بشكل موثوق، وحل التحديات التقنية المتبقية مثل بناء أوعية دموية مستقرة وأعضاء معقدة تشريحياً. إذا نجح ذلك، فقد يقل الاعتماد على اختبارات الحيوانات، ويُخفض الفشل المكلف في مراحل متأخرة من تطوير الأدوية، ويُقدَّم علاج آمن وأكثر فعالية يعكس بيولوجيا ما يهم حقاً: أجسامنا.
الاستشهاد: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
الكلمات المفتاحية: الطباعة الحيوية ثلاثية الأبعاد, بدائل اختبار الحيوانات, تطوير الأدوية, نماذج الأنسجة, الطباعة الحيوية الحجمية