Clear Sky Science · ar
هندسة البالعات الكبيرة للعلاج المناعي للسرطان: رؤى ناشئة وإمكانات علاجية
تحويل طاقم التنظيف في الجسم إلى مقاتلين ضد السرطان
أجسامنا مليئة بالبالعات الكبيرة—خلايا «تنظيف» تجوب الجسم وتبتلع الجراثيم والأنسجة الميتة. تستعرض هذه المقالة كيف يتعلم العلماء توجيه هذه الخلايا ضد السرطان. وبما أن البالعات الكبيرة وفيرة داخل الأورام، بما في ذلك تلك التي تقاوم العلاجات المناعية الرائدة اليوم، فإن فهمها وهندستها قد يفتح خيارات علاجية جديدة للمرضى ذوي السرطانات شديدة المراس.
الوجوه المتعددة لنوع خلوي واحد
البالعات الكبيرة ليست نوعاً خلويًا ثابتًا واحدًا؛ إنها قادرة على التغيّر. قد تأتي من مجرى الدم أو تعيش بالفعل في الأنسجة، ومتى استقرت تستجيب للإشارات المحلية. داخل الأورام يمكن لهذه البالعات المرتبطة بالورم أن تساعد في قتل الخلايا السرطانية أو، بشكل محير، أن تساعد الورم على النمو والانتشار. سابقًا حاول الباحثون حشرها في صندوقين—«M1» (وضع الهجوم) و«M2» (وضع الإصلاح أو الدعم). تُظهر أدوات التحديد الجيني والمكاني الحديثة الآن طيفًا أغنى بكثير من الحالات، مع مجموعات فرعية متعددة وسلوكيات تختلف بين ورم وآخر وبين موقع وآخر. حتى الخلايا التي كانت تُعتبر سابقًا «مؤيدة للورم» قد تستطيع، في بعض السياقات، استنهاض الخلايا التائية ودعم المناعة المضادة للسرطان.
إحساسهم بالمحيط وابتلاعهم للخلايا السرطانية
البالعات الكبيرة لا تكتفي بالاستماع لإشارات كيميائية؛ بل تشعر أيضًا بالعالم الفيزيائي من حولها. أثناء زحفها عبر شبكة البروتين الكثيفة داخل الورم، وانضغاطها بين الخلايا، وتحملها لقوى السوائل، تستشعر الصلابة والشد عبر مستقبلات متخصصة مثل Piezo1. هذه الإشارات الميكانيكية، جنبًا إلى جنب مع الإشارات المناعية التقليدية، يمكن أن تميل بالبالعات نحو أدوار أكثر التهابية أو أكثر مهدئة. وظيفيًا، تستطيع البالعات ابتلاع الخلايا السرطانية، ثم تقطعها وتعرض شظاياها (مستضدات) للخلايا التائية، جسرًا بين المناعة الفطرية والمكتسبة. تقاوم الخلايا السرطانية ذلك بإرسال إشارات «لا تأكلني»، على نحو خاص عبر جزيء سطحي يسمى CD47 الذي يرتبط بفرامل على البالعات. العقاقير التي تحجب هذا التفاعل في العديد من التجارب السريرية تعزز تطهير الخلايا السرطانية لكنها تتطلب ضبطًا دقيقًا لتجنب إلحاق الضرر بالخلايا السليمة.
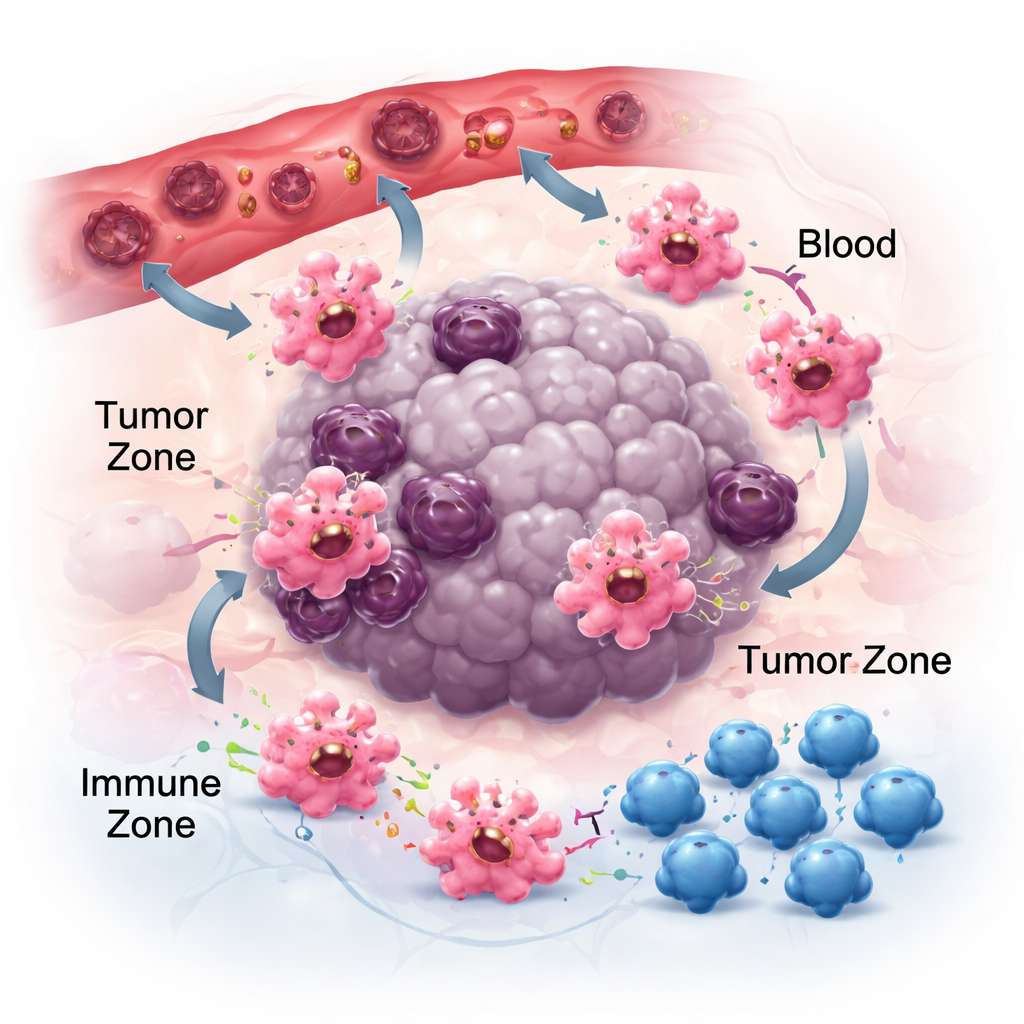
الحركة والالتصاق والتواصل في حي الورم
لكي تكون البالعات مهمة في السرطان، يجب أولاً أن تصل إلى الأورام ثم تتوضع في المواضع المناسبة. تتبع آثارًا كيميائية—كيموكينات وعوامل نمو—تفرزها الخلايا السرطانية والمحيطة بها. أزواج مثل CCR2–CCL2 تساعد في سحبها إلى الأورام، والأدوية التي تحجب هذه الإشارات قد تقلل تراكم البالعات، وإن لم تقضِ عليه تمامًا، مما يشير إلى وجود عوامل جذب أخرى مثل CSF-1 وVEGF. وبمجرد تموضعها، فإن طريقة التصاق البالعات بالمصفوفة المحلية تشكل أيضًا سلوكها. مستقبلات الالتصاق لديها، المسماة الإنتجرينات، لا تعمل كلاصق فقط؛ بل تضخم الإشارات الالتهابية ويمكن أن توجه الخلايا نحو حالات أكثر محاربة للورم. في الوقت نفسه، تفرز البالعات حزمًا صغيرة تسمى الحويصلات خارج الخلوية تحمل RNA وبروتينات إلى الخلايا المجاورة. اعتمادًا على نوع الورم، قد تخفف هذه الحويصلات المناعة وتساعد على الانتشار أو تعزز الاستجابات المضادة للورم، مما يبرز الطابع المعتمد على السياق للتواصل بين البالعات والخلايا الأخرى.
إعادة برمجة البالعات بالجينات والمواد
لأن البالعات تتسرب بطبيعتها إلى الأورام الصلبة أفضل من العديد من الخلايا التائية، يعيد الباحثون الآن تصميمها كعلاجات حية. إحدى الاستراتيجيات الجينية تستعير من علاج الخلايا التائية بمستقبلات المستضد الكيمرية (CAR): إضافة مستقبل اصطناعي لخلق بالعات CAR. تتعرف هذه الخلايا المصممة على علامات الورم، وتبتلع الخلايا السرطانية بكفاءة أكبر، وتهضم المصفوفة المحيطة، وتطلق إشارات التهابية، وتفعّل الخلايا التائية من خلال عرض مستضدات الورم. تُظهر التجارب البشرية المبكرة على بالعات CAR المستهدفة ضد HER2 أمانًا ونشاطًا بيولوجيًا مشجعين، على الرغم من الحاجة لمزيد من العمل لإثبات فوائد قوية وطويلة الأمد. بالتوازي، تستخدم الطرق غير الجينية جسيمات و«حقائب ظهر» مصنوعة من الشحميات أو البوليمرات. يمكن للبالعات ابتلاع جزيئات نانوية محمّلة بالأدوية وحملها عميقًا داخل الأورام كحصان طروادة، أو ارتداء رقع سطحية تُطلق إشارات منشطة للمناعة ببطء، مما يساعدها على الحفاظ على هوية مقاتلة للورم دون تحميل مفرط لمحتواها الداخلي. كما تُختبر الحويصلات المستمدة من البالعات نفسها كناقلات طبيعية خالية من الخلايا.
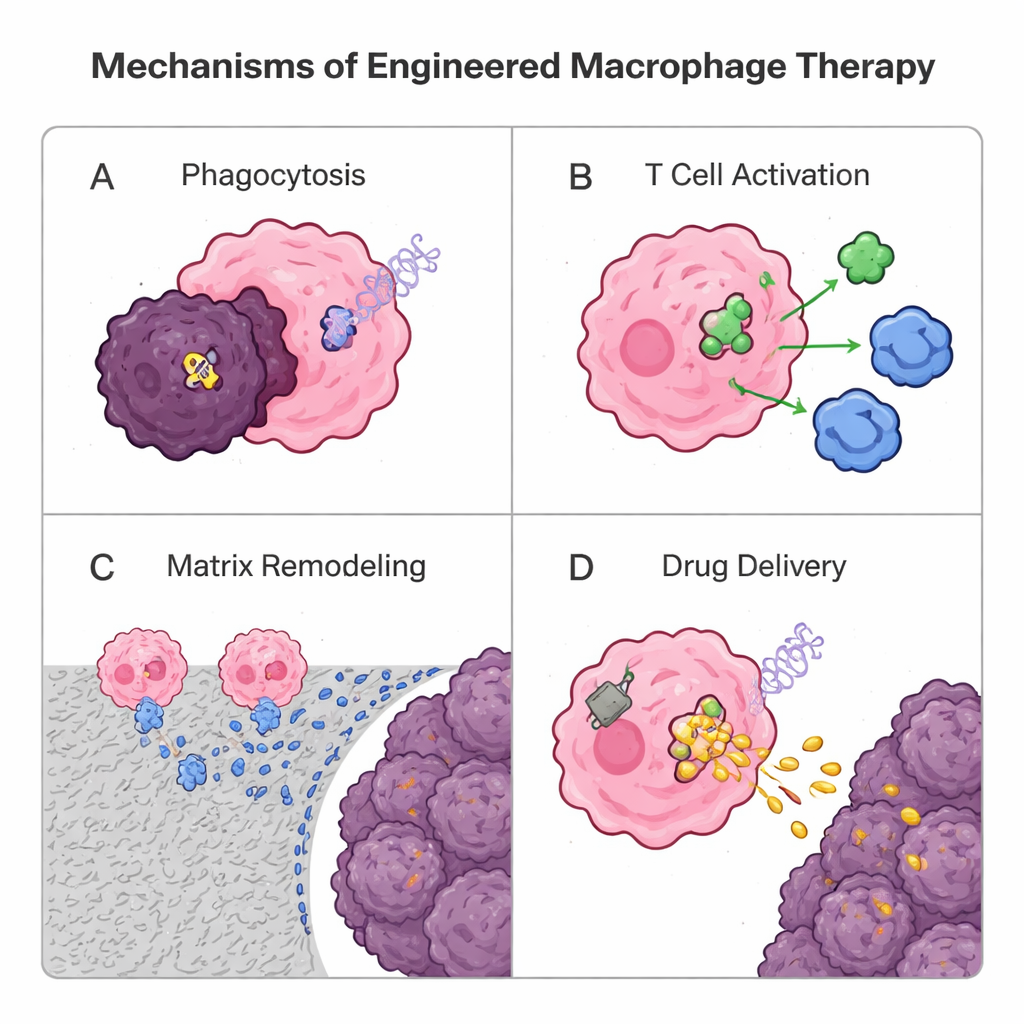
التحديات المقبلة وأسباب التفاؤل
رغم وعودها، يجب أن تتغلب علاجات البالعات على عقبات عملية. يستغرق توليد عدد كافٍ من الخلايا المتسقة من المرضى وقتًا وتكلفة، ومتى أُدخلت لا تعيش هذه الخلايا أو تتكاثر إلى ما لا نهاية. قد تجعل مرونتها المدمجة، رغم فائدتها البيولوجية، من الصعب إبقاؤها محبوسة في وضع مضاد للورم داخل بيئة دقيقة معقدة وقمعية. يجادل المؤلفون بأن النماذج الحيوية المتقدمة—الزرعيات ثلاثية الأبعاد، والأورغانويدات، وأنظمة العضو على رقاقة التي تحاكي ميكانيكا الأنسجة الحقيقية—ستكون حاسمة لفهم وتوقُّع كيف تتصرف البالعات المهندسة في المرضى. ومع ذلك، فإن قدرتها الطبيعية على دخول الأورام الصلبة وابتلاع الخلايا السرطانية وإيقاظ الخلايا التائية، إلى جانب سجل مبكر من الأمان، يشير إلى أن العلاجات القائمة على البالعات قد تصبح سلاحًا جديدًا مهمًا، خصوصًا ضد الأورام «الباردة» التي تقاوم حاليًا معظم علاجات المناعة.
الاستشهاد: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
الكلمات المفتاحية: العلاج المناعي بالبالعات الكبيرة, البيئة الدقيقة للورم, بالعات CAR, الابتلاع الخلوي, توصيل الأدوية بالنانوذرات