Clear Sky Science · ar
علاجات قائمة على الأحماض النووية لاستعادة توازن المفصل في التهاب المفاصل المرتبط بالشيخوخة وما بعد الإصابات
لماذا تحتاج المفاصل المتألمة إلى أنواع جديدة من الأدوية
يُنظر إلى التهاب المفاصل العظمي، الشكل الأكثر شيوعًا من التهاب المفاصل، غالبًا على أنه مجرد «تآكل واهتراء»، لكنه في الواقع مرض معقد حيث ينهار التوازن الطبيعي للمفصل بين التلف والإصلاح. ومع ازدياد طول عمر الناس وبقائهم نشطين لسنوات أطول، أصبحت المفاصل المؤلمة والمتيبسة سببًا رئيسيًا للإعاقة، والعلاجات الحالية في الغالب تخفف الأعراض فقط أو تنتهي باستبدال المفصل المكلف. تستعرض هذه المراجعة فئة جديدة من العلاجات المبنية على تعليمات جينية — خيوط صغيرة من الحمض النووي الريبي — التي تهدف ليس فقط إلى تخفيف الألم، بل إلى استعادة التوازن الصحي داخل المفاصل المتضررة.
من غضروف مهترئ إلى انهيار كامل للمفصل
يُعترف الآن بأن التهاب المفاصل العظمي اضطراب يشمل المفصل بأكمله، وليس مجرد مشكلة في ترقق الغضروف. في ركبة مصابة بالتهاب مفاصل، على سبيل المثال، يتآكل الغضروف الناعم الذي يوسّد العظام، وقد يتعرض الغضروف الهلالي للتقطع، وتزداد سماكة العظم الموجود تحت الغضروف، وقد يصبح بطانة المفصل ملتهبة. هذا الالتهاب المزمن منخفض الدرجة يغذي المرض بهدوء لسنوات. يصف المؤلفون كيف تتفاعل الشيخوخة والإصابة والوزن الزائد والعوامل الوراثية لتدفع المفصل نحو عمليات «قَابِلة للهدم» تكسر النسيج، متغلبةً على العمليات «البنائية» التي تصلحه. وبما أن مرض كل مريض يُحفَّز بمزيج مختلف قليلًا من العوامل، فإن الاستجابة للعلاجات الشائعة مثل المسكنات أو الحقن أو حتى الجراحة تتفاوت إلى حد كبير، ولا يوجد دواء اليوم يمكنه إيقاف التهاب المفاصل العظمي أو عكسه بشكل حقيقي.
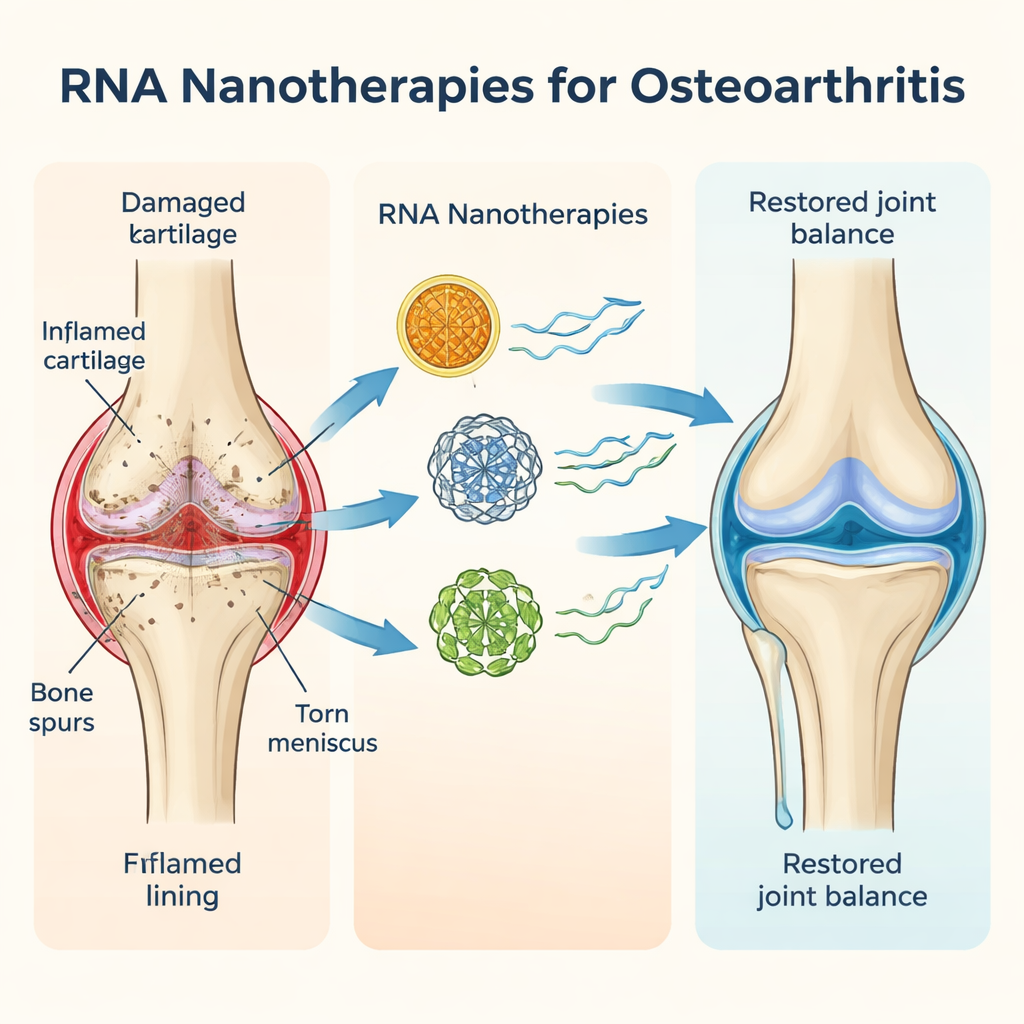
لماذا تقصِر العلاجات التقليدية
تحدد المراجعة العديد من الخيارات الحالية — من حبوب الألم التي تُصرف دون وصفة وحقن الستيرويد إلى العلاج الفيزيائي، والدعامات، وإجراءات متقدمة مثل زراعة الغضروف. لكل منها فوائد، لكن أيضًا عيوب واضحة. قد تُسبب مسكنات الألم تهيجًا في المعدة أو مشاكل قلبية، وقد تتلف الستيرويدات الغضروف عند الاستخدام المتكرر، وتُعد الطرق التجديدية مثل البلازما الغنية بالصفائح الدموية أو الخلايا الجذعية مكلفة وتفتقر إلى دليل طويل الأمد. والأهم من ذلك أن معظم الأدوية الحالية تتعامل مع جانب واحد فقط من المشكلة: إما تهدئ الالتهاب وتبطئ التحلل، أو تحاول تعزيز الإصلاح. ونادرًا ما تهدف النهج إلى مهاجمة الجانبين معًا، وهو ما يفسر على الأرجح صعوبة تغيير مسار المرض.
أدوية الـRNA: إعادة كتابة النص الداخلي للمفصل
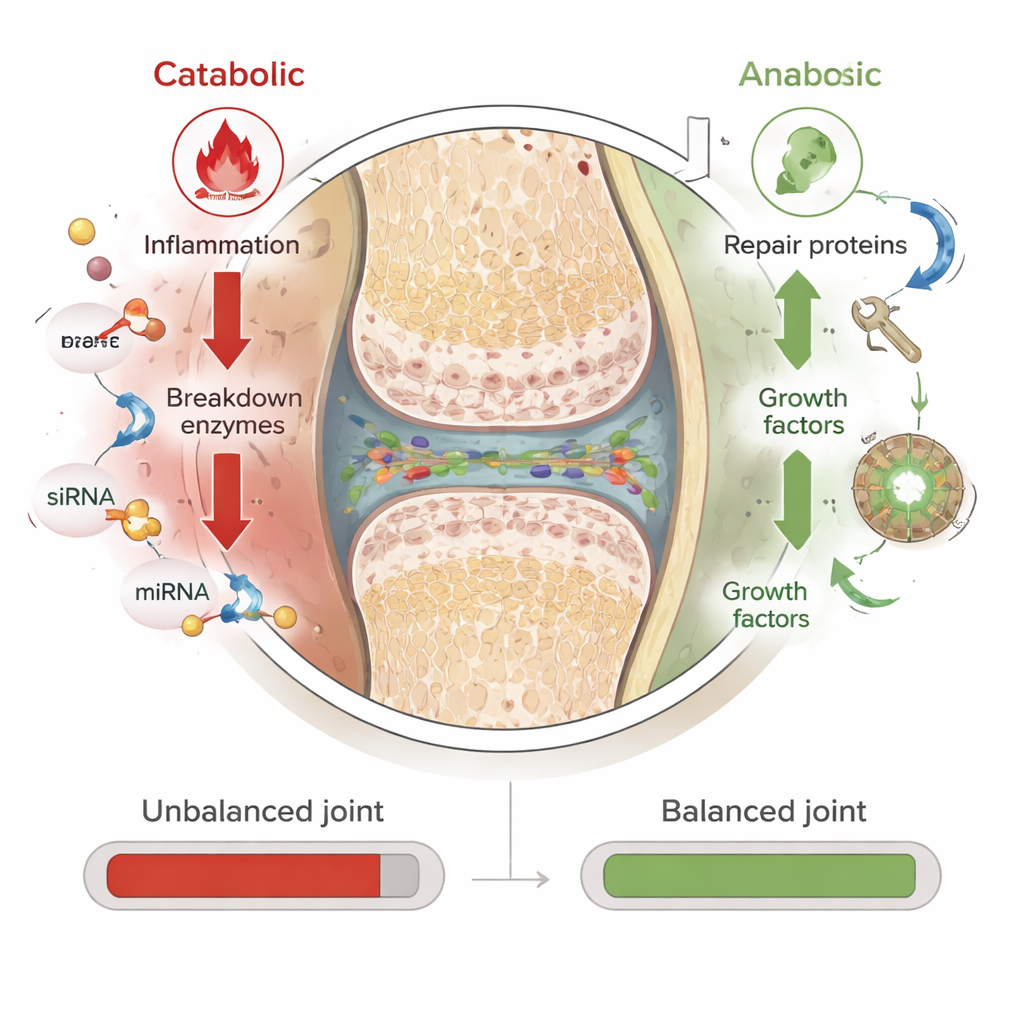
تعمل العلاجات القائمة على الـRNA على مستوى مختلف. فبدلاً من استهداف البروتينات بعد تكونها، فإنها تؤثر في الرسائل الجينية قصيرة العمر التي تخبر الخلايا أي بروتينات تصنع. يركز المؤلفون على ثلاثة أنواع. يمكن لـRNA متداخل صغير (siRNA) إسكات جين واحد ضار بدقة عالية. يمكن للميكروRNA (miRNA) ضبط شبكات كاملة من الجينات بشكل دقيق، موجهًا مسارات ضارة متعددة إلى الانخفاض في آن واحد. أما الـmRNA فيعمل بالعكس: يوفر تعليمات لصنع بروتينات مفيدة، مثل عوامل النمو التي تحفز إصلاح الغضروف أو الجزيئات التي تحجب إشارات الالتهاب. وبما أن تأثيرات الـRNA مؤقتة ولا تغير الـDNA، فهي قابلة للعكس ومبدئيًا أكثر أمانًا من التعديل الجيني الدائم. وبالاستفادة من نجاح لقاحات mRNA لفيروس كوفيد-19، يختبر الباحثون الآن أفكارًا مماثلة في نماذج حيوانية لالتهاب المفاصل.
الجسيمات النانوية: إيصال الرسائل الهشة إلى الخلايا المناسبة
تتمثل تحديات رئيسية في أن الـRNA العاري هش ولا يمكنه اختراق الخلايا بسهولة. تصف المراجعة كيف يقوم العلماء بتعبئة الـRNA داخل «منصات نانوية» واقية — حوامل دقيقة مصنوعة من دهون أو بوليمرات أو ببتيدات قصيرة. تحمي هذه الجسيمات النانوية الـRNA من التحلل، وتساعده على المرور عبر مصفوفة الغضروف الكثيفة، وتشجع خلايا بطانة المفصل والغضروف على امتصاصه. في دراسات قبل إكلينيكية، استخدمت جزيئات محملة بـsiRNA لإيقاف جينات تدعم الالتهاب والإجهاد التأكسدي وتحلل النسيج، بينما عززت الجسيمات المحملة بـmRNA بروتينات واقية تشجع التزليق والإصلاح. أظهرت التجارب المبكرة انخفاضًا في تلف الغضروف والألم في النماذج الحيوانية، مما يوحي بأن مجموعات مصممة بعناية من RNAs المضادة للتحلل والمحفزة للإصلاح قد تعمل يومًا ما كعلاجات معدلة للمسار المرضي.
العقبات في طريق الوصول إلى العيادة
بالرغم من وعودها، لا تزال علاجات الـRNA النانوية لالتهاب المفاصل العظمي تواجه عقبات مهمة. فقد يخطئ الجهاز المناعي في تشخيص كل من الـRNA وحامله كغزاة، مما يثير التهابًا غير مرغوب فيه في مفاصل مصابة بالفعل. تُزال الحقن داخل المفصل خلال أيام إلى أسابيع، لذا من المرجح أن تتطلب الفوائد طويلة الأمد أنظمة إطلاق بطيء أذكى أو جرعات متكررة. كما أن تصنيع RNA وجسيمات نانوية عالية الجودة على نطاق واسع مكلف، ولدى الجهات التنظيمية خبرة محدودة في تقييم مثل هذه الأدوية لأمراض مفاصل تتقدم ببطء. وأخيرًا، لأن التهاب المفاصل العظمي متباين بشدة من شخص لآخر، سيتطلب الأمر طرقًا أفضل لمطابقة خلطات RNA الخاصة مع نمط تلف والتهاب المفصل الفريد لدى كل مريض.
ماذا يعني هذا للأشخاص المصابين بالتهاب المفاصل
بعبارة بسيطة، يجادل هذا المقال بأن لعلاج الأشخاص المصابين بالتهاب المفاصل العظمي بفعالية، يجب أن تفعل العلاجات المستقبلية أكثر من تخفيف الألم—عليها استعادة التوازن المفقود للمفصل عن طريق خفض نشاط الجينات التي تسبب التلف وزيادة نشاط الجينات التي تدعم الإصلاح. توفر الأدوية القائمة على الـRNA، والمقدمة بواسطة حوامل جسيمية نانوية متقدمة، مجموعة أدوات مرنة لتحقيق ذلك. وبينما لم تصبح جاهزة بعد للاستخدام العيادي ولا تزال هناك أسئلة مهمة تتعلق بالسلامة والمتانة والتكلفة والتنظيم، يراها المؤلفون طريقًا واقعيًا نحو علاجات مخصصة وقليلة التدخل قد تؤخر أو حتى تمنع الحاجة لاستبدال المفصل في حالات التهاب المفاصل المرتبطة بالعمر أو الناتجة عن إصابة.
الاستشهاد: Rai, M.F., Pham, C.T., Hou, K. et al. Nucleic acid-based therapeutics to restore joint homeostasis in age-related and post-traumatic arthritis. npj Biomed. Innov. 3, 17 (2026). https://doi.org/10.1038/s44385-026-00068-8
الكلمات المفتاحية: التهاب المفاصل العظمي, علاجات الحمض النووي الريبي, الطب النانوي, تجديد المفصل, siRNA mRNA miRNA