Clear Sky Science · ar
التحويل الكيميائي-الميكانيكي خارج التوازن لفك طي البروتين المدفوع بـATP في البروتيزوم 26S
كيف يحافظ آلة صغيرة على ترتيب بروتيناتنا
داخل كل خلية، جهاز تمزيق مجهري يُسمى البروتيزوم 26S يدمر باستمرار البروتينات التالفة أو غير المطلوبة بعد الآن، محافظًا على صحة الخلية. في قلب هذه الآلة حلقة من المحركات تحرق وقودًا كيميائيًا (ATP) لتُمسك البروتينات، وتفك طيها، وتسحبها إلى حجرة مركزية حيث تُقسَّم إلى قطع. تستخدم هذه الورقة محاكاة حاسوبية متقدمة لتكشف كيف يحوّل هذا المحرك الطاقة الكيميائية إلى حركة ميكانيكية، مقدمة صورة تفصيلية كمية لعملية تشكل أساس الشيخوخة وأمراض الدماغ والمناعة والسرطان.
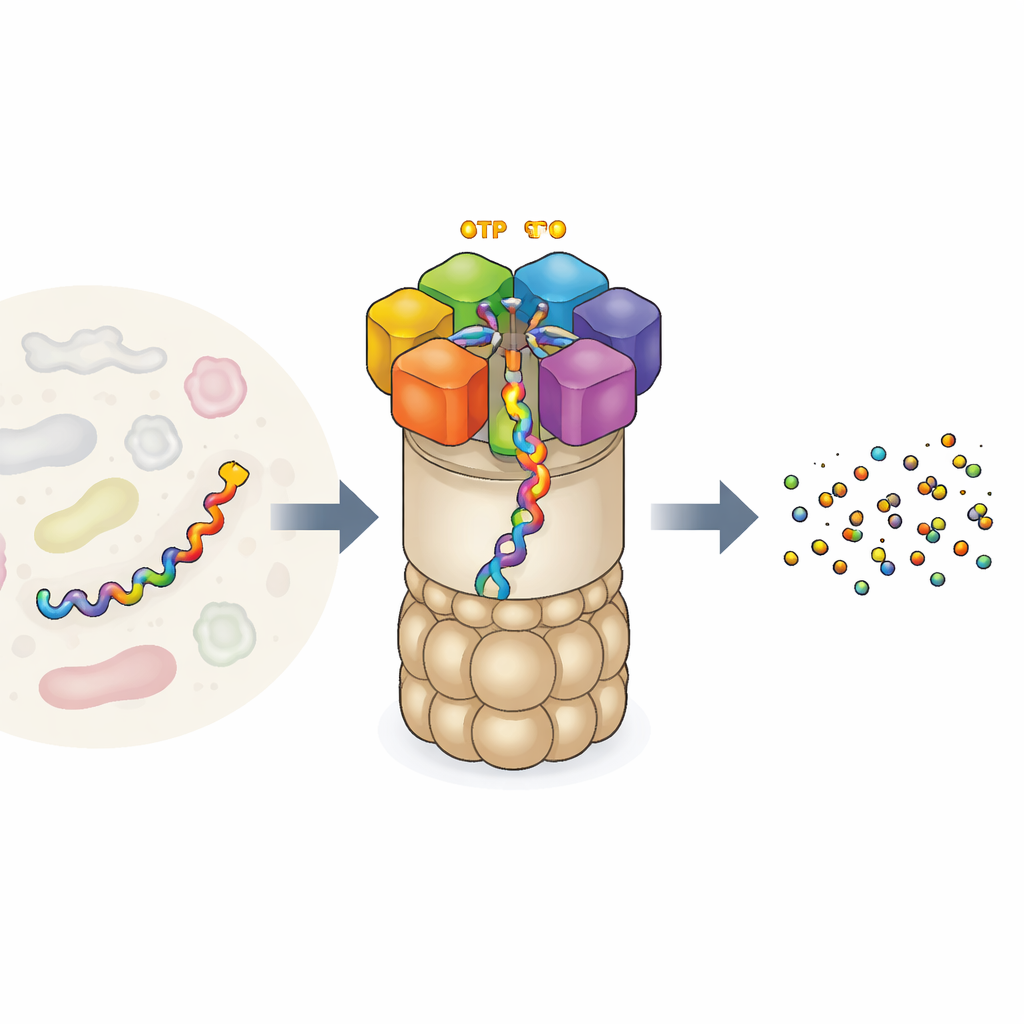
مصنع إعادة تدوير البروتينات في الخلية
يعد البروتيزوم 26S واحدًا من أكبر وأعقد الآلات البروتينية في خلايانا. يتكوّن من نواة على شكل برميل تقطع البروتينات وغطاء تنظيمي يتعرف على البروتينات التي يجب تدميرها. عند بوابة الدخول توجد حلقة تتألف من ست وحدات محرك مختلفة. يمكن لكل وحدة أن تَرْتبط بـATP، عملة الطاقة العالمية للخلية، وتستخدم تلك الطاقة لتثبّت سلسلة البروتين وتسحبها إلى النواة للتفكك. لا يتصرف هذا المحرك عشوائيًا: أشارت تجارب سابقة إلى أن الوحدات الست تعمل بتنسيق بطريقة “يد فوق يد”، تمرر البروتين كما يفعل المتسلقون على حبل. لكن التجارب أظهرت فقط لقطات قليلة من هذا الإجراء، تاركة أسئلة عن التسلسل الكامل للحركات وكيف يُرتبط بالضبط حرق الوقود بالعمل الميكانيكي.
محاكاة شد الحبل الجزيئية
بنى المؤلفون نموذجًا احتماليًا على الحاسوب يعامل المحرك كنظام ينتقل بين أشكالٍ ممكنة عديدة بينما ترتبط وتتفكك جزيئات ATP ومنتجاتها. عرّفوا 30 حالة تَشكُّل رئيسية للحلقة يُفقد فيها واحد أو اثنان أو ثلاثة من وَحدات المحرك قبضتهم على البروتين، بالإضافة إلى حالة مغلقة بإحكام خاصة تُمسك فيها جميع الوحدات الست. باستخدام خوارزمية معيارية لمحاكاة الأحداث الكيميائية العشوائية، تتبعوا مئات الآلاف من الخطوات التي تحدث فيها ربط ATP، وتحطيم ATP، وتغيرات شكل المحرك. من هذه المسارات استطاعوا التنبؤ بسرعة سحب البروتين تحت ظروف مختلفة، مثل اختلاف كميات ATP وشكله المنفق ADP ونظير ATP غير القابل للتحلل المستخدم غالبًا في التجارب.
عندما يبطئ فائض الوقود المحرك
أعادت المحاكاة إنتاج عدة نتائج تجريبية محيرة. مع ارتفاع مستويات ATP من قيم منخفضة، يسحب المحرك البروتينات بسرعة أكبر لأن ربط الوقود هو الخطوة البطيئة. لكن عند تجاوز نحو 1 مليمولار من ATP، تبلغ السرعة ذروتها ثم تنخفض: تقضي الحلقة مزيدًا من الوقت في حالة عالِقَة لا تُنقِل فيها البروتين رغم احتلال جميع الوحدات الست بـATP. إضافة ADP أو النظير غير القابل للتحلل لـATP يبطئ المحرك باستمرار، لأن هذه الجزيئات تتنافس مع ATP على مواقع الارتباط لكنها لا تكمل خطوة القوة الكاملة. كما يتنبأ النموذج بكيفية تصرف المحرك عند مواجهة مناطق من البروتين مطوية بإحكام، تعمل كعوائق. في هذه الحالات، يقضي المحرك وقتًا أطول في المجادلة مع المقاومة، وينخفض معدل التحلل الكلي، مطابقًا لقياسات على نطاقات بروتينية مُثبتة اصطناعيًا.
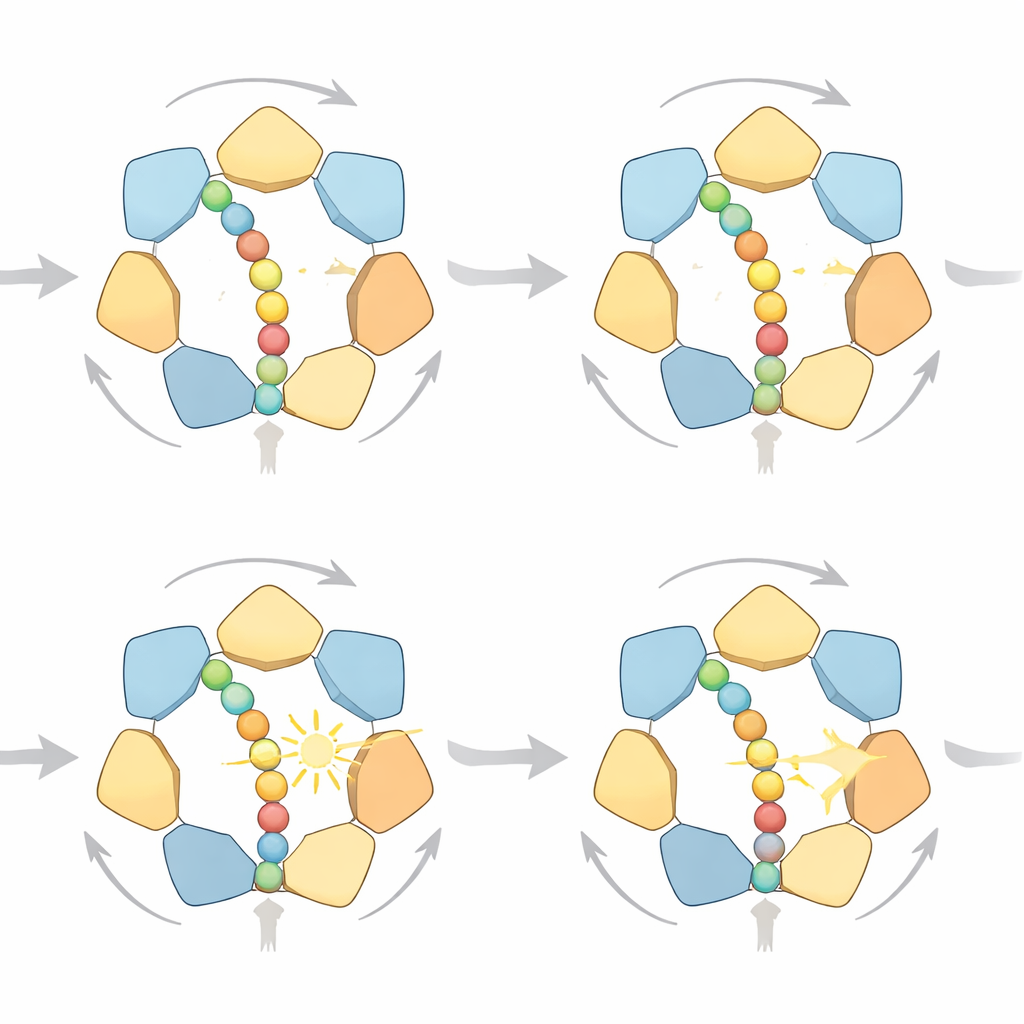
طرق متعددة لأخذ خطوة
من خلال فحص المسارات المحاكاة بالتفصيل، وجد الباحثون أن الحلقة لا تتبع دورة صارمة واحدة. بدلًا من ذلك، توجد مسارات متعددة ذات احتمالية عالية تلتزم جميعها بنفس قاعدة “يد فوق يد” الاتجاهية: تطلق الوحدات قرب مخرج الحلقة البروتين بعد تحلل ATP، تنتقل إلى قمة سلم لولبي من الوحدات، وتعيد الإمساك بالسلسلة أعلى قليلًا. أحيانًا يتقدم البروتين بخطوة صغيرة واحدة، وأحيانًا بخطوتين، اعتمادًا على عدد الوحدات التي تترك الإمساك معًا. عند وفرة الوقود، تهيمن الحركات ذات الخطوة الواحدة لأنها تُهدر طاقة أقل مقابل القوى المعاكسة؛ وعندما يكون الوقود شحيحًا، يتنبأ النموذج بقفزات ثنائية أكثر تكرارًا. كما تربط المحاكاة الحمل الميكانيكي بالحالة الكيميائية للمحرك: مع زيادة المقاومة وتوقف تقدم البروتين، يميل ADP إلى التراكم في مزيد من مواقع الارتباط الست — وهو ما تلاحظه الدراسات البنائية عالية الدقة بالضبط.
استخدام الطاقة وقواعد التصميم المشتركة
يتيح النموذج للمؤلفين رسم كيف ترتفع طاقة المحرك عند تحلل ATP وتنخفض عندما تُحوّل تلك الطاقة إلى حركة. حسبوا منحنى كفاءة يُظهر أن المحرك يعمل بأفضل شكل عند قوة معاكسة متوسطة: مقاومة قليلة جدًا فَيُهدر ATP؛ ومقاومة كبيرة جدًا فتتوقف الآلة تقريبًا. عندما قارن الفريق تنبؤاتهم ببيانات من آلات مدمرة للبروتين ذات صلة في البكتيريا والخباز (الخميرة)، وجدوا اتجاهات مشابهة جدًا في كيفية إبطاء هذه المحركات بنظير ATP غير القابل للتحلل. يشير هذا إلى أن العديد من أفراد عائلة هذه الإنزيمات الحلقية قد تشترك على الأرجح في آلية محكمة ومحفوظة لسحب البروتينات.
لماذا يهم هذا للصحة والمرض
من خلال تحويل لقطات بنيوية متفرقة وقياسات بيوكيميائية إلى إطار عمل موحد وقابل للاختبار، يظهر هذا العمل بالتفصيل الكمي كيف يترجم محرك جزيئي صغير الوقود الكيميائي إلى قوة لإعادة تدوير بروتينات الخلية. لا يفسر النموذج مجموعة واسعة من التجارب الحالية فحسب، بل يقدم أيضًا تنبؤات حول كيفية تأثير تغيّر مستويات الوقود أو الحمل الميكانيكي أو طفرات المحرك على تدمير البروتين. ونظرًا لأن آلات مشابهة تعمل عبر أشكال الحياة كافة وتلعب دورًا مركزيًا في حالات مثل التنكس العصبي والسرطان، فقد يساعد فهم آلياتها الداخلية بهذا المستوى في نهاية المطاف على تصميم أدوية تضبط أو تعزز أو تحجب انتقائيًا هذه الممزقات المجهريّة.
الاستشهاد: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
الكلمات المفتاحية: بروتيزوم, محرك AAA+ ATPase, تحلل البروتين, آلات جزيئية, الاقتران الكيميائي-الميكانيكي