Clear Sky Science · ar
مستشعر حيوي ميكروفلويدي قائم على أعضاء دقيقة لمراقبة مستويات الجلوكوز بشكل مستمر في الجسم الحي
لماذا يهم هذا الأشخاص المصابين بالسكري
بالنسبة للأشخاص الذين يعيشون مع داء السكري من النوع الأول، لا تزال أنظمة «البنكرياس الاصطناعي» الحالية تتطلب مراقبة مستمرة — إعلان الوجبات، التعامل مع إنذارات، والقلق من انخفاض سكر الدم أثناء الليل. تستكشف هذه الدراسة نوعًا مختلفًا جذريًا من حسّاسات الجلوكوز التي لا تعتمد على إنزيم واحد أو معادلة حاسوبية، بل تستعير قطعة حية صغيرة من آلية الجسم نفسها للتحكم بالسكر: مجموعات من خلايا البنكرياس تُسمى الجزر. من خلال السماح لهذه الأعضاء الدقيقة بأن تقوم بما صقلته لها التطور، يهدف الباحثون إلى بناء مراقبات جلوكوز أذكى وأكثر أمانًا قد تعمل يومًا ما بشكل أكثر استقلالية في الخلفية.
عضو صغير كحسّاس حي
تكتشف معظم أجهزة الاستشعار الحيوية الحالية المواد الكيميائية باستخدام جزيئات نقية أو خطوط خلوية واحدة. تستجيب لمادة محددة ثم تمرِّر الإشارة الخام إلى برنامج يحاول تفسيرها. يجادل المؤلفون بأن هذا النهج يتجاهل «حاسوب» قوي مضمّن: أعضاء دقيقة مثل جزر البنكرياس، التي تستشعر بشكل طبيعي إشارات متعددة في آن واحد وتحولها إلى استجابة منسقة. تحتوي كل جزيرة على عدة أنواع من الخلايا المنتجة للهرمونات التي تتواصل مع بعضها باستمرار. معًا تحافظ على سكر الدم ضمن نطاق ضيّق وآمن، فتستجيب ليس للجلوكوز فحسب، بل أيضًا للأحماض الأمينية وهرمونات الأمعاء والضغط ولتاريخ الجسم الحديث من الفترات المرتفعة والمنخفضة. يقترحون أن هذه التعقيدات المدمجة يمكن استغلالها لإنتاج معلومات أغنى وأكثر موثوقية من حسّاس أكسيد الجلوكوز البسيط.
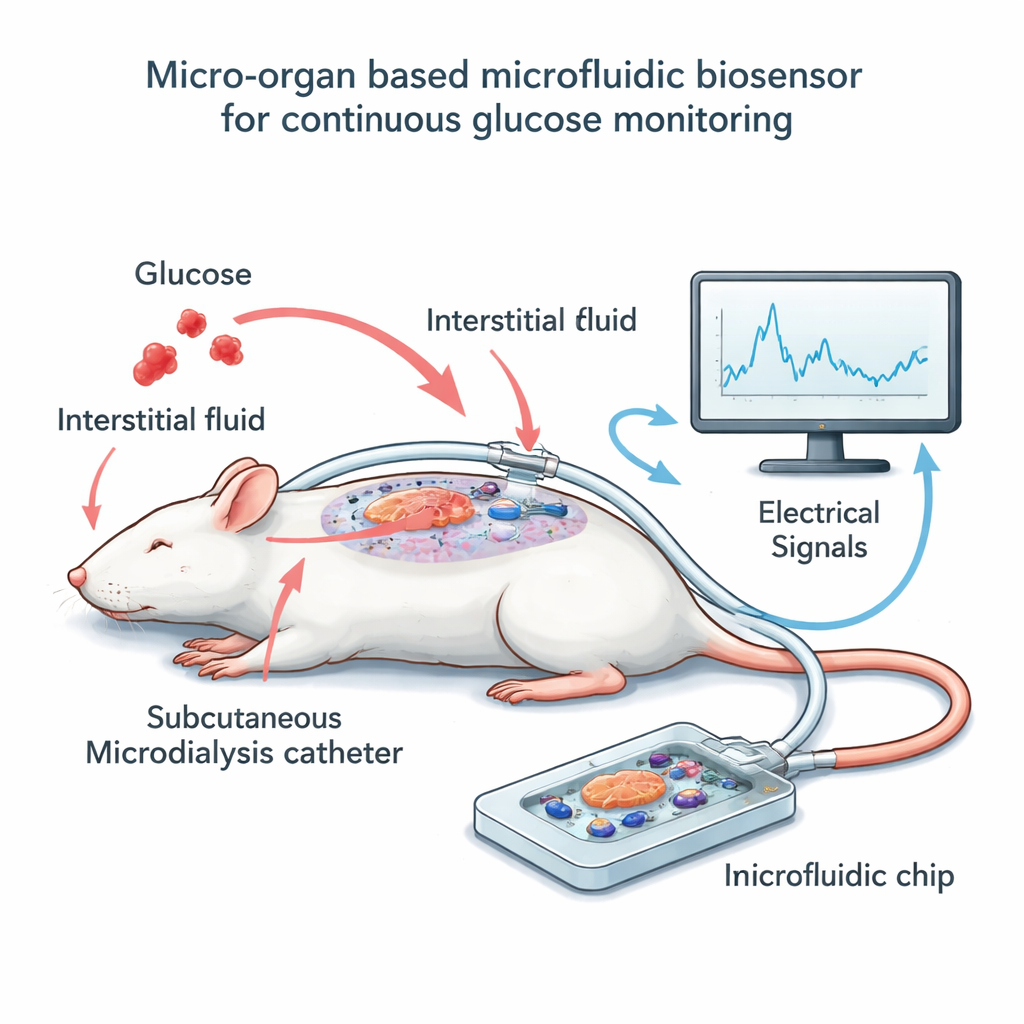
بناء نظام الشريحة والقسطرة
لاختبار هذه الفكرة، بنى الفريق جهازًا صغيرًا خارج الجسم يضم بضع عشرات من جزر الفئران فوق شبكة من الأقطاب الصغيرة المجهرية. بدلًا من غمر هذه الخلايا مباشرة في الدم، استخدموا تقنية تسمى الغسيل المجهري (microdialysis): قسطرة رفيعة ومرنة تقع تحت جلد جرذان مُخدَّرة وتجمع ببطء سائل الأنسجة المحيط، الذي يتتبع سكر الدم عن قرب لكنه مع تأخير قصير. يتدفق هذا السائل بمعدل ثابت ومنخفض عبر قناة ضيقة فوق الجزر على الشريحة. مع ارتفاع وانخفاض مستويات الجلوكوز في سائل الغسيل، تغيرت نشاطات الجزر الكهربائية، والتي تلتقطها الأقطاب كإشارات بطيئة على شكل موجات. بالتوازي، قاس الباحثون دوريًا الجلوكوز في دم الجرذان وفي سائل الغسيل، مما سمح لهم بمطابقة القراءة الكهربائية مع مستويات السكر الفعلية عبر الزمن.
كيف استجاب الحساس الحي لتغيرات السكر
أولًا، اختبر العلماء ما إذا كانت الجزر على الأقطاب قادرة على الاستجابة لمكونات دم حقيقية بدلًا من محاليل مخبرية بسيطة. عرضوها لمصل بشري وفأري بمستويات جلوكوز مختلفة ولاحظوا تغيّرات متدرجة وواضحة في كل من تكرار وحجم موجاتهم الكهربائية. كانت الاستجابات قوية بما يكفي لتمييز خطوات صغيرة في تركيز السكر عبر النطاق ذي الصلة بالسكري. ثم انتقلوا إلى تجارب على الفئران، حيث أعطوا حقنة جلوكوز لرفع سكر الدم ولاحقًا حقنوا إنسولين لخفضه. بعد مراعاة الوقت الذي يستغرقه الجلوكوز للانتقال من الدم إلى سائل الأنسجة ومن خلال الأنابيب، وجدوا أن تكرار الإشارات الكهربائية البطيئة للجزر ارتفع وانخفض بشكل يكاد يكون متزامنًا مع سكر الدم. أظهر التحليل الإحصائي عبر عدة حيوانات علاقة محكمة وقابلة للتكرار بشكل ملحوظ بين تكرار الإشارة ومستوى الجلوكوز، بينما كان سعة الإشارة، على الرغم من كونها مفيدة، أكثر تقلبًا إلى حد ما.
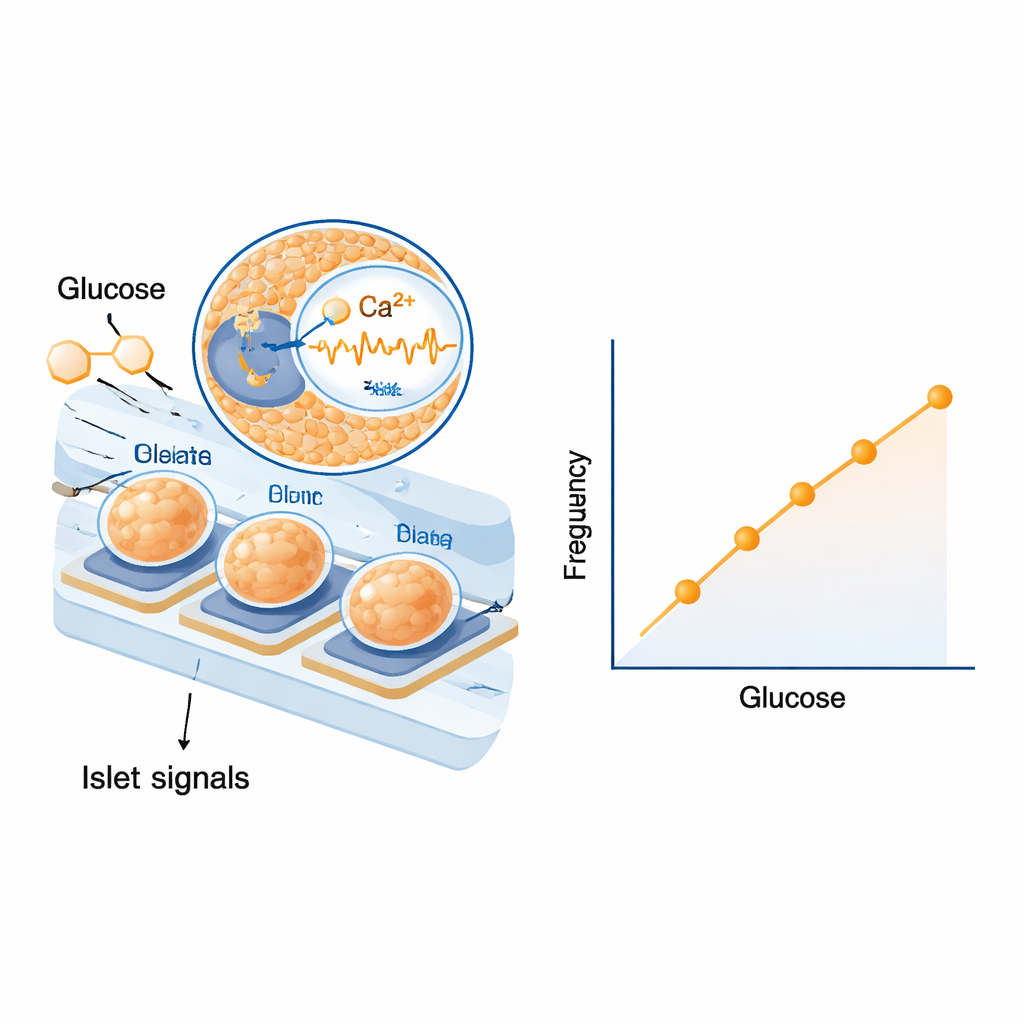
ميزات أمان مدمجة من البيولوجيا
ميزة مهمة لاستخدام الجزر الكاملة بدلاً من جزيء واحد هي أن سلوكها يتضمن بالفعل آليات أمان شكلتها قوى الانتقاء الطبيعي. تظهر أعمال سابقة، وإشارات من هذه الدراسة، أن الجزر تتفاعل بقوة أكبر عندما ينخفض الجلوكوز مقارنة عندما يرتفع — شكل من أشكال «الذِهان المتبقي» (hysteresis) الذي يساعد على الحماية من نقص السكر الخطير. تُشكِّل الأنماط الكهربائية أيضًا عن طريق أنواع الخلايا المجاورة التي تكبّر أو تخفف إفراز الإنسولين حسب حاجة الجسم. وبما أن الشريحة تكتفي بالاستماع لهذه الإشارات المندمجة دون إضافة أصباغ أو تعديلات جينية، يمكنها التسجيل لأيام دون إلحاق ضرر بالخلايا. يشير المؤلفون إلى تحديات تقنية قادمة، مثل تجنب فقاعات الهواء، وضمان أداء الغسيل المجهري على المدى الطويل، وتحديد أي نوع من الجزر البشرية أو المشتقة من الخلايا الجذعية ينبغي استخدامه أخيرًا. ومع ذلك، تشير محاكاة حاسوبية باستخدام نموذج سكري معتمد إلى أن مثل هذا المستشعر القائم على الجزر قد يضاهي أو حتى يتفوق على أجهزة مراقبة الجلوكوز الحالية في الظروف الصعبة.
ماذا قد يعني هذا لرعاية السكري مستقبلاً
تُظهر هذه الدراسة أن حفنة من أعضاء البنكرياس الدقيقة، المُحافَظ على حيويتها على شريحة صغيرة ومتصلة بالجسم عبر قسطرة رفيعة، يمكنها تتبع سكر الدم بشكل مستمر في حيوانات حية عبر همهمة كهربائية طبيعية. للمتخصص غير المختص، الرسالة الأساسية هي أنه بدلًا من مطالبة حسّاس كيميائي بسيط بقياس الجلوكوز ثم إجبار حاسوب على التخمين فيما يعنيه ذلك للجسم، يستمع هذا النهج مباشرة إلى نفس النوع من الأنسجة الحية التي تقرر عادة كمية الإنسولين المطلوب إفرازها. إذا تم تحسينه وجعله عمليًا للاستخدام البشري، فقد تصبح مثل هذه الحساسات الحية جوهر أنظمة البنكرياس الاصطناعي المستقلة حقًا — أجهزة تتوقع بهدوء احتياجات الجسم وتقلل العبء اليومي لإدارة السكري.
الاستشهاد: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
الكلمات المفتاحية: المراقبة المستمرة للجلوكوز, البنكرياس الاصطناعي, جزر البنكرياس, مستشعر حيوي ميكروفلويدي, داء السكري النوع 1