Clear Sky Science · ar
تقنيات تصوير متقدمة للملاحة داخلية الجراحة الأورامية
رؤية السرطان بوضوح أكبر داخل غرفة العمليات
غالبًا ما تتعلق جراحة السرطان بمفاضلة حساسة: إزالة كل خلية سرطانية ممكنة مع الحفاظ على أكبر قدر ممكن من الأنسجة السليمة. يشرح هذا المقال الاستعراضي كيف تساعد جيل جديد من أدوات التصوير الجراحين على رؤية الأورام وحوافها في الوقت الحقيقي أثناء العملية. بالنسبة للقارئ العام، الجاذبية واضحة — هذه التقنيات تعد بعمليات تكرار أقل، وإزالة أكثر دقة للأورام، وفرص أفضل للبقاء على المدى الطويل، كل ذلك من خلال تزويد الجراحين بـ «خريطة» أوضح أثناء العمل.
لماذا تهم رؤية أفضل أثناء الجراحة
أصبح السرطان الآن من بين أكثر أسباب الوفاة شيوعًا في العالم، وتبقى الجراحة ركيزة أساسية للعلاج. ومع ذلك، لطالما اقتصر الجراح الماهر على ما يمكن رؤيته ولمسه يدويًا، وعلى الفحوصات التي أُجريت قبل أيام أو أسابيع من العملية. تساعد الأدوات التقليدية مثل الموجات فوق الصوتية وCT وMRI وPET في تخطيط الجراحة، لكنها غالبًا ما تكون ضخمة أو بطيئة أو غير مناسبة للاستخدام المستمر أثناء العملية. ونتيجة لذلك، قد يكون من الصعب تحديد نقطة انتهاء الورم وبداية النسيج السليم بدقة، مما يزيد من مخاطر ترك السرطان خلفه أو استئصال كمية كبيرة من النسيج الطبيعي. يبيّن الاستعراض كيف يغيّر «التصوير أثناء العملية» — أي التصوير الحي المستخدم داخل غرفة العمليات — هذه المعادلة.
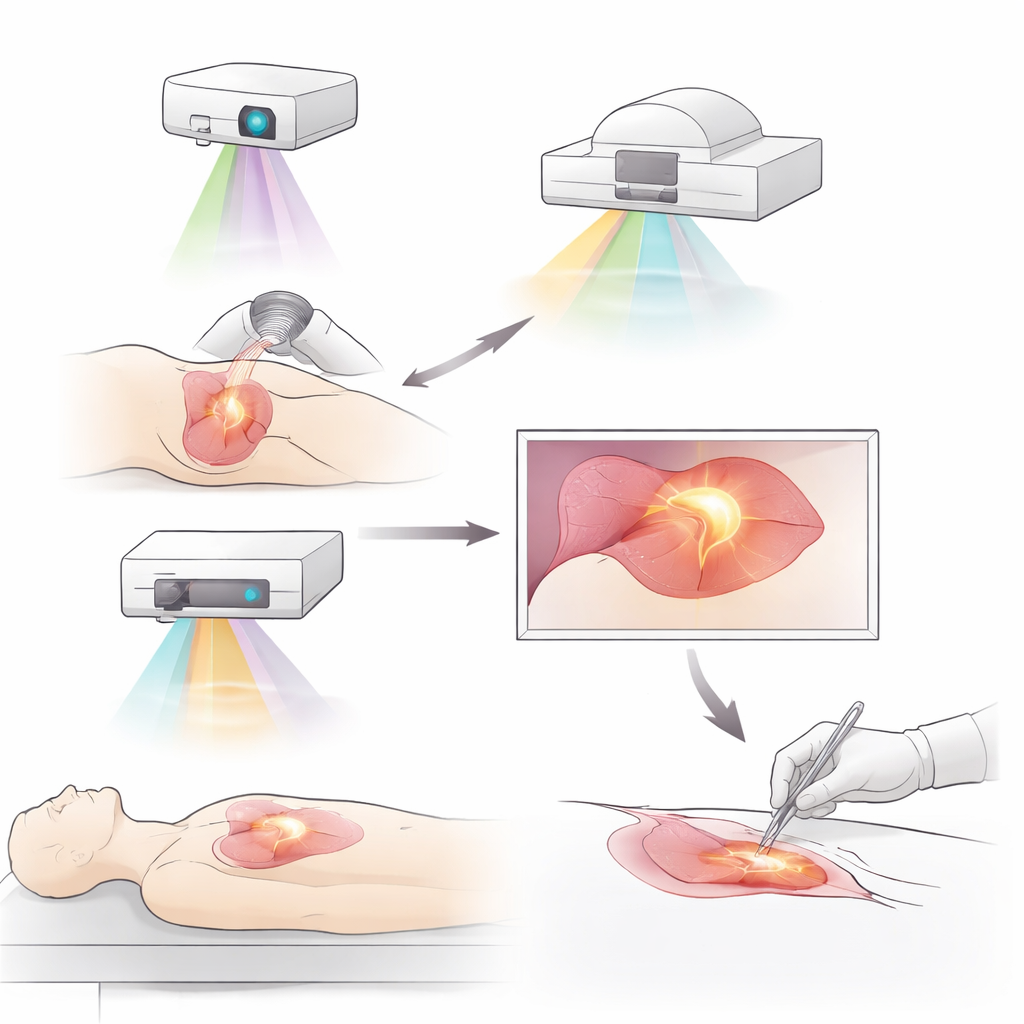
أورام متألقة وطرق جديدة لإنارتها
أحد التطورات الرئيسية هو تصوير التألق، حيث تجعل أصباغ خاصة أو مجسات جزيئية الأورام تتوهج تحت ضوء الأشعة تحت الحمراء القريبة. ساعدت الأصباغ القديمة غير الموجهة مثل الإندوسيانين غرين الجراحين بالفعل على تحديد محيط الأورام، وتتبع أوعية الليمف، والعثور على العقد اللمفاوية الحاسمة في سرطانات الثدي والكبد والرئة والمعدة. تتقدم المجسات الموجهة الأحدث أكثر باصطيادها لجزيئات يفرزها خليط الأورام أو بيئتها المحيطة بكثرة. من أمثلة ذلك مجسات تلتصق بمستقبلات عوامل النمو، أو بنقاط تفتيش مناعية، أو ببروتينات وفيرة في نسيج الدعامة الورمية أو في المناطق منخفضة الأكسجين. يمكن ربط بعض هذه العوامل حتى بعقاقير مضادة للسرطان، لتجمع بين التصوير الدقيق والعلاج داخل جزيء واحد. تُظهر التجارب السريرية المبكرة أن مثل هذه المتتبعات يمكن أن تكشف ترسبات أورامية مخفية وتقلل الحاجة لإجراء جراحات تكرارية بعد عمليات الحفاظ على الثدي.
أبعد من اللمعان: صوت، ضوء، وألوان متعددة
بينما يحتل التصوير اللامع مكانًا مركزيًا، يبرز الاستعراض عدة مناهج مكمِّلة ترى جوانب مختلفة من الورم. يستخدم التصوير الضوئي الصوتي دفعات من الضوء لتوليد موجات صوتية داخل النسيج، مجمِّعًا بين تفاصيل الطرق البصرية ومدى اختراق الموجات فوق الصوتية، وقد نجح في كشف نقائل صغيرة جدًا تفوتها فحوصات أخرى. يقوم التصوير الطيفي متعدد النطاقات والتصوير الطيفي الفائق بتقسيم الضوء إلى نطاقات عديدة، ملتقطًا اختلافات دقيقة في امتصاص وتعكس الأنسجة للضوء؛ ما يمكن أن يميز السرطان عن النسيج الطبيعي بدقة عالية في أورام الثدي وعنق الرحم والجهاز الهضمي. تضيف تقدمات الموجات فوق الصوتية — بما في ذلك تقنيات تقيس صلابة النسيج — معلومات عمقية وتساعد على إظهار مدى تغلغل السرطان. يقدم مطياف رامان، الذي يقرأ «بصمة» كيميائية للنسيج استنادًا إلى تشتت الجزيئات للضوء، تمييزًا عالي التحديد للسرطان أثناء الجراحة بدون ملصقات، خاصة عند الجمع بينه وبين وسائط أخرى.
بناء خرائط ثلاثية الأبعاد ودمج عروض متعددة
ثيمة أخرى في المقال هي دمج الصور في عروض ثلاثية الأبعاد ومتعددة الوسائط يمكن للجراحين استخدامها بشكل بديهي. تساعد إعادة البناء ثلاثي الأبعاد للأوعية الدموية وقنوات اللمف والأعضاء، المكسوة بإشارات متألقة، على تخطيط استأصال أجزاء محددة من الكبد والرئة وتوجيه استئصال العقد اللمفاوية الصعب. تسمح الأنظمة الهجينة التي تدمج PET مع التصوير البصري أو تقترن متتبعات الطب النووي بالتألق باستخدام نفس المجس لفحص الجسم بأكمله قبل العملية وتوجيه الجراحة داخلها. تدمج المنصات الناشئة الاستئصال بالليزر، تصوير التماسك البصري، والروبوتات لتحديد ومعالجة الآفات تلقائيًا بدقة عالية. تهدف هذه الطرق إلى تزويد الجراحين كلًا من «الصورة الكبيرة» لانتشار الورم والتفاصيل الدقيقة اللازمة للقطع على حواف آمنة ونظيفة.
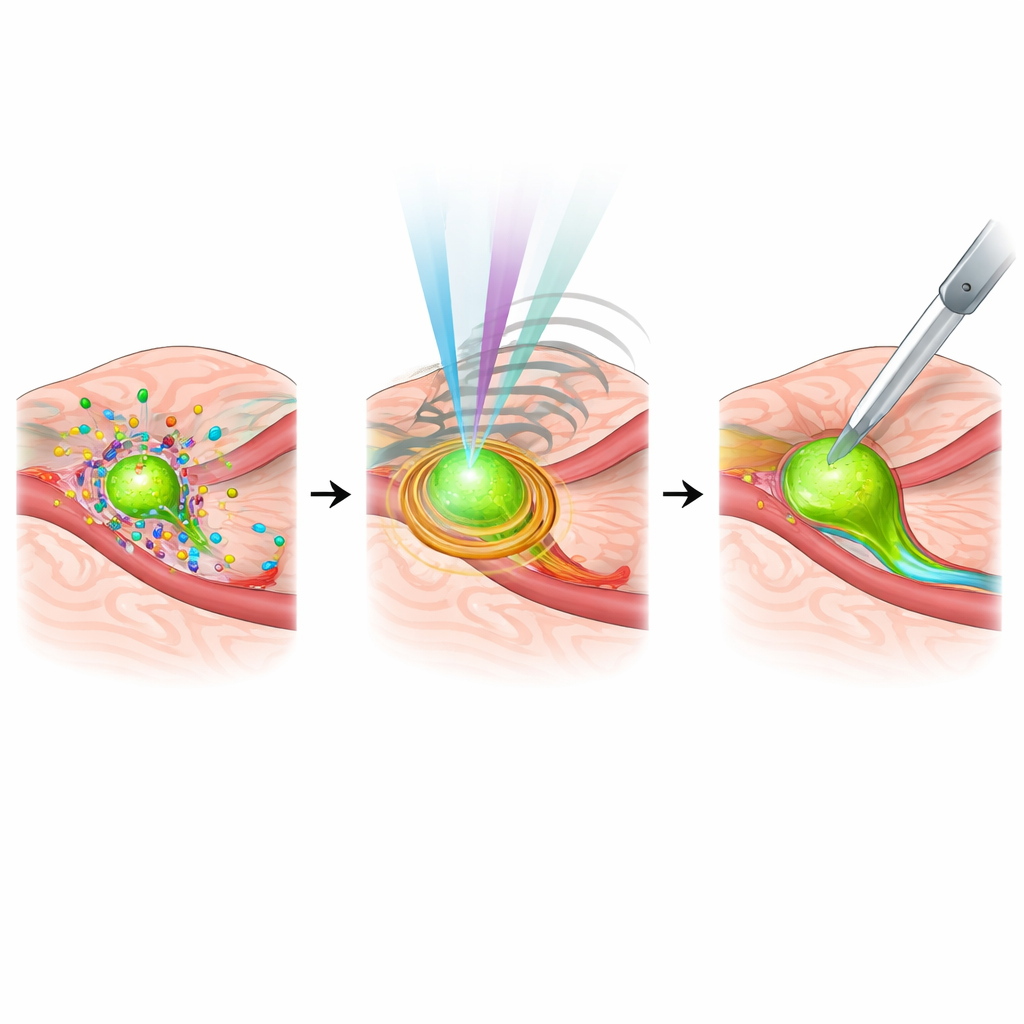
أنظمة أذكى، أهداف مخصصة، والمعوقات المتبقية
ينظر الاستعراض أيضًا قدمًا إلى دور الذكاء الاصطناعي والطب المخصص. تساعد نماذج التعلم الآلي بالفعل في تمييز الأنسجة السرطانية عن الطبيعية في الوقت الحقيقي، والتعرف على الهياكل التشريحية الحرجة، وحتى التنبؤ بانتشار العقد اللمفاوية أثناء جراحة البنكرياس، مما قد يقلل الاعتماد على علم الأمراض السريع. في الوقت نفسه، يُعاد تصميم مجسات التصوير لتتناسب مع البصمات الجزيئية الفريدة لورم كل مريض، رابطًا الصور داخل العملية بالبروفايلات الوراثية والجزيئية. ومع ذلك، تبقى عقبات: العديد من الأنظمة مكلفة ومعقدة وصعبة الدمج في مسارات العمل الروتينية؛ بعضها يتطلب عوامل تباين متخصصة بملفات سلامة تُدار بعناية؛ ومعايير دمج كل هذه البيانات في أنظمة الملاحة لا تزال تتطور.
ماذا يعني هذا للمرضى
بعبارات يسهل فهمها، الخلاصة أن الجراحين يكتسبون شيئًا لم يتح لهم وجوده حقًا من قبل: القدرة على رؤية السرطان الحي بوضوح عالٍ أثناء العمل الجراحي. من خلال إضاءة الأورام، وقراءة كيميائها، ورسم خرائط ثلاثية الأبعاد لها، ودمج أنواع متعددة من الصور — وغالبًا بمساعدة الذكاء الاصطناعي — يمكن لهذه الأدوات أن تساعد في ضمان إزالة مزيد من الورم والحفاظ على مزيد من النسيج السليم. وعلى الرغم من أن التكلفة والتدريب والفجوات التكنولوجية يجب معالجتها قبل أن تتوفر هذه الأنظمة على نطاق واسع، فإن اتجاه التطور واضح. تستعد تقنيات التصوير المتقدمة أثناء العملية لتصبح جزءًا أساسيًا من جراحة السرطان القياسية، مقدِّمة للمرضى عمليات أكثر دقة، ونكسات أقل، وفرصًا أفضل للسيطرة طويلة الأمد.
الاستشهاد: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
الكلمات المفتاحية: التصوير أثناء العملية, الجراحة الموجهة بالتألق, كشف حواف الورم, التصوير المتعدد الوسائط للسرطان, التصوير الضوئي الصوتي