Clear Sky Science · ar
استراتيجية وضع علامة مشعّة بخطوة واحدة لـ PET وSPECT والنظائر العلاجية باستخدام الجسيمات النانوية كمُربِط شامل
لماذا تهم الجسيمات المشعة الصغيرة
تعتمد رعاية السرطان الحديثة بشكل متزايد على رؤية الأورام وعلاجها بأدوية مشعة تظهر في الفحوص وتصيبها أحيانًا من الداخل. ومع ذلك، فإن بناء كل دواء مشع جديد بطيء ويحتاج إلى ضبط دقيق، لأن معظم التصاميم يجب أن تُبنى حسب كل معدن مشع بعينه. تستعرض هذه الدراسة نهجًا مختلفًا: استخدام نوع واحد من الجسيمات النانوية القائمة على الحديد كمِقبس «شامل» يمكنه احتواء نظائر طبية مختلفة للتصوير والعلاج، مما قد يسرّع إنشاء هذه الأدوية وضبطها.
من مفاتيح متعددة إلى قفل واحد
تعتمد الأدوية المشعة الحالية عادةً على مخالب كيميائية تُسمى الشوارد (chelator) تمسك ذرات المعدن وتربطها بالأجسام المضادة أو جزيئات الاستهداف الأخرى. كل معدن مشع يميل إلى الحاجة إلى شوارد خاص وصفة تفاعلية خاصة — مثل الحرارة والحموضة ووقت التفاعل تختلف. لبعض المعادن المهمة طبيًا، خصوصًا تلك المستخدمة في علاجات جسيمات ألفا القوية، لا يوجد شوارد مثالي حتى الآن. يجادل المؤلفون بأن هذا النهج القائم على معدن بمفرده أصبح عنق زجاجة: فعدد النظائر المفيدة يزداد، لكن الكيمياء اللازمة للتعامل معها بأمان لا تلحق بالركب.
الجسيمات النانوية كمِقبس شامل
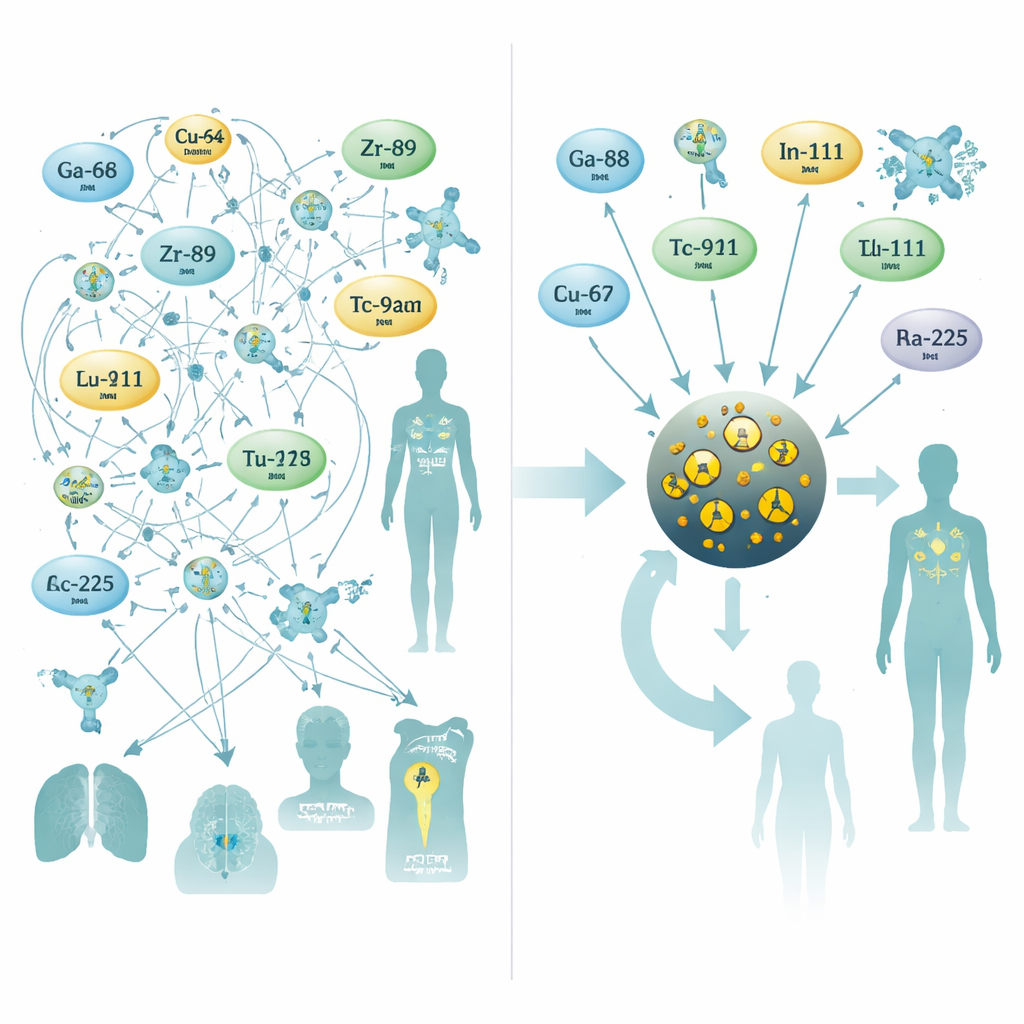
لمعالجة ذلك، لجأ الباحثون إلى جسيمات نانوية صغيرة جدًا من أكسيد الحديد، وهي مادة سبق استكشافها لتباين الرنين المغناطيسي. صمّموا جسيمات ذات نواة من أكسيد الحديد بعرض حوالي ثلاثة نانومترات، مغلفة بطبقة من جزيئات السترات التي تبقيها مستقرة في مجرى الدم. خلال خطوة تخليق بمساعدة الميكروويف استغرقت عشر دقائق فقط، زوّدوا النواة بواحد من عشرة معادن مشعة مختلفة تُستخدم عادةً لتصوير PET أو SPECT أو للعلاج الإشعاعي الداخلي. أنتجت هذه العملية أحادية الإناء جسيمات ذات حجم متناسق مع عوائد عالية، والأهم من ذلك، ثبات ممتاز في مصل الإنسان — حتى مع نظائر علاجية صعبة مثل الراديوم‑223 والأكتينيوم‑225، التي تتسرب نواتج تحللها غالبًا من الشوارد التقليدية.
تصوير الجلطات وأورام المخ
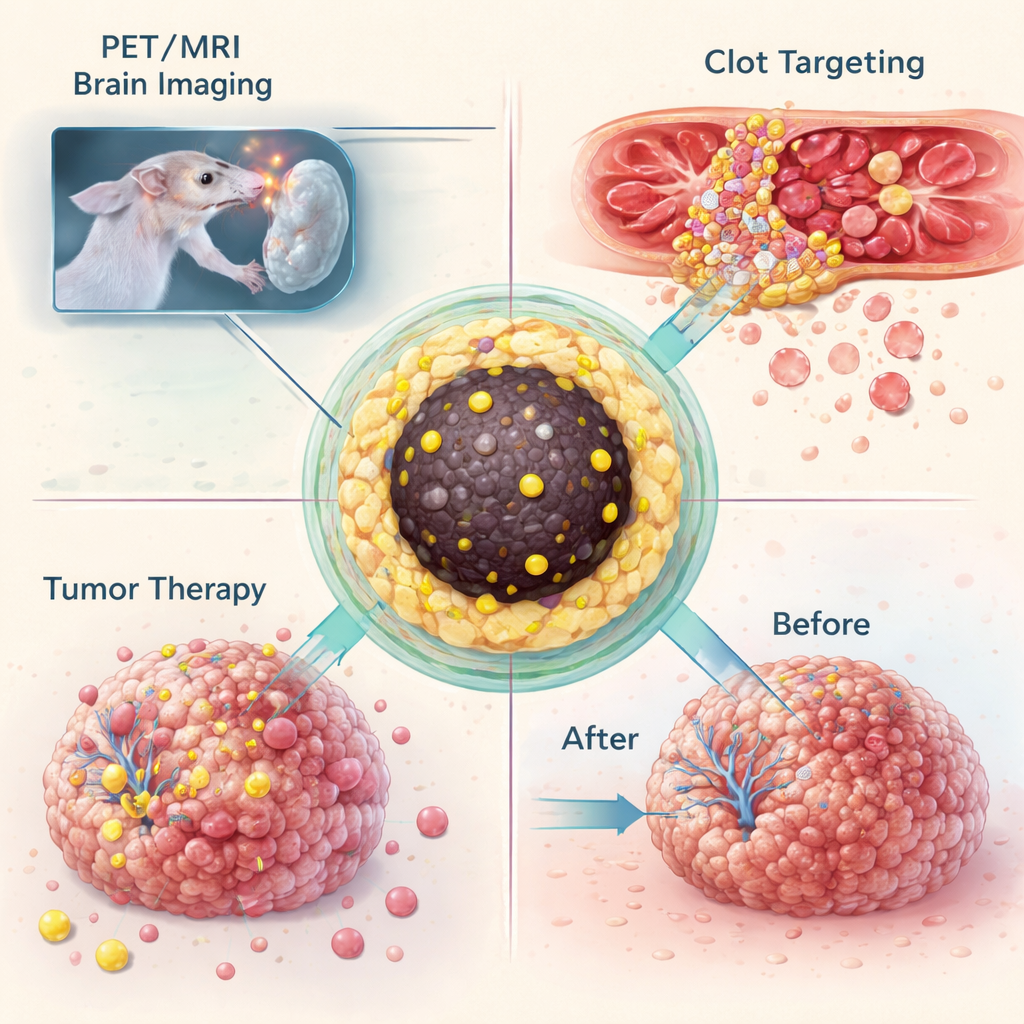
بعد إثبات قدرتهم على احتجاز نظائر مختلفة في نفس تصميم الجسيمات، اختبر الفريق ما تفعله هذه «المتبنيات النانوية» في حيوانات حية. في نموذج فأري للمُتَغِبِّلة، وهي ورم دماغي قاتل، حقنوا جسيمات معنونة بالجاليوم‑68 في مجرى الدم وصوروها باستخدام PET وMRI المدمجين. تراكمت الجسيمات في الأورام الكبيرة بما يكفي لتعطيل الحاجز الدموي الدماغي، مما سمح لنفس التركيب أن يوفر تباينًا واضحًا في MRI وإشارة PET حساسة. في تجربة منفصلة، عدّلوا كيميائيًا الجسيمات لتتمكّن من الارتباط عبر تفاعل «نكسة اختيارية» عالي الاختيار مع جسم مضاد يستهدف الصفائح الدموية النشطة داخل الجلطات. في فئران ذات شريان سِباتي مُصاب، أنتج هذا الاستراتيجية ذات الخطوتين «الاستهداف المسبق» إشارات PET واضحة عند موقع الجلطة، بينما لم تُظهر الحيوانات الضابطة مثل هذه البؤرة.
من التشخيص إلى العلاج وإخراج أكثر أمانًا
استخدموا نفس المنصة أيضًا لتوصيل العلاج. عندما حقنوا جسيمات محمّلة باللوتيشيوم‑177 مباشرة في أورام المتغِبِّلة لدى الفئران، بقيت الجسيمات إلى حد كبير محصورة داخل كتلة الورم لمدة لا تقل عن أسبوعين. خلال ذلك الوقت نما الورم غير المعالج لعدة أضعاف حجمه الأصلي، بينما توقفت الأورام المعالجة عن النمو، مما يشير إلى أن الجرعة الإشعاعية الموضعية كانت كافية لإيقاف التقدم. وباعترافهم بأن العلاجات المتكررة قد تُحمّل الكبد والطحال بالحديد، عدّل الفريق ظروف التخليق لصنع جسيمات أصغر — حوالي أربعة إلى خمسة نانومترات — بحيث تكون صغيرة بما يكفي لترشيحها عبر الكليتين. كانت هذه الجسيمات المُصغرة لا تزال تحافظ على حمولتها المشعة بأمان ولكنها طُرِدَت بسرعة إلى المثانة، مما يقلل التراكم طويل الأمد في الأعضاء الرئيسية.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
لغير المتخصصين، الرسالة الأساسية أن الباحثين بنوا منصة جسيمات نانوية واحدة ومرنة يمكن إقرانها بالعديد من المعادن المشعة المختلفة دون الحاجة لإعادة اختراع الكيمياء في كل مرة. في نماذج حيوانية، يمكن أن يساعد نفس الجسيم الأساسي على اكتشاف أورام المخ، إبراز الجلطات الدموية، توصيل الإشعاع مباشرة إلى الأورام، وحتى تعديل سلوكه لخروج الجسم عبر الكليتين. بينما هناك حاجة إلى مزيد من العمل قبل أن يصل هذا النهج إلى المرضى، فإنه يقدم مسارًا واعدًا لتصميم عائلات من العوامل التشخيصية والعلاجية التي تشترك في نفس السلوك الحيوي، وتختلف فقط بنوع الإشعاع الذي تحمله. قد تُبسّط هذه الثباتية التطوير، تحسن اختبارات السلامة، وتجعل أدوات الطب النووي المتقدمة أكثر توفّرًا على نطاق أوسع.
الاستشهاد: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
الكلمات المفتاحية: العلاج التشخيصي الإشعاعي, الجسيمات النانوية, تصوير PET, المُتَغِبِّلة, الإشعاع المستهدف للعلاج