Clear Sky Science · ar
تسارع وتوطن اعتلال السِنيوكلين في نموذج فأري هجين: دلالات لدراسات التصوير المقطعي بالإصدار البوزيتروني
لماذا يهم هذا البحث
يشتهر مرض باركنسون بالرعشات ومشاكل الحركة، لكن بدايته في أعمق مناطق الدماغ تتمثل في تغيرات دقيقة يصعب رؤيتها. يحتاج الأطباء بشكل عاجل إلى طرق لرصد هذه التغيرات مبكراً ولاختبار أدوية جديدة بسرعة. تصف هذه الدراسة نموذج فأري مُحسّن يعيد إنتاج سمات رئيسية من تلف الدماغ الشبيه بمرض باركنسون في غضون أسابيع قليلة وفي منطقة دماغية محددة للغاية، ومصمم خصيصاً للاستخدام مع تقنيات المسح المتقدمة المعروفة بتصوير PET. 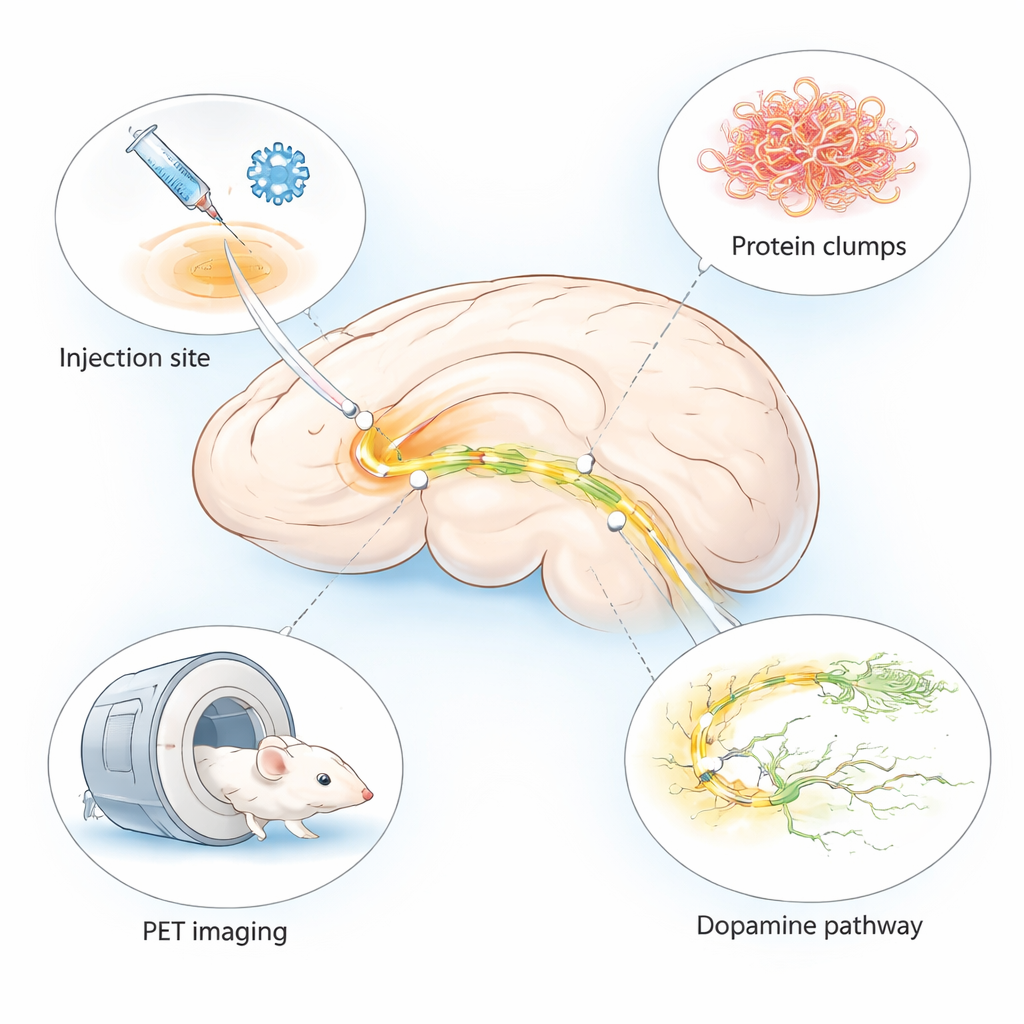
بناء نموذج مرضي أسرع وأكثر تركيزاً
تستغرق العديد من نماذج الحيوانات الحالية لمرض باركنسون شهوراً لتظهر الأعراض أو تفشل في إظهار نطاق التغيرات الدماغية الكامل كما في المرضى. جمع المؤلفون بين نهجين راسخين في نموذج "هجيني" واحد. حقنوا فيروساً آمناً يجعل خلايا الدماغ تنتج ألفا‑سينوكلين البشري — وهو بروتين يتكتل في باركنسون — مع خيوط متشكلة مسبقاً تعمل كبذور تحفز المزيد من التكتل. تم توصيل كلا المادتين إلى منطقة صغيرة مرتبطة بالحركة تسمى المادة السوداء على جانب واحد من دماغ الفأر. ينتج عن هذا التصميم تغيرات موضعية لكنها مكثفة شبيهة بالمرض على الجانب المحقون، بينما يبقى الجانب الآخر نسبياً سليماً للمقارنة.
تتبع تكتلات البروتين وخلايا الأعصاب الميتة
خلال أسبوعين فقط من الحقن، أظهرت الفئران مستويات عالية من ألفا‑سينوكلين البشري وصيغته الشاذة الفسفورية في المنطقة الدماغية المستهدفة. تحت المجهر، رأى الباحثون هياكل تشبه أجسام ليوي والمحاور الليفية ليوي التي تُعد من العلامات المميزة لمرض باركنسون. خلال الأسابيع التالية، ازدادت هذه الترسبات الشاذة. وفي الوقت نفسه، بدأت الخلايا العصبية المنتجة للدوبامين — الناقل الكيميائي الحاسم للحركة السلسة — في الاختفاء. انخفضت مؤشرات هذه الخلايا إلى نحو 60 بالمئة من المستوى المرصود على الجانب غير المعالج بحلول الأسبوع الخامس، مما يؤكد فقداناً واضحاً وتقدّمياً في نظام الدوبامين.
الالتهاب وتلاشي المشابك ومصانع الطاقة المتعبة
دخلت خلايا الجهاز المناعي في الدماغ، المسماة بالميكروجليا، أيضاً في حالة نشاط التهابية شديدة حول المنطقة المتضررة. كانت صبغات عدة بروتينات مرتبطة بالالتهاب أقوى بكثير بالقرب من ترسبات ألفا‑سينوكلين مقارنة بالجانب المقابل من الدماغ. وفي مراحل لاحقة، اكتشف الفريق فقداناً في المشابك — نقاط الاتصال الدقيقة التي تتواصل من خلالها الخلايا العصبية — وعلامات على أن الميتوكوندريا، مصانع طاقة الخلايا، لا تعمل بشكل سليم. تُظهر هذه النتائج معاً أن النموذج لا يخلق مجرد تكتلات بروتينية؛ بل يلتقط أيضاً سلسلة التفاعلات من الالتهاب وفشل الاتصالات ومشكلات الطاقة التي تسهم في موت الخلايا العصبية في مرض باركنسون. 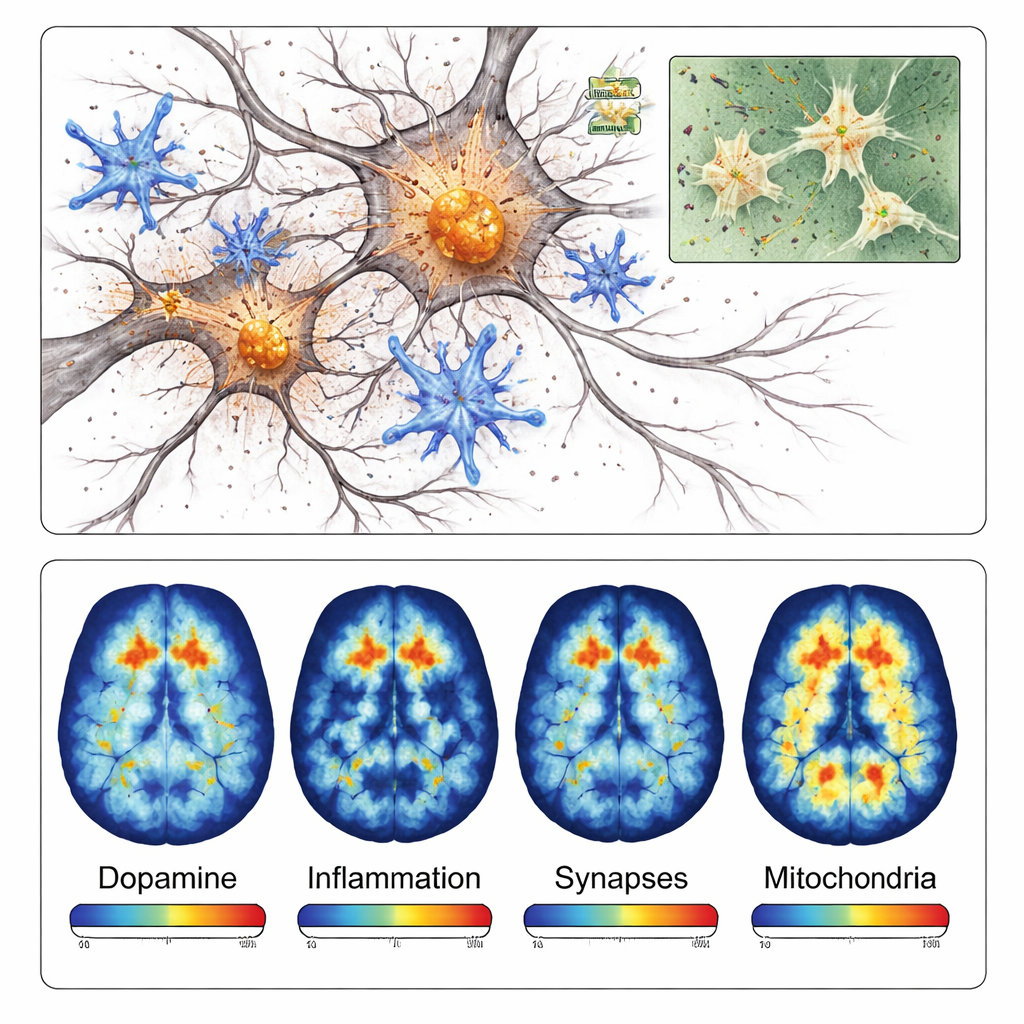
استخدام أجهزة PET
بما أن هذا النموذج موضعي ويتطور بسرعة، فهو مناسب بشكل خاص للتصوير المقطعي بالإصدار البوزيتروني (PET)، تقنية مسح يمكنها قياس جزيئات محددة في أدمغة حية. اختبر الباحثون أربعة متتبِعات PET مختلفة ترتبط بنهايات الأعصاب الدوبامينية والميكروجليا الالتهابية وبروتينات المشبك وإنزيمات الميتوكوندريا. في كل حالة، أظهرت مسوحات PET إشارات أقل أو أعلى على الجانب المحقون بطرق تتوافق مع نتائج المجهر. على سبيل المثال، أظهر المتتبع المستهدف لمسارات الدوبامين إشارة أقل بحوالي 40 بالمئة على الجانب المتضرر، بينما أظهر متتبع الالتهاب زيادة في الإشارة بأكثر من 40 بالمئة في المنطقة المتأثرة.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
يجمع نموذج الفأر الجديد، في إطار زمني قصير، العديد من التغيرات الرئيسية التي تحدث على مدى سنوات في أدمغة الأشخاص المصابين بمرض باركنسون. وبما أن الضرر مقصور على منطقة صغيرة ومحددة ويمكن متابعته بواسطة مسوحات PET، يمكن للباحثين اختبار متتبِعات تصويرية وعلاجات محتملة بكفاءة أكبر. وبينما لا يمكن لأي فأر أن يعيد إنتاج الحالة البشرية بالكامل، يوفر هذا النهج أداة قوية وعملية لردم الفجوة بين العمل المختبري الأساسي والدراسات البشرية، مما يساعد في النهاية على تحسين التشخيص وتسريع البحث عن علاجات أفضل.
الاستشهاد: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
الكلمات المفتاحية: مرض باركنسون, ألفا-سينوكلين, اعتلال السينوكلين, تصوير PET, نموذج فأري