Clear Sky Science · ar
البروتين G القابل للذوبان لفيروس المتلازمة التنفسية المخللية يعزز انتشار الفيروس عبر تمهيد NLRP3 المتوسط بواسطة TLR2 والموت الخلوي النَّاروِي (بايروبتوز)
لماذا يهم هذا الفيروس الرئوي الجميع
فيروس المتلازمة التنفسية المخللية (RSV) معروف بصورة أساسية كمصدر للمرض في الشتاء بين الرضع، لكنه يسبب أيضًا دخول المستشفيات لدى العديد من كبار السن والأشخاص ذوي المناعة الضعيفة. وحتى مع وجود لقاحات وأجسام مضادة واقية حديثة، يعيد RSV إصابة الناس مرارًا ويمكن أن يسبب ضررًا رئويًا شديدًا. تفحص هذه الدراسة بروتينًا فيروسيًا غير معروف كثيرًا، وهو شكل قابل للذوبان من بروتين G الخاص بـ RSV، وتكشف كيف قد يهيئ خلايا الرئة بهدوء لالتهاب انفجاري ويساعد الفيروس على الانتشار بكفاءة أكبر عبر الممرات الهوائية.
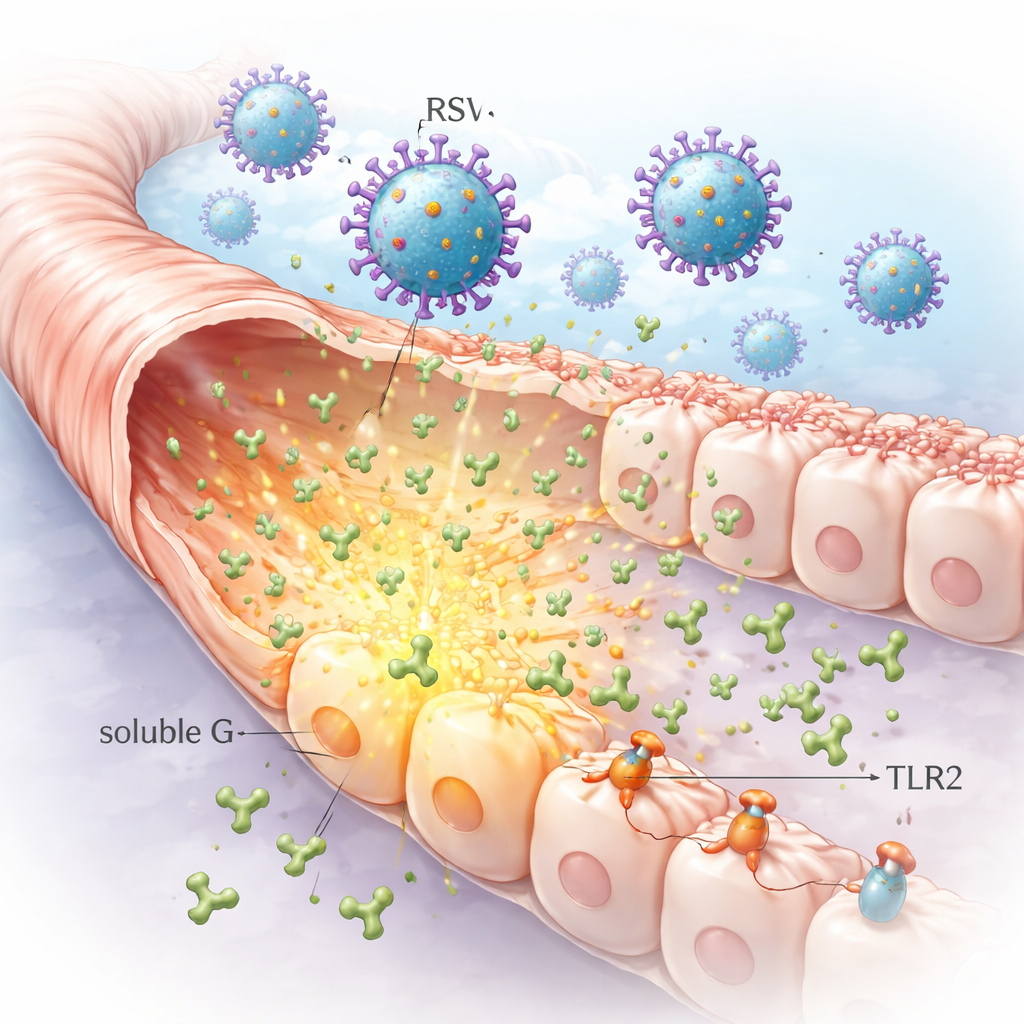
بروتين فيروسي مُفرَز يتقدم الإصابة
يحمل RSV بروتينًا للتعلق يُدعى G على سطحه يساعده على الالتصاق بخلايا الممرات الهوائية. وبشكل غير معتاد، تُفرز الخلايا المصابة أيضًا كميات كبيرة من شكل حر من هذا البروتين، المعروف باسم G القابل للذوبان. أظهر الباحثون أن خلايا الرئة المصابة في المختبر يمكن أن تطرح مستويات عالية جدًا من G القابل للذوبان إلى محيطها. وبما أن هذا الشكل يمكن أن ينتشر بعيدًا عن موقع العدوى الأصلي، فإنه قد يصل إلى خلايا مجاورة لم تُصب بعد، ممهِّدًا الطريق لتغييرات أوسع في بطانة الرئة أكثر مما قد يسببه الفيروس وحده.
G القابل للذوبان كمفتاح مزدوج السِّمَتَيْن لأسطح الخلايا
بدمج المجهر، واختبارات السحب البيوكيميائية، ومعالجات بالإنزيمات، رسم الفريق خريطة كيفية التصاق G القابل للذوبان بالخلايا. وجدوا أنه يمكن أن يرتبط بسلاسل سكرية تُسمى الغليكوزأمينوجليكانات، وكذلك بمستقبل معروف لـ RSV يُدعى CX3CR1. وبشكل حاسم، يرتبط G القابل للذوبان أيضًا بجزيء مستشعر الأنماط على الخلايا المناعية وخلايا الممرات الهوائية يُدعى TLR2. أدى نقش صغير في بروتين G، معروف باسم CX3C، دورًا مهمًا في الارتباط القوي بـ CX3CR1 وفي تجنيد قوي لـ TLR2. وهذا يعني أن G القابل للذوبان يمكن أن يُؤسر أولًا بشكل ضعيف على سطح الخلية ثم يتفاعل مع مستقبلات أكثر تحديدًا تتحكم بكيفية استجابة الخلايا للتهديدات.
تمهيد خلايا الرئة لنوع التَّلف الخِلوي الالتهابي
اتضح أن تفاعل TLR2 مع G القابل للذوبان بعيد عن أن يكون حميدًا. في خلايا مناعية حاملة لمؤشرات وخطوط خلايا رئة بشرية، فعَّل G القابل للذوبان مسار الإشارة MyD88–NF-κB الناتج عن TLR2، مما أدى إلى إفراز رسائل التهابية مثل IL-6 وIL-8. وفي الوقت نفسه عزز إنتاج مكونات “نظام الإنذار” الجزيئي المعروف بالإنفلامازوم NLRP3 وإنزيمات تولد جزيئات تفاعلية مثل أكسيد النيتريك وجذور الأكسجين. بمفردها سببت هذه التغيرات ضررًا طفيفًا فقط. لكن عندما أُصيبت الخلايا الممهَّدة لاحقًا بـ RSV، أدى الضربة الثانية إلى تجميع كامل للإنفلامازوم، وتفعيل إنزيم الكاسبيز‑1، وتشكيل مسام في غشاء الخلية، وشكل اشتعالي من الموت الخلوي يُعرف بالبايروبتوز. أنتج هذا العملية ثقوبًا في الخلايا، وانسكاب محتوياتها الالتهابية، وتزامن مع كميات أعلى من الفيروس المعدٍ التي أُفرِج عنها في سائل الزرع.
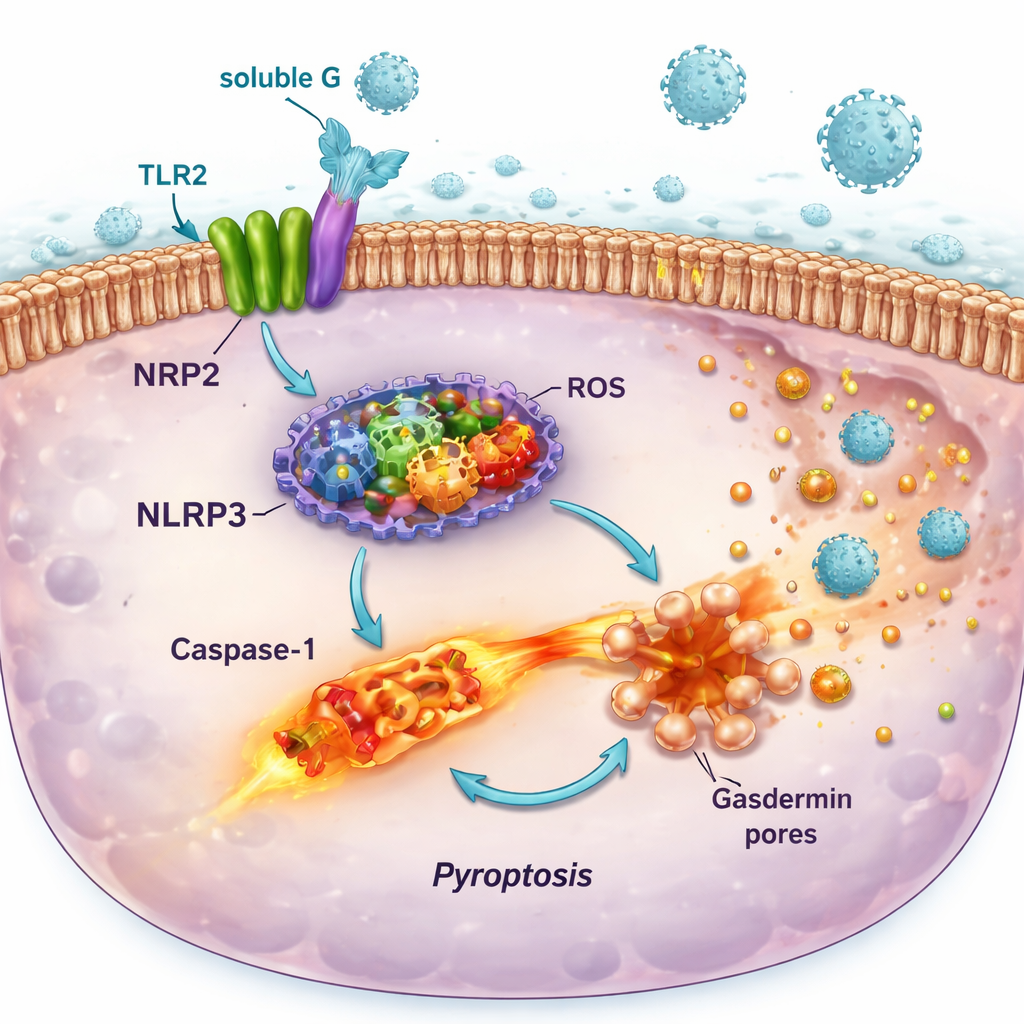
كيف قد تفاقم هذه السلسلة التفاعلية مرض الرئة
كان التأثير المسبب للموت بواسطة G القابل للذوبان أقوى في خلايا الظهارة الهوائية—الخلايا التي يفضّل RSV إصابتها—واعتمد على إنفلامازوم NLRP3، لأن مثبطًا محددًا لـ NLRP3 أعاد حيوية الخلايا إلى حد كبير. بالمقابل، لم تخضع بعض الخلايا المناعية الغنية بـ TLR2 لكن الفقيرة في مستقبل CX3CR1 لموت تحللي قوي تحت الشروط نفسها. يشير هذا النمط إلى أن RSV يستخدم G القابل للذوبان لاختيار إضعاف وتدمير الطِّبقة الواقية للممرات الهوائية مع الحفاظ على بعض الخلايا المناعية التي يمكنها الاستمرار في إنتاج الإشارات. النتيجة بيئة رئوية أكثر التهابًا، ومزيدًا من حطام الخلايا، ومزيدًا من الفرص لجسيمات فيروسية جديدة للهروب وإصابة الخلايا المجاورة.
ماذا يعني هذا للعلاجات المستقبلية
للغير متخصصين، الرسالة الرئيسية أن RSV لا يعتمد فقط على الضرر المباشر الناجم عن غزو الفيروس. عبر إفراز كميات كبيرة من بروتين G القابل للذوبان، يمكنه "تليين" الخلايا المجاورة عبر TLR2، مما يجعلها أكثر عرضة للموت بطريقة التهابية ولانسكاب الفيروس. تحدد هذه الدراسة عدة خطوات في تلك السلسلة—G القابل للذوبان نفسه، ونقشه CX3C، وTLR2، وإنفلامازوم NLRP3—كأهداف دوائية محتملة. من حيث المبدأ، قد تقلل العلاجات التي تمنع التفاعل بين G القابل للذوبان وTLR2 أو التي تخفف نشاط NLRP3 كلاً من إصابة الرئة وانتشار الفيروس. قد تكمل مثل هذه الاستراتيجيات يومًا ما اللقاحات والأجسام المضادة القائمة، لتوفر حماية أفضل للأصغر سنًا والأكثر عرضة للخطر من المرضى.
الاستشهاد: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
الكلمات المفتاحية: فيروس المتلازمة التنفسية المخللية, البروتين G القابل للذوبان, الإنفلامازوم TLR2, البايروبتوز, التهاب الرئة