Clear Sky Science · ar
الاستجابة العالمية للتعرُّض للمضادات الحيوية تكشف دورًا حاسمًا لاستقلاب النيوكليوتيدات في التحمل العالي لمضادات بيتا-لاكتام
لماذا تتجاهل بعض البكتيريا أقوى مضاداتنا الحيوية
من المفترض أن تقضي المضادات الحيوية على البكتيريا الضارة، ومع ذلك تستمر العديد من العدوى بعناد أو تعود بعد العلاج. يستكشف هذا البحث سببًا قليل التقدير: بعض البكتيريا قادرة على التماسك والبقاء مؤقتًا حتى عند تعرضها لكميات عالية جدًا من أدوية قوية مثل البنسلين. من خلال كشف كيفية إعادة هذه الميكروبات تهيئة كيميائها الداخلية لتحمُّل الهجوم، يشير الباحثون إلى طرق جديدة قد نستعيد بها فعالية المضادات الحيوية الحالية.
حيلة بقاء خفية داخل العدوى
عند التعرض لمضادات بيتا-لاكتام مثل البنسلين، لا تموت العديد من بكتيريا غرام-سلبية الخطرة ببساطة. بدلًا من ذلك، يمكنها أن تتخلص من جدارها الخلوي الصلب وتتحول إلى أجسام هشة مستديرة تُسمى سبيروبلاستات (spheroplasts). في هذه الحالة، تتوقف عن التكاثر لكنها تظل حية ونشطة أيضيًا. بمجرد زوال الدواء، تعيد بناء جدارها، وتستعيد شكلها العصوي الطبيعي، وقد تعيد إشعال العدوى. ونظرًا لأن هذا «التحمل» يشكل خطوة نحو مقاومة المضادات الحيوية الكاملة وفشل العلاج، فإن فهم كيفية بقاء السبيروبلاستات أمر بالغ الأهمية للطب المستقبلي.
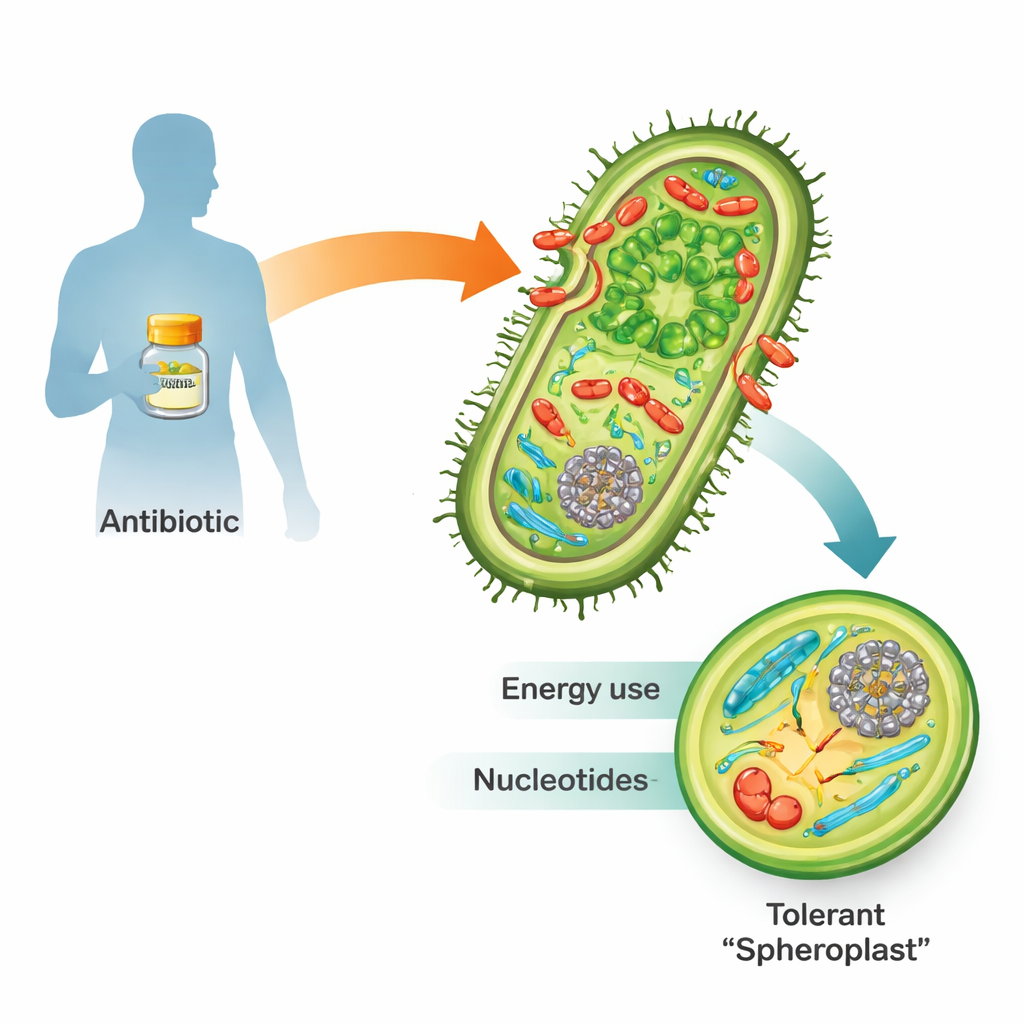
الاستماع إلى بث الطوارئ داخل الخلية
استخدم الفريق بكتيريا Vibrio cholerae، المسببة للكوليرا، كنموذج لأنها متسامحة بشكل استثنائي مع بيتا-لاكتامات وسهلة التلاعب جينيًا. غمروا البكتيريا بعشرة أضعاف الجرعة القاتلة الدنيا من البنسلين وتتبعوا الاستجابة بمرور الوقت باستخدام أداتين قويتين. سجلت الترانسكريبتوميكس أي الجينات التي فُعِّلت أو أُطفئت، بينما قاست الميتابولوميكيات مئات الجزيئات الصغيرة التي تغذي وتبني الخلية. معًا، خلقت تقنيات «متعددة الأومكس» هذه خريطة زمنية لكيفية إعادة الخلية المتحملة تشكيل آلياتها الداخلية أثناء الهجوم الدوائي.
إعادة توجيه استقلابي ونقطة ضعف خفية
كشفت البيانات عن تغييرات واسعة في المسارات الأساسية. تم تنشيط جينات بناء الجدار الخلوي بشدة، بما يتوافق مع محاولة الخلية إصلاح الضرر والاستعداد للتعافي. كما تفعلَّلت نظم الاستجابة للحرارة والضغط، على الأرجح للتعامل مع البروتينات المطوية بشكل خاطئ أو المؤكسدة الناتجة عن الإجهاد الناجم عن المضاد الحيوي. وفي الوقت نفسه، تغيّر أيض الكربون المركزي: زُوِّدَت بعض خطوات دورة حمض الستريك (دورة الـTCA) — مولد الطاقة الرئيسي للخلية — بينما استُنفِدت بشكل كبير وسطاء رئيسية في التحلل السكري مثل غلوكوز-6-فوسفات وفركتوز-6-فوسفات. هذه الوسائط عادةً ما تغذي كلًا من إنتاج الطاقة وبناء الجدار الخلوي، مما يشير إلى أن «دورات عبثية» مستمرة ومهدِرة لمواد الجدار تستنزف الموارد.
الضغط على النيوكليوتيدات
أبرز تغيير شمل النيوكليوتيدات، وحدات البناء للحمض النووي والحمض النووي الريبي والعديد من جزيئات نقل الطاقة. هبطت مستويات العديد من النيوكليوتيدات ومقدماتها بشكل حاد في الخلايا المعالجة بالبنسلين، على الرغم من أن الجينات المسؤولة عن تصنيعها من الصفر كانت مفعلة بشدة. وفي الوقت نفسه، خُنِّدِت الجينات المشاركة في «إعادة تدوير» النيوكليوتيدات، كما لو أن الخلية تحاول الحفاظ على ما تبقّى منها. ترجح هذه الأنماط أن السبيروبلاستات تحت ضغط شديد على مستوى النيوكليوتيدات. عندما تدخل الباحثون عمدًا في المسارات التي تزود مقدّمات النيوكليوتيدات — مثل مسار فسفات البنتوز (pentose phosphate pathway) — أو حظروا إنتاج النيوكليوتيدات بدواء آخر، التريميثوبريم، فإن الجمع مع بيتا-لاكتامات قضى على عدد أكبر بكثير من البكتيريا مقارنة بكل دواء على حدة. لوحظ هذا التآزر القوي ليس فقط في Vibrio cholerae بل أيضًا في سلالات سريرية شديدة التحمل من Klebsiella pneumoniae وEscherichia coli.
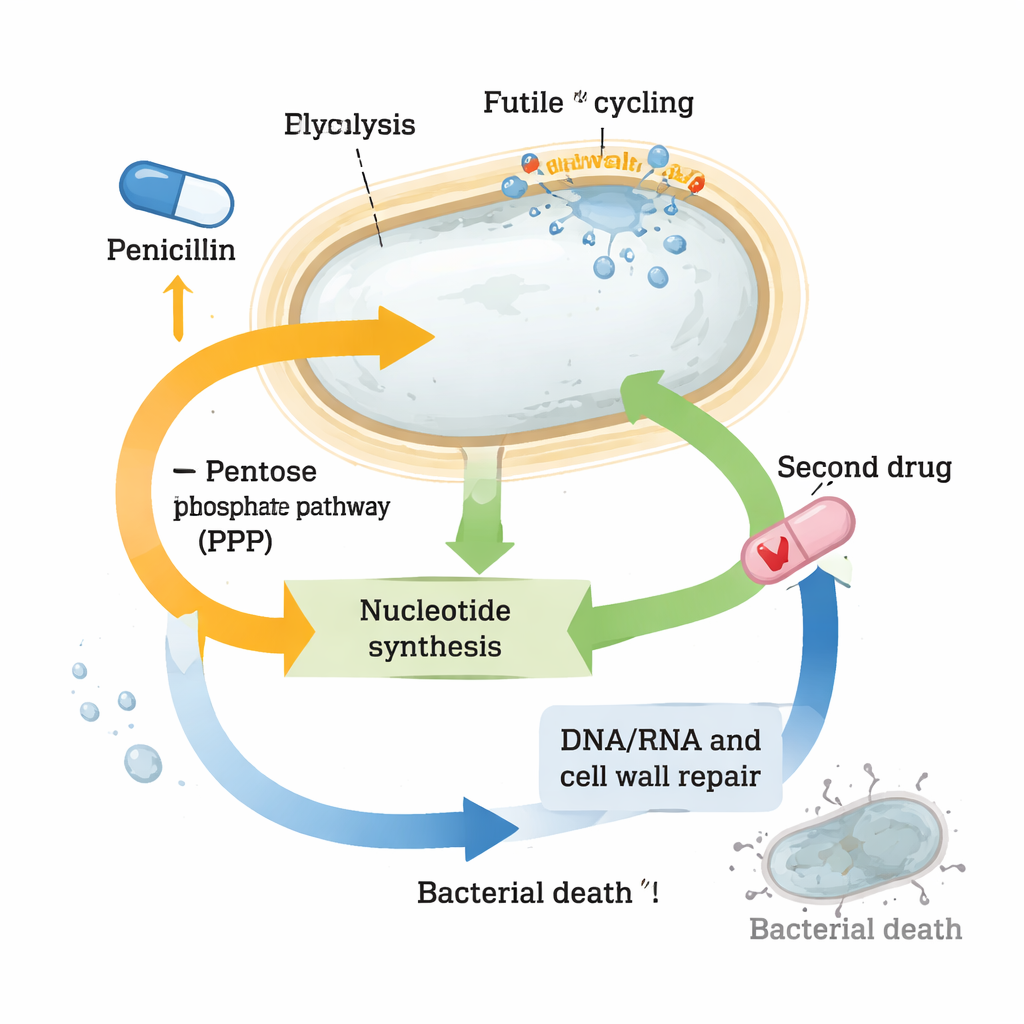
تحويل كيمياء البقاء إلى ميزة علاجية
على الرغم من إعادة تشكيل استقلابها إلى حد كبير، تضمن السبيروبلاستات المتحملة الحفاظ على عملتها الطاقية، ATP، بشكل نسبي وتتفادى الضرر الكارثي، مما يساعدها على الصمود أمام تعرضات طويلة للمضاد الحيوي. لكن العمل يوضح أنه في سبيل ذلك تدفع بمخزون النيوكليوتيدات إلى حافة الانهيار. هذا التوازن الهش يخلق نقطة ضعف: دفع استقلاب النيوكليوتيدات قليلاً أكثر بدواء ثانٍ ينهار دفاعها ويستعيد القتل الفعال. للقراء العامين، الخلاصة أن بعض البكتيريا تبقى على قيد الحياة أمام المضادات الحيوية ليس لأن الأدوية تفشل في استهدافها، بل لأن الخلايا تعيد بسرعة توصيل كيميائها لتحمُّل الضربة. من خلال إيجاد واستغلال الروابط الضعيفة في هذه شبكة البقاء — هنا، استقلاب النيوكليوتيدات — قد يتمكن الباحثون من تحويل المضادات الحيوية القديمة إلى علاجات تركيبية قوية تُغلب حتى العوامل الممرضة شديدة التحمل.
الاستشهاد: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
الكلمات المفتاحية: تحمل المضادات الحيوية, مضادات بيتا-لاكتام, استقلاب النيوكليوتيدات, استمرار البكتيريا, تركيبات دوائية