Clear Sky Science · ar
تخفيف تنشيط التأم فوق القلب وكثرة الخلايا الليفية العضلية عبر محور Fbln2–Nupr1b يحفّز تجدد القلب في سمك الزرد
لماذا بعض القلوب قادرة على الشفاء ذاتياً
عند تعرض شخص لنوبة قلبية، يُغطي النسيج العضلي المتضرر عادةً بِندبة صلبة لا تلتئم تمامًا. يقوم سمك الزرد، وهو سمك صغير مخطط يستخدم في الأحواض، بشيء استثنائي: يعيد نمو نسيج قلبه وفي النهاية يزيل معظم الندبة. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذا تبعات طبية كبيرة: كيف يعرف القلب الشافي متى يبني نسيج ندبي ومتى يزيله لتسمح العضلة الجديدة بالنمو؟ عبر فك توازن هذه العملية في سمك الزرد، تشير الدراسة إلى استراتيجيات قد تساعد يوماً ما القلوب البشرية المصابة على الإصلاح بدلاً من الفشل.
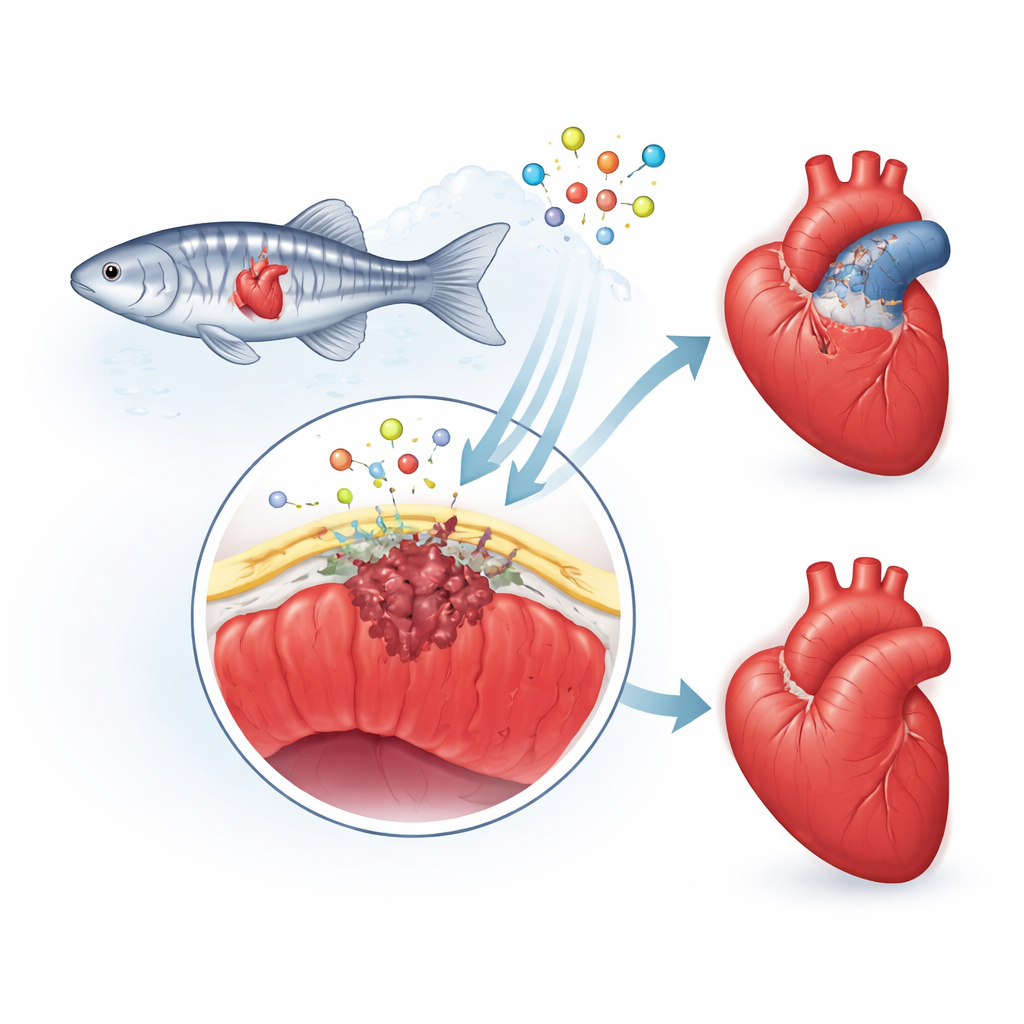
الطبقة الواقية الخارجية للقلب
تركز الباحثون على التأم فوق القلب، طبقة رقيقة «كجلد» تغطي القلب. بعد الإصابة، تستيقظ هذه الطبقة، وتتغير هوية خلاياها، وبعضها يغوص إلى المنطقة المتضررة. هناك تتحوّل إلى خلايا داعمة وخلايا مكوِّنة للندوب، وتفرز إشارات كيميائية توجه نمو الأوعية الدموية وعضلة القلب الجديدة. لدى البشر، تميل استجابة الإصلاح هذه إلى الإفراط، مما يترك ندبة سميكة ودائمة. بينما في سمك الزرد تكون الندبة مؤقتة وتتفكك تدريجياً مع عودة العضلة السليمة. شكّ الفريق في أن بروتيناً يسمى فيبولين-2 (Fbln2)، الموجود في السقالة المحيطة بالقلب، يساعد على ضبط سرعة وشدة استجابة التأم فوق القلب.
مفتاح خافت جزيئي للتندب
باستخدام تحرير الجينات في سمك الزرد، أنشأ العلماء نوعين من الحيوانات بمستويات مختلفة من Fbln2: سلالة بمستوى منخفض من Fbln2 وأخرى خُلت تماماً من البروتين. أصابوا قلوب السمك بمسبار تجميد، مُحاكيًا للنوبة القلبية، وتابعوا الشفاء على مدى أسابيع إلى أشهر. عندما انخفضت مستويات Fbln2، تقلّص الانقسام الخلوي المبكر في عضلة القلب وبطانة الأوعية، لكن النسيج الليفي الناتج كان أصغر وأسهل إعادة تشكيل. بعد ثلاثة أشهر، كانت هذه القلوب قد تجددت جيداً وبقيت القليل من الكولاجين، المكوّن الرئيسي للندبة. في المقابل، أظهر السمك الذي يفتقد Fbln2 تماماً إيقافاً أقوى لمسار رئيسي للتحوّل والنمو، يشمل عائلة إشارات معروفة باسم TGFβ، وكان هناك عدد أقل بكثير من الخلايا المكوِّنة للندوب أسفل التأم فوق القلب. كانت ندوبهم المبكرة أصغر أيضاً — ومع ذلك بعد ذلك فشلت هذه القلوب في إزالة الكولاجين وانتهى بها المطاف بندوب كبيرة ودائمة وتجدد ضعيف.
التدقيق في تغيرات حالة التأم فوق القلب
لمعرفة كيفية تصرف خلايا التأم فوق القلب على مستوى الخلية الواحدة، استخدم الفريق تسلسل RNA الخلوي المفرد بعد وقت قصير من الإصابة. حدّدوا عدة «حالات» لخلايا التأم فوق القلب، بما في ذلك خلايا هادئة، وخلايا فُعّلت حديثاً، وخلايا متوترة تتأقلم مع نقص الأكسجين، وخلايا في طور الانقسام النشط. في الأسماك ذات Fbln2 الطبيعي، تقدّمت خلايا التأم فوق القلب بسلاسة من حالة الهدوء إلى التفعيل ثم النضج. في الأسماك ذات Fbln2 المنخفض أو المفقود، توقفت هذه المرحلة: بقيت الخلايا في المراحل المبكرة وكانت المجموعات الناضجة النشطة ناقصة، لا سيما في حيوانات الفقد التام. نُكست عدة جينات تُشغَّل عادة أثناء تفعيل التأم فوق القلب واستجابة لإشارة TGFβ، مما يشير إلى أن Fbln2 يعمل كضابط لهذا المسار الذي يحدد مدى التزام التأم بتكوين وإعادة تشكيل النسيج الندبي.
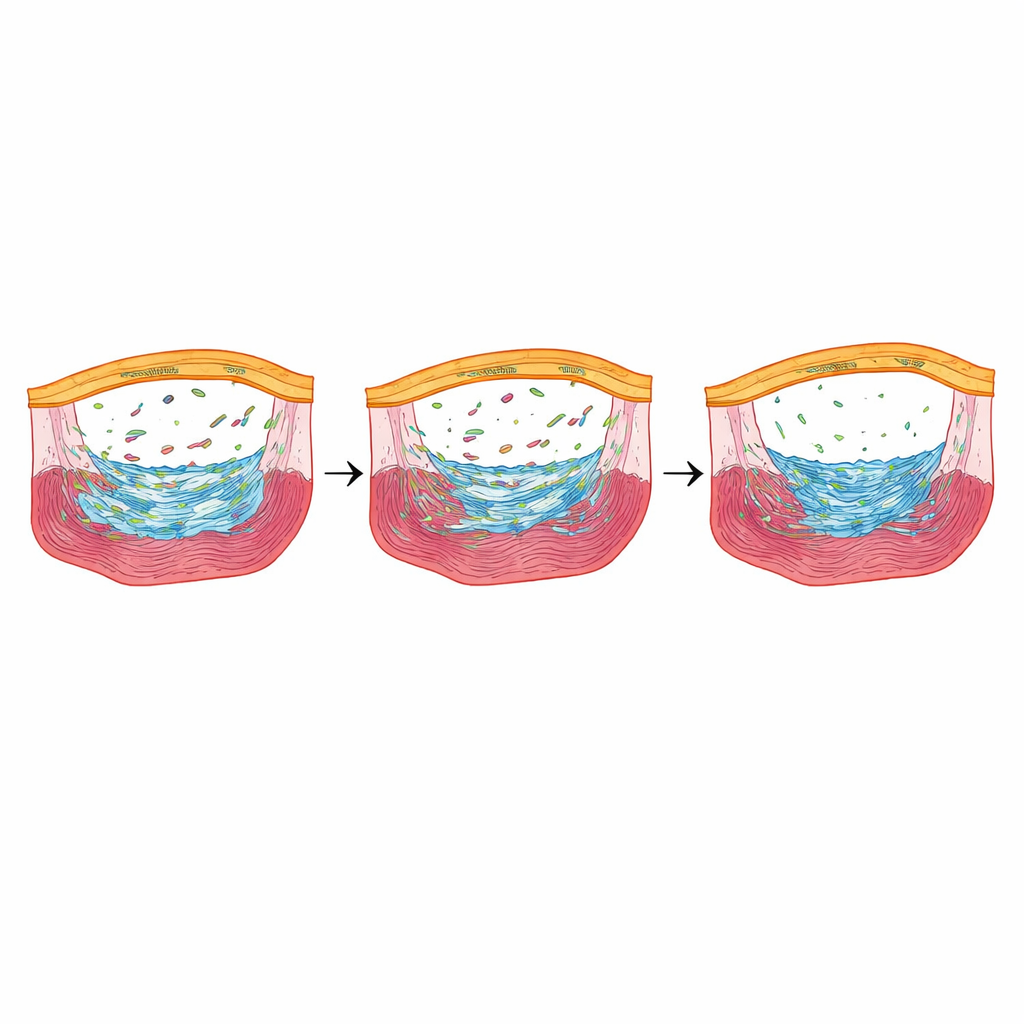
مستجيب للضغط ينقح عملية الإصلاح
من بين الجينات التي انخفضت بشدة عندما نُقص Fbln2، برز واحد: nupr1b، منظم مستجيب للإجهاد ينشط في خلايا التأم فوق القلب خلال المراحل المبكرة من الشفاء. عند حذف nupr1b، أظهر سمك الزرد عددًا أقل من خلايا التأم المكوِّنة للندوب وانخفض انقسام خلايا عضلة القلب، وبقوا بترسبات كولاجين كبيرة بعد أشهر من الإصابة — شبيهاً بالأسماك التي تفتقد Fbln2 تماماً. ولافت أن إعادة تشغيل nupr1b لفترة وجيزة فقط في خلايا التأم فوق القلب في الأسماك ذات Fbln2 المنخفض أعادت عدد الخلايا المكوِّنة للندوب وانقسام خلايا عضلة القلب إلى سابق عهدها، وزادت الندب المتأخرة. كبت مستقبلات TGFβ كيميائياً خفّض مستويات nupr1b، مما يضع nupr1b أسفل محور إشارة Fbln2–TGFβ.
ماذا يعني هذا لشفاء القلب البشري
تُظهر هذه النتائج معاً «محور Fbln2–Nupr1b في التأم فوق القلب» الذي يساعد قلوب سمك الزرد على السير في توازن دقيق بين قلة وكثرة التليف. خفض هذا المحور قليلاً يروّض الطفرة الأولية للندب ويشجّع الإزالة الفعّالة له، بينما إيقافه تماماً يعيق التجدد ويترك ندبة جامدة. بالنسبة للطب البشري، الدرس هو أن الهدف ليس منع التندب تماماً، بل ضبطه — الحفاظ على بنية كافية لمنع التمزق مع ضمان أن النسيج الندبي مؤقت ويمكن استبداله بعضلة سليمة. فهم هذا النظام الضابط في سمك الزرد واستغلاله قد يوجّه علاجات مستقبلية تدفع القلب البشري المصاب نحو تجدد حقيقي بدلاً من التندب المزمن.
الاستشهاد: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
الكلمات المفتاحية: تجدد القلب, التليف, سمك الزرد, التأم فوق القلب, إشارة TGF-beta