Clear Sky Science · ar
تقييم تكاملي للجينوم والأدبيات لاعتلال عضلة القلب الإيقاعي المرتبط بالـ desmoglein 2 مع تحقق من مجموعة إيطالية
لماذا يهم هذا الجين القلبي للعائلات
العديد من المشاكل القلبية المفاجئة لدى شباب يبدو عليهم الصحة ليست عشوائية—إنها مكتوبة، على الأقل جزئياً، في حمضهم النووي. يستعرض هذا المقال بروتين «الغراء» القلبي الرئيس المسمى ديسموغليين‑2 ويبين كيف أن تغييرات صغيرة في جينه يمكن أن تضعف عضلة القلب، وتعطل إيقاعه الكهربائي، وتزيد خطر أحداث خطيرة. من خلال الجمع بين قواعد بيانات جينية ضخمة ومجموعة إيطالية تم متابعتها بعناية، يقدم الباحثون إجابات أوضح للعائلات التي تتساءل ماذا يعني نتيجة اختبار هذا الجين بالفعل.
الغراء الميكانيكي للقلب
يجب أن تلتصق خلايا عضلة القلب ببعضها بإحكام أثناء نبضها ملايين المرات خلال حياة الإنسان. يشكل ديسموغليين‑2 جزءاً من بنية مجهرية تشبه المسامير التي تقفل الخلايا المجاورة معاً حتى تتمكن من السحب كفريق واحد. يشرح المؤلفون كيف يمتد هذا البروتين من خارج الخلية، حيث يمسك بشريك مطابق على الخلية المجاورة، إلى الداخل حيث يرتبط بإطار داعم. ولأن ديسموغليين‑2 هو العضو الوحيد من عائلته الموجود في خلايا القلب، فإن أي تلف خطير فيه لا يمكن تعويضه ببديل، مما يجعل القلب عرضة بشكل خاص.
فرز التغيرات الجينية ذات المعنى من الضوضاء الخلفية
تكشف تقنيات التسلسل الحديثة عن آلاف الاختلافات في جين ديسموغليين‑2 عبر السكان، لكن معظمها لا يسبب مرضاً. راجع الفريق منهجياً 115 دراسة منشورة واستند إلى قاعدتين عامتين كبيرتين تضمّتا معاً أكثر من 5000 متغير. باستخدام قواعد مقبولة على نطاق واسع في علم الوراثة الطبية، أعادوا تصنيف كل تغيير بحسب احتمالية أن يكون ضاراً. وجدوا أن المتغيرات الضارة حقاً تتجمع في مناطق محددة من البروتين—خصوصاً المقاطع الخارجية التي تحتاج إلى الكالسيوم لتشكيل جسر صلب بين الخلايا، ومقطع قصير يجب قطعه لنضج البروتين، والمنطقة الداخلية التي تتشبث ببروتين قلبي رئيسي آخر. بقيت العديد من التغيرات «غير مؤكدة» ولكن جزءاً منها أظهر دلائل قوية على الأهمية وتم تمييزه للمتابعة الأوثق.
ما تكشفه مجموعة المرضى الإيطالية
لمعرفة كيف تتجلى هذه الأنماط الجينية في أشخاص حقيقيين، درس الباحثون 95 فرداً في إيطاليا حاملين لمتغيرات في ديسموغليين‑2 وتم تقييمهم بعمق عبر فحوص تصويرية، واختبارات إيقاع القلب، ومتابعة طويلة الأمد. استوفى نحو نصفهم معايير صارمة لاعتلال عضلة القلب الإيقاعي، وهو حالة تُستبدل فيها أجزاء من عضلة القلب ببطء بالندبة والدهون، ما يمهد لحدوث اضطرابات إيقاعية خطيرة. من بين الأقارب الحاملين للمتغير، أظهر حوالي أربعة من كل عشرة فقط علامات المرض، مما يؤكد أن نتيجة الاختبار الإيجابية للجين لا تضمن المرض لكنها تشير إلى الحاجة للمراقبة الدقيقة. أظهر الأشخاص المصابون بوضوح عبئاً ملحوظاً من أحداث إيقاعية خطيرة، بينما كانت عمليات الزرع والوفيات أقل تكراراً لكنها لم تكن معدومة.
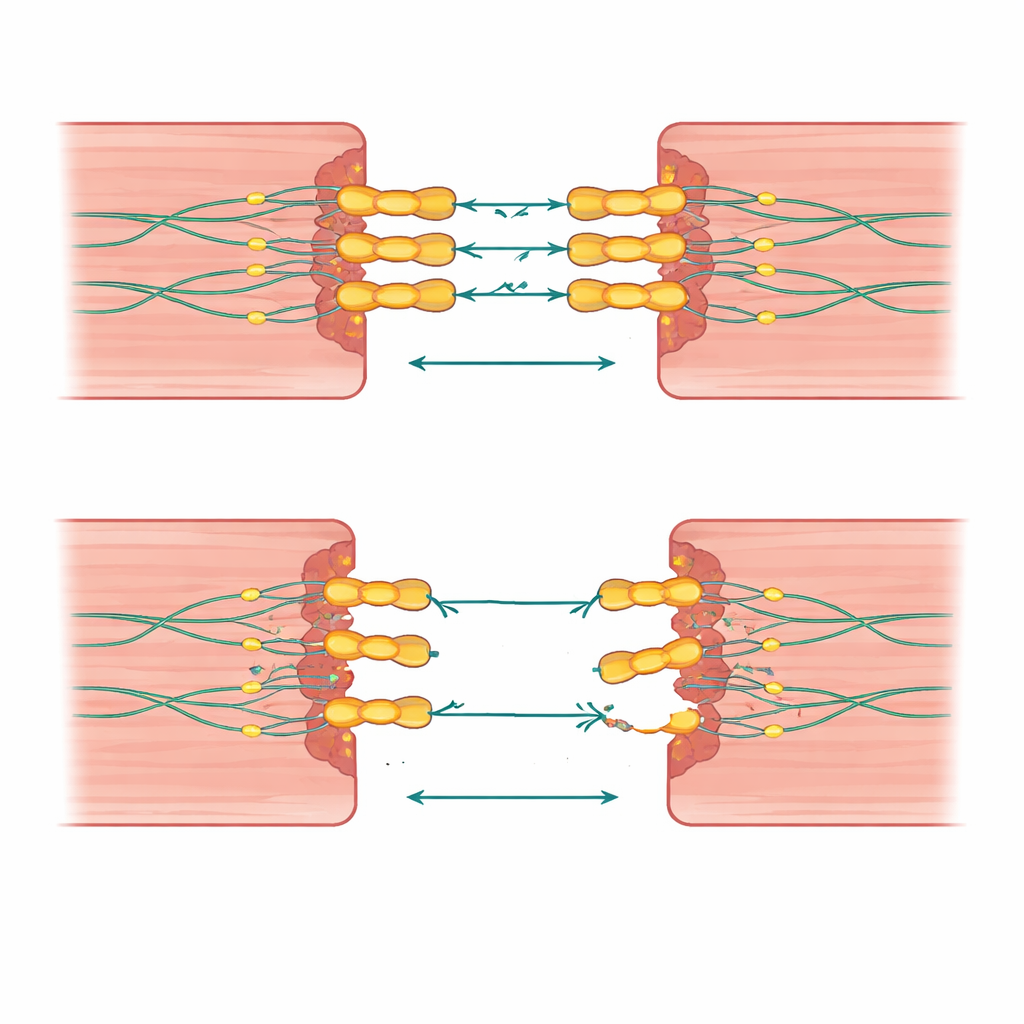
عندما لا تكفي ضربة واحدة
إحدى الرؤى اللافتة من هذا العمل هي أن عدد وتركيبة التغيرات الجينية لهما أهمية. أميل الأشخاص الذين ورثوا نسختين معيوبتين من ديسموغليين‑2، أو حاملوا متغير ديسموغليين‑2 بالإضافة إلى تغيير في جين غراء قلبي ذي صلة، إلى المرض في سن أصغر وإظهار تلف أوسع لكلا جانبي القلب. حملت بعض العائلات حذوفات أو تكرارات كبيرة أزالت أو ضاعفت ليس فقط ديسموغليين‑2 بل أيضاً جينات مجاورة، ما ربط هذه الطفرات مرة أخرى بمرض عدواني وتجمعات وفيات مفاجئة. في المقابل، كان لدى العديد من الأقارب الذين لديهم تغير واحد فقط أعراض خفيفة أو لا أعراض، مما يشير إلى أن الجينات الخلفية وعوامل الحياة مثل التمارين قد تميل بالميزان بين خطر صامت ومرض واضح.
من شكل البروتين إلى خطر المريض
لربط رمز الـ DNA بالتأثيرات الفيزيائية، استخدم الفريق نماذج ثلاثية الأبعاد متقدمة للبروتين لرؤية كيف قد تؤدي استبدالات محددة إلى إرخاء هيكل ديسموغليين‑2. التغيرات التي شوهت حلقات ربط الكالسيوم أو كسرّت نقاط ارتباط أساسية كان من المتوقع أن تُضعف استقرار البروتين وتقلل التصاق الخلية بالخلية. أدمجت هذه الدلائل البنيوية في نظام التصنيف، مما ساعد على دفع بعض المتغيرات الحدودية نحو أن تُعتبر أكثر احتمالاً ضارة أو أكثر احتمالاً حميدة. هذا الجسر بين النمذجة الجزيئية والبيانات السريرية يدفع الاختبارات الجينية إلى ما وراء مجرد قراءة الشفرة نحو فهم أكثر وظيفية.
ما الذي يعنيه هذا للمرضى والعائلات
بالنسبة للعائلات المتأثرة باعتلال عضلة القلب الإيقاعي، يقدم هذه الدراسة كل من الحذر والإرشاد. تُظهر أن ليس كل متغير في ديسموغليين‑2 هو حكم بالإصابة بمرض قلبي شديد، لكن أن أنماطاً معينة—لا سيما الضربات المتعددة أو التغيرات في مناطق حاسمة من البروتين—مرتبطة بمشكلات أبكر وأكثر خطورة. يجادل المؤلفون بأن الأشخاص الحاملين لهذه المتغيرات لا ينبغي تجاهلهم باعتبارهم «أصحاء حتى يثبت العكس»، بل يجب متابعتهم طوال حياتهم بفحوص إيقاع وتصوير مصممة حسب الحاجة. نهجهم التكاملي—المزج بين جينات البيانات الكبيرة، والدراسات العائلية التفصيلية، وبنية البروتين—يشير إلى طريق نحو تقديرات مخاطر أكثر دقة وإرشاد أكثر ثقة عندما يظهر تغير في ديسموغليين‑2 في اختبار جيني.
الاستشهاد: Pinci, S., Celeghin, R., Martini, M. et al. Integrative genomic and literature assessment of desmoglein 2-related arrhythmogenic cardiomyopathy with Italian cohort validation. Commun Med 6, 145 (2026). https://doi.org/10.1038/s43856-026-01416-w
الكلمات المفتاحية: اعتلال عضلة القلب الإيقاعي, ديسموغليين-2, أمراض القلب الموروثة, المخاطر الجينية, الموت القلبي المفاجئ