Clear Sky Science · ar
الحجب الانتقائي لتنشيط TGF-β1 الكمون يثبط تليف الأنسجة مع سلامة جيدة
لماذا يهم التندب الخفي
تتلف العديد من الأمراض المزمنة أعضائنا بهدوء عن طريق ترسيب نسيج ندبي صلب، وهي عملية تُعرف بالتليف. يمكن لهذا التندب أن يخنق الوظيفة الطبيعية ببطء في الكبد والكليتين والرئتين، وحتى حول الأورام، حيث يمكن أن يضعف أيضاً تأثيرات العلاجات المناعية الحديثة للسرطان. يقف بروتين TGF-β1 في قلب هذه العملية التليّفية، لكن إيقافه في جميع أنحاء الجسم ثبت أنه خطر. تصف هذه الدراسة جسمًا مضادًا جديدًا يسمى SOF10، مصممًا لحجب تفعيل TGF-β1 الضار فقط مع الحفاظ على أدواره الأساسية، مظهراً فوائد واعدة في نماذج حيوانية لأمراض الكبد وفشل الكلى والسرطان.
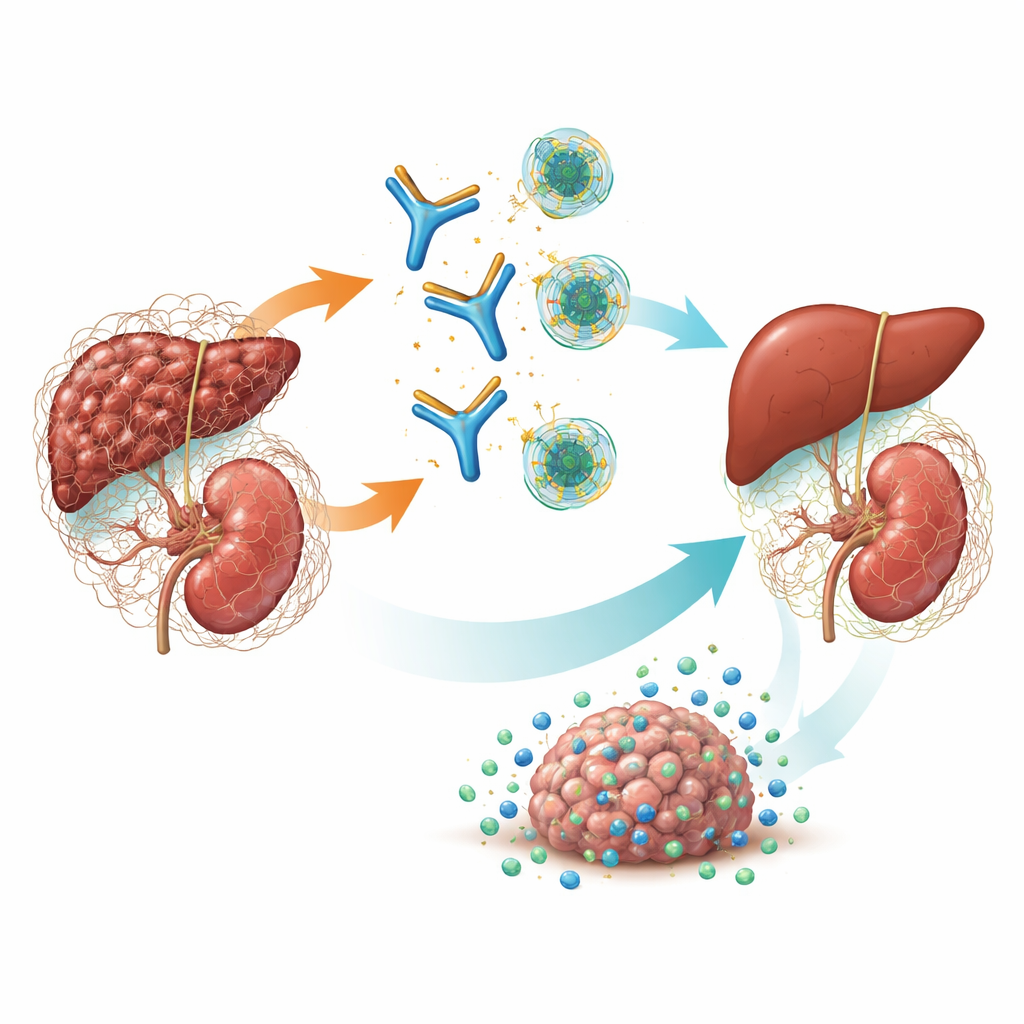
مفتاح رئيسي للتندب والسرطان
يُعد TGF-β جزيئًا إشارياً قوياً يساعد في التحكم بكيفية نمو الخلايا وشفائها وتفاعلها مع الجهاز المناعي. في المرض المزمن، يدفع أحد الأشكال—TGF-β1—الخلايا الليفية إلى بناء نسيج ضام زائد، مما يؤدي إلى تصلب الأعضاء وفشلها. كما يشكل غلافًا ليفيًا وكابحًا للمناعة حول الأورام يمنع الخلايا المناعية والأدوية من الوصول إلى الخلايا السرطانية. حاولت الأدوية السابقة إيقاف الأشكال الثلاثة لـTGF-β في آن واحد، لكن هذا «الحجب الشامل» تسبب في آثار جانبية خطيرة مثل تلف صمامات القلب والنزيف وأورام الجلد. أشارت دراسات وراثية ونماذج سابقة إلى أن TGF-β1 هو الفاعل الرئيسي في تليف الكلى والعديد من الأورام الصلبة، ما أثار الاحتمال بأن استهداف هذا النوع بدقة قد يكون فعالًا وأكثر أمانًا.
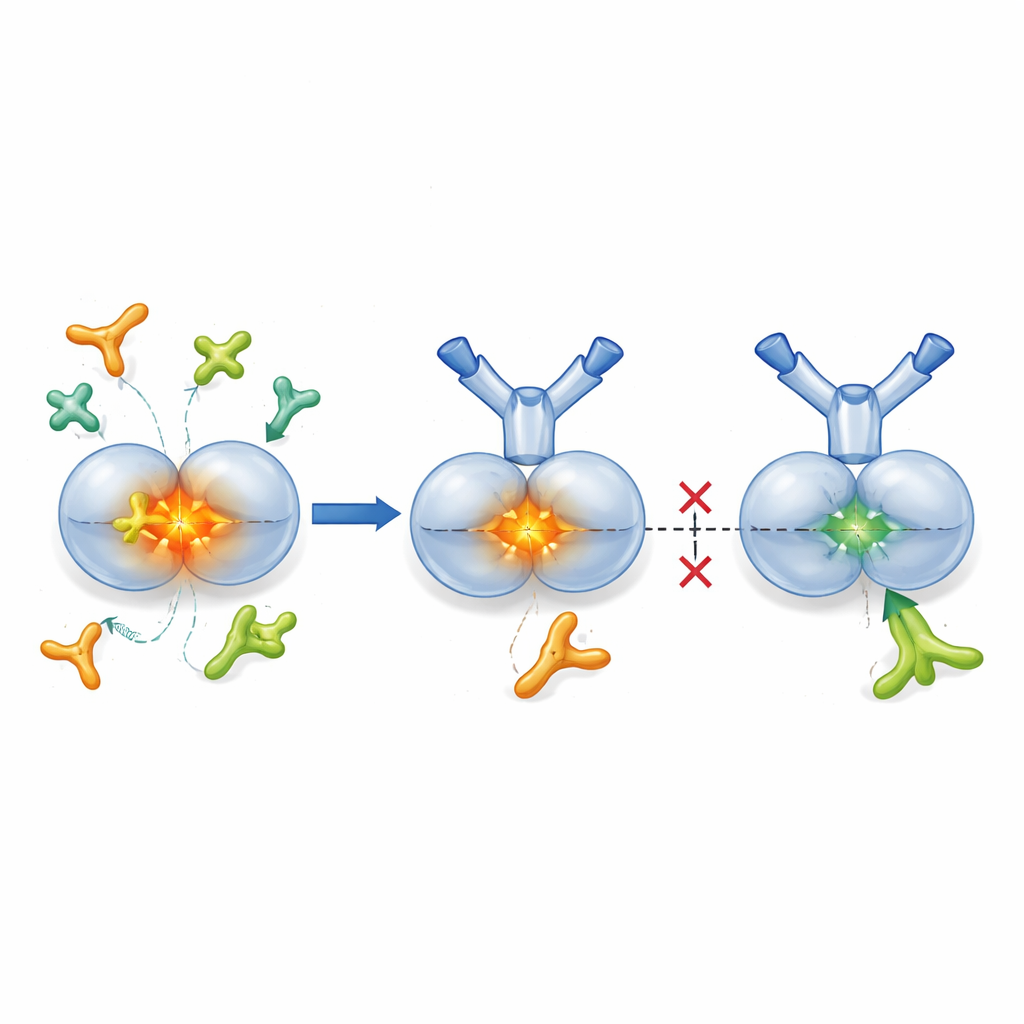
قفل TGF-β1 في صورته غير النشطة
يُنتَج TGF-β1 عادة في حزمة «كمون» حيث يُغلف اللب النشط ببروتين شريك يبقيه مطفأً حتى الحاجة. يمكن للإنزيمات المسماة بروتيزات وبعض بروتينات سطح الخلية المعروفة بالإنتيغرينات أن تفتح هذه الحزمة، مطلقةً TGF-β1 النشط في الأنسجة المجاورة. قام الباحثون بتصميم SOF10، جسم مضاد مؤنسن يرتبط فقط بالشكل الكمون لـTGF-β1، وليس بالهرمون النشط أو الأشكال الأخرى. أظهرت دراسات هيكلية باستخدام حيود الأشعة السينية أن SOF10 يندفع إلى واجهة بين نصفَي المركب الكمون، مثبتًا إياه مثل مشبك. في اختبارات المختبر، منع ذلك البروتيزات وواحدة من الإنتيغرينات (αvβ8) من تحرير TGF-β1 النشط، بينما ترك أنتيغرينًا آخر (αvβ6)—المهم للحفاظ على التوازن المناعي في الأنسجة السليمة—بالغ الأثر دون مساس يذكر. وباختصار، يخمد SOF10 مسارات التفعيل الضارة بشكل انتقائي مع الحفاظ على مسار توازن حيوي.
حماية الكبد والكلى من التلف البطيء
لاختبار ما إذا كان هذا القفل الانتقائي على TGF-β1 يمكن أن يحد فعلاً من التندب، جرب الفريق SOF10 في عدة نماذج فأرية. في نموذج غذائي سريع التحريض لمرض الكبد الدهني الذي يتقدم إلى تليف كبدي، قلل علاج SOF10 من تعبير الكبد عن الجينات المستجيبة لـTGF-β وجينات بناء الكولاجين، وخفّض مستويات الهيدروكسي برولين، وهو علامة كيميائية لتراكم النسيج الندبي. في نموذجين مختلفين للكلى—نموذج انسداد جراحي يدفع التليف الخلالي ونموذج وراثي لمتلازمة ألبورت التي تطور ندبًا كلوياً في الكبيبات وفشلًا كلويًا—قلل SOF10 نشاط الجينات الليفية وخفض محتوى الكولاجين وصغر بوضوح المناطق الندبية تحت المجهر. في نموذج ألبورت المزمن، أظهرت اختبارات الدم تحسنًا في وظيفة الكلى، وكانت هذه الفوائد مماثلة لجسم مضاد أوسع حجبًا لـTGF-β، ولكن من دون حجب الأشكال الأخرى من TGF-β.
إطلاق الجهاز المناعي داخل الأورام
بما أن النسيج الندبي حول الأورام يمكن أن يعمل كحاجز مادي وككابح مناعي، سأل الباحثون ما إذا كان SOF10 يمكن أن يحسن الاستجابة لأدوية مثبطات نقاط التفتيش المناعية. في نماذج فأرية لسرطان الثدي والقولون التي تستجيب عادة بشكل ضعيف لعلاج مضاد–PD-L1، أدى إضافة SOF10 إلى إبطاء نمو الورم بشكل كبير، بينما كان لـSOF10 أو مضاد–PD-L1 وحدهما تأثير قليل. احتوت الأورام من الحيوانات المعالجة بالمزيج على المزيد من خلايا CD8 القاتلة والمزيد من الإنزيمات السامة التي تستخدمها لتدمير الخلايا السرطانية. أظهرت الخلايا الليفية المأخوذة من هذه الأورام نشاطًا أقل في مسارات بناء الكولاجين والمصفوفة ولكن نشاطًا أعلى في مسارات الإنترفيرون وتقديم المستضدات، وهو تحول نحو نسيج داعم للمناعة. طابقت هذه التغيرات إلى حد كبير ما شوهد مع الحجب الشامل لـTGF-β، مما يشير إلى أن استهداف TGF-β1 الكمون بمفرده يمكن أن يعيد برمجة بيئة الورم بطريقة مماثلة.
إشارات سلامة في الحيوانات
نظرًا لأن المحاولات السابقة لحجب TGF-β على نطاق واسع واجهت مشاكل سلامة، أجرى الفريق دراسات سمية لمدة 13 أسبوعًا في الفئران وقرود السنجوب (cynomolgus)، مع إعطاء جرعات متكررة عالية من SOF10. تصرف الدواء مثل جسم مضاد نموذجي في مجرى الدم، وعلى مدى نطاق جرعات واسع لم تكن هناك علامات تلف في الأعضاء الرئيسية أو في تعداد خلايا الدم أو في وظيفة القلب والرئتين. تم تحديد أعلى الجرعات المختبرة—حتى 200 ملغم/كغ كل أسبوعين في الفئران و100 ملغم/كغ في القرود—كمستويات لم تُظهر آثار ضارة مرصودة. يدعم هذا الملف السلامي فكرة أن توفير TGF-β2 وTGF-β3 وتفادي تعطيل تنشيط αvβ6 يقلل المخاطر التي لوحظت مع النهج الأقل انتقائية السابقة.
ماذا قد يعني ذلك للمرضى
تشير النتائج مجتمعة إلى أن قفل TGF-β1 في غلافه غير النشط—بدلاً من محو جميع إشارات TGF-β—يمكن أن يخفف التندب في عدة أعضاء، ويحسن وظيفة الكلى، ويجعل الأورام العنيدة أكثر عرضة للعلاج المناعي، وكل ذلك مع إشارات سلامة مشجعة في الاختبارات الحيوانية. وبينما هناك حاجة لتجارب بشرية لتأكيد هذه الفوائد ومراقبة الآثار الطويلة، قد تفتح SOF10 واستراتيجيات مماثلة طريقًا جديدًا لعلاج الأمراض الليفية المزمنة وبعض السرطانات، بخفض التندب الضار مع الحفاظ على أدوار الشفاء وموازنة المناعة التي تحتاجها أنسجتنا.
الاستشهاد: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
الكلمات المفتاحية: التليف, TGF-beta1, جسم مضاد وحيد النسيلة, أمراض الكبد والكلى, المناعة السرطانية العلاجية