Clear Sky Science · ar
نقص إعادة التركيب المتناظر في سرطان الثدي الأساسي الإيجابي لمستقبل الاستروجين والسالب لـ HER2
لماذا يهم هذا لمرضى سرطان الثدي
تقع معظم حالات سرطان الثدي ضمن مجموعة كبيرة تُسمى موجبة مستقبل الاستروجين وسالبة HER2. تُعالج هذه الأورام عادةً بأدوية حاصرة للهرمونات، وأحيانًا بالاشتراك مع العلاج الكيميائي. ومع ذلك ينهار بعض المرضى ويرجع السرطان، ويعاني الأطباء من قلة أدوات دقيقة لتحديد من يحتاج فعلاً إلى علاج مكثف أو قد يستفيد من أدوية موجَّهة جديدة. تستكشف هذه الدراسة ضعفًا محددًا في بعض الأورام — يُسمى نقص إعادة التركيب المتناظر أو HRD — يجعل خلايا السرطان سيئة في إصلاح كسر الحمض النووي، مما قد يفتح الباب لعلاجات أكثر تخصيصًا.
ضعف خفي في بعض الأورام فقط
إعادة التركيب المتناظر هي أحد الأنظمة الرئيسية داخل الخلية لإصلاح الكسور الخطيرة في الحمض النووي. عندما يفشل هذا النظام — غالبًا بسبب عيوب في جينات معروفة مثل BRCA1 وBRCA2 وPALB2 أو RAD51C — تتراكم الطفرات وقد تصبح الخلايا شديدة الحساسية لأدوية معينة، بما في ذلك أدوية البلاتين ومثبطات PARP. يُعد HRD شائعًا في شكل عدواني من سرطان الثدي يُسمى ثلاثي السلبي، لكن دوره في المجموعة الأكثر شيوعًا الموجبة لمستقبل الاستروجين والسالبة لـ HER2 ظل غير واضح. لتوضيح ذلك، حلل الباحثون 502 من هذه الأورام من دراسة SCAN‑B السويدية باستخدام تسلسل الجينوم الكامل، إلى جانب بيانات مطابقة عن نشاط الجينات، ميثلة الحمض النووي، العلاجات المتلقاة، والنتائج طويلة الأمد.
كيف أُجريت الدراسة
جُمعت جميع الأورام في وقت الجراحة، قبل أي علاج دوائي، مما وفر لقطة واضحة من بيولوجيتها الأصلية. استخدم الفريق أداة متقدمة للتعرّف على الأنماط، HRDetect، لقراءة «بصمات الطفرة» التي يتركها كسر إعادة التركيب المتناظر في الحمض النووي للسرطان. وُصفت الأورام بأنها HRD إذا تجاوزت عتبة احتمال صارمة. قارن العلماء أيضًا طرقًا مختلفة لكشف HRD — من درجات معتمدة على الحمض النووي إلى اختبار التعبير الجيني القائم على RNA — ليروا مدى اتفاق الطرق المختلفة. بالإضافة إلى ذلك فحصوا سمات أوسع مثل الحمل الطفري الإجمالي، أنماط مكاسب وفقدان الكروموسومات، نشاط الجينات المرتبطة بالمناعة، والعلامات الكيميائية على الحمض النووي (الميثلة) التي يمكن أن تشغّل أو تُطفئ الجينات.
ما مدى شيوع HRD وما أسبابها؟
وجد الباحثون أن 8.4% فقط من أورام موجبة مستقبل الاستروجين وسالبة HER2 في المجموعة التي جُسّمت أظهرت أدلة قوية على HRD — وهو أقل بكثير من النسبة البالغة حوالي 60% في مرض ثلاثي السلبي. من خلال دمج هذه البيانات مع معلومات السجلات الوطنية ودراسات أخرى، قدّروا أن نحو حالة من كل 20 ورمًا في هذه الفئة السريرية، وحوالي حالة من كل 9 حالات سرطان ثدي بشكل عام في سكان غرب أوروبا/الدول الإسكندنافية، تكون HRD. في الأورام المصنفة كـ HRD تمكنوا غالبًا من تحديد سبب محتمل: نحو 70% كان لديها تلف واضح في BRCA1 أو BRCA2 أو RAD51C أو PALB2، عبر طفرات موروثة أو طفرات خاصة بالورم أو حذف جيني، أو كبت إبجيني لمحفزات الجينات. ومن اللافت أن نحو ثلث حالات HRD كانت ناتجة عن فرط ميثلة المحفز — طبقة كيمائية إضافية تُطفئ جينات إصلاح الحمض النووي دون تغيير تسلسلها. مع ذلك، نحو 30% من أورام HRD لم تُظهر ضربة مفردة واضحة، مما يشير إلى مسارات إضافية لهذه الفشل في الإصلاح لم تُكتشف بعد.
كيف تبدو أورام HRD تحت المجهر وفي العيادة
اتسمت أورام HRD في هذه المجموعة الشائعة من سرطان الثدي بسمات غالبًا ما تشير إلى مرض أكثر عدوانية: كانت لديها معدلات انقسام خلوية أعلى، ومستويات أقل من تلطيخ مستقبلات الهرمونات، وجينومات أكثر تعقيدًا وغنى بالطفرات مقارنة بالأورام المتمتعة بكفاءة إعادة التركيب. ظهرت عبر تقريبًا جميع الأنماط الجزيئية الرئيسية، لكنها كانت نادرة في فئة Luminal A الأكثر رُقَدًا ومُخصَّبة نسبيًا في مجموعة أصغر شبيهة بالقاعدية (basal‑like). ومع ذلك عندما نظر الباحثون إلى النشاط الجيني العام وأنماط ميثلة الحمض النووي، لم تقع أورام HRD ضمن بروفايل وحيد سهل التعرّف. بدلاً من ذلك كانت أنماط التعبير متنوعة، وأي فروق داخل أنواع فرعية محددة كانت متواضعة. بعض أورام HRD، وخصوصًا في مجموعات Luminal B والشبيهة بالقاعدية، أظهرت علامات أعلى لنشاط المناعة وزيادة تعبير PD‑L1، مما يوحي بأنها قد تكون أكثر وضوحًا للجهاز المناعي وربما أكثر استجابة للمناعية.
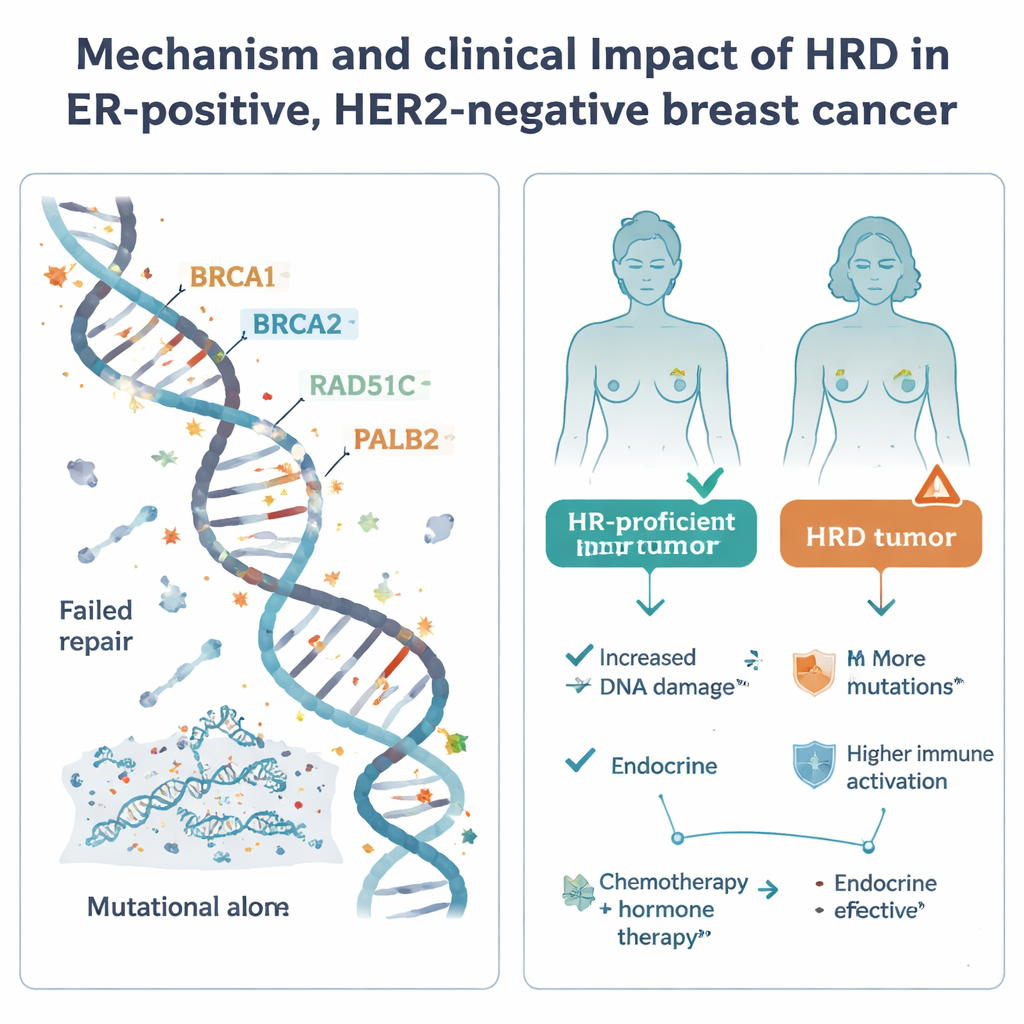
هل يغير HRD نتائج المرضى؟
ثم فحصت الدراسة كيف يرتبط وضع HRD بالنتائج في العالم الواقعي تحت الرعاية القياسية. في المرضى الذين عولجوا بالعلاج الهرموني فقط بعد الجراحة، أظهرت أورام HRD توجهًا نحو تراجع البقاء الخالي من ارتداد نقيلي أسوأ، رغم أن عدد حالات HRD كان صغيرًا ولم يصل النتيجة إلى دلالة إحصائية رسمية. هذا النمط، إلى جانب سماتها الجزيئية العدوانية، يشير إلى أن الاعتماد فقط على العلاج الهرموني قد يكون محفوفًا بالمخاطر للمرضى الذين أورامهم HRD. بالمقابل، بين المرضى الذين تلقوا كلا من العلاج الكيميائي والعلاج الهرموني، لم يكن وضع HRD مرتبطًا بوضوح بنتائج أفضل أو أسوأ؛ فقد كانت معدلات الارتداد متشابهة إلى حد كبير بين المجموعات، وقد يكون العلاج الكيميائي قد خفف بعض المخاطر الإضافية في أورام HRD.
ماذا يعني هذا لخيارات العلاج المستقبلية
بالنسبة للقارئ العام، الرسالة الأساسية هي أن قلة فقط من أورام موجبة مستقبل الاستروجين وسالبة HER2 تحمل هذا الضعف الخاص بإصلاح الحمض النووي، لكن عندما يكون موجودًا فإن ذلك يميل إلى دلالة مرض أكثر عدوانية قد لا يُتحكم فيه جيدًا بواسطة العلاج الهرموني وحده. تدعم هذه الدراسة فكرة أن تسلسل الجينوم الكامل يمكن أن يميز HRD بشكل موثوق ويوضح أسبابه الأساسية، إلى ما هو أبعد من اختبار الطفرات الموروثة في BRCA1 أو BRCA2 فحسب. على الرغم من أن الدراسة لا تثبت بعد أن تغيير العلاج استنادًا إلى حالة HRD يحسن البقاء، فإنها تقدم أدلة أولية تفيد بأن المرضى ذوي أورام HRD قد يستفيدون من العلاج الكيميائي ومن مثبطات PARP أو العلاجات المناعية في تجارب مستقبلية. باختصار، قد يصبح اختبار HRD إحدى أدوات مجموعة أدق لتفصيل شدة العلاج — وخيارات موجهة جديدة — وفقًا لبيولوجيا سرطان الثدي لكل مريض.
الاستشهاد: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
الكلمات المفتاحية: سرطان الثدي, إصلاح الحمض النووي, جينات BRCA, تسلسل الجينوم, العلاج الموجَّه