Clear Sky Science · ar
جسيمات نانوية ليبوزومية مستهدفة للأورام ومحمّلة بعقارَين على السطح للتغلّب على مقاومة العلاج في الورم الأرومي الدبقي المتعدد
لماذا يهم هذا البحث حول سرطان الدماغ
الورم الأرومي الدبقي من أشد أشكال سرطان الدماغ فتكًا. حتى مع الجراحة والإشعاع والعلاج الكيميائي، يعيش معظم المرضى قليلًا بعد سنة من التشخيص. تكمن مشكلة رئيسية في أن الأدوية التقليدية غالبًا لا تستطيع الوصول إلى الورم داخل الدماغ، وحتى عندما تصل فإن الورم يتكيف بسرعة ويصبح مقاومًا. تستكشف هذه الدراسة طريقة جديدة لتهريب أدوية متعددة عبر الحواجز الطبيعية للدماغ وتركيزها داخل الورم، بهدف جعل العلاجات الحالية مثل الإشعاع أكثر فاعلية بكثير.
شاحنة توصيل صغيرة جدًا لأدوية السرطان
بنى الباحثون حوامل أدوية فائقة الصغر تُسمى ليبوزومات مستهدفة للأورام. هذه فقاعات طرية ذات أساس شحمي بحجم أجزاء من المليار من المتر يمكنها احتواء الأدوية بداخلها. عدّل الفريق سطح هذه الفقاعات بببتيد خاص يتعرف على خلايا الورم الأرومي الدبقي ويلتصق بها، مما يساعد الجسيمات على التوجه نحو الأورام بدلًا من الأنسجة السليمة. صُممت كل فقاعة لتحمل زوجًا من الأدوية في وقت واحد: إما إيفروليموس مع فينوريليبن أو رابامايسين مع فينوريليبن. الفكرة أن الدوائين يهاجمان خلايا الورم بطرق مكملة، بينما يساعد الغلاف الحامي الأدوية على البقاء في مجرى الدم والتسلل إلى الدماغ.
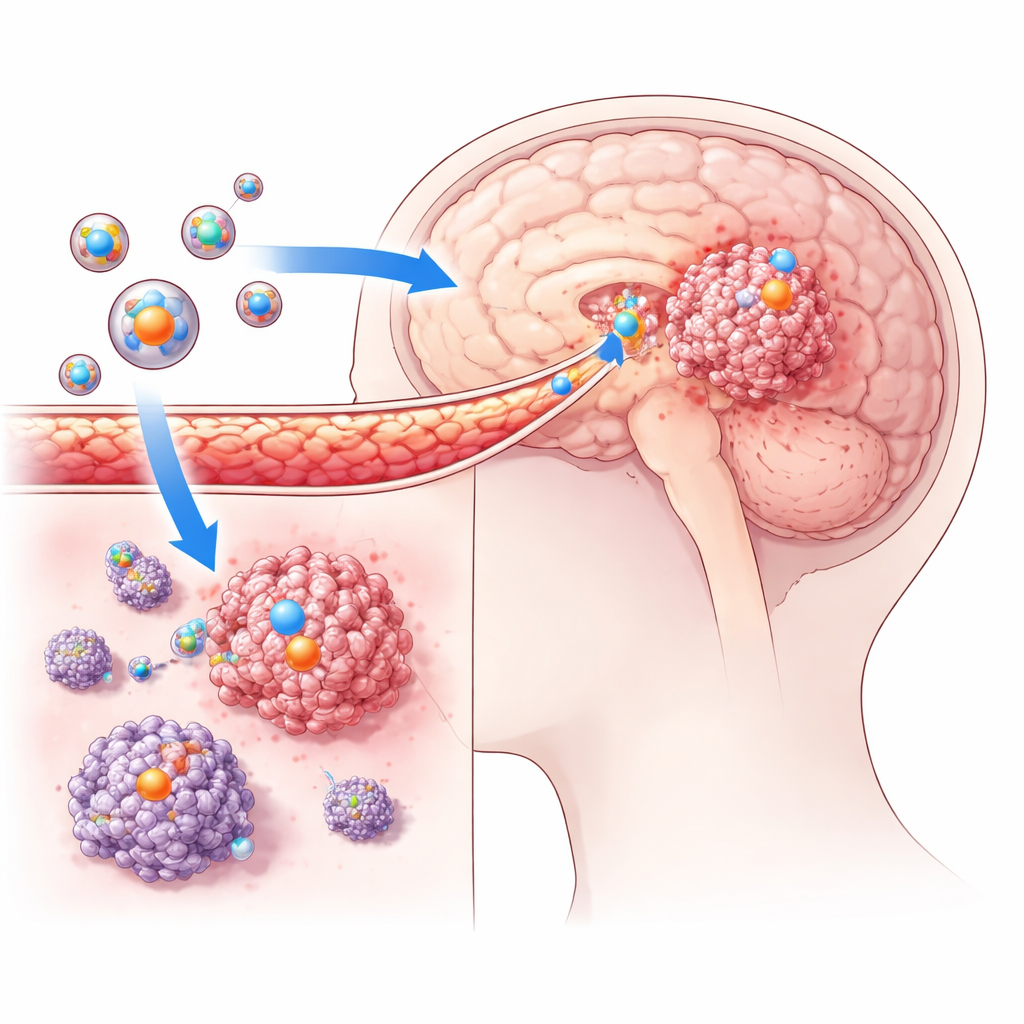
عبور جدار الدماغ الواقي
باستخدام نماذج فئران مزروعة بخلايا ورم أرومي دبقي بشرية، اختبر الفريق ما إذا كانت هذه الليبوزومات قادرة فعلاً على الوصول إلى الأورام داخل الدماغ. وسموا الجسيمات بأصباغ فلورية وتتبعوا مسارها باستخدام أدوات تصوير متقدمة. مقارنةً بالليبوزومات غير المستهدفة، أظهرت النسخ المستهدفة إشارات أقوى بكثير داخل أورام الدماغ وإشارات قليلة في المناطق الدماغية الطبيعية. وأكد ذلك أن الجسيمات المُهندسة كانت قادرة على عبور الحاجز الدموي الدماغي والتراكم تحديدًا حيث تنمو خلايا السرطان. في تجارب زراعة الخلايا، استوعبت خلايا الورم الأرومي الدبقي أيضًا كمية أكبر بكثير من الليبوزومات المستهدفة مقارنةً بالليبوزومات الضابطة، مما يعزز فكرة أن الببتيد السطحي يُحسن بشكل كبير السعي للورم والدخول إليه.
ضرب الورم بشدة مع حماية بقية الجسم
قارن العلماء أولًا مدى فعالية الليبوزومات الحاملة لدواء واحد مقابل تلك الحاملة لدوائين في قتل خلايا السرطان في الأطباق المخبرية. كانت النسخ الحاملة لدوائين، وخصوصًا تركيب إيفروليموس–فينوريليبن، أكثر فاعلية من كل دواء بمفرده، وعملت أفضل من إعطاء نفس الأدوية دون الحامل الليبوزومي. عند الجمع مع الإشعاع، ازداد التأثير قوة: شكلت خلايا السرطان مستعمرات أقل بكثير، تحركت أقل، وأظهرت علامات ضرر متزايد. في أورام دماغ الفئران، كانت الحيوانات المعالجة بالليبوزومات الحاملة لدوائين مع الإشعاع أبطأ في نمو الأورام وعاشت لفترة أطول مقارنة بمن خضعوا للإشعاع وحده أو الليبوزومات وحدها أو العلاج الكيميائي التقليدي بالتيموزولوميد. بالأهم من ذلك، لم يرَ الباحثون أذى واضحًا في أعضاء أخرى، ما يشير إلى أن تركيز العلاج داخل الورم قد يقلل من الآثار الجانبية.
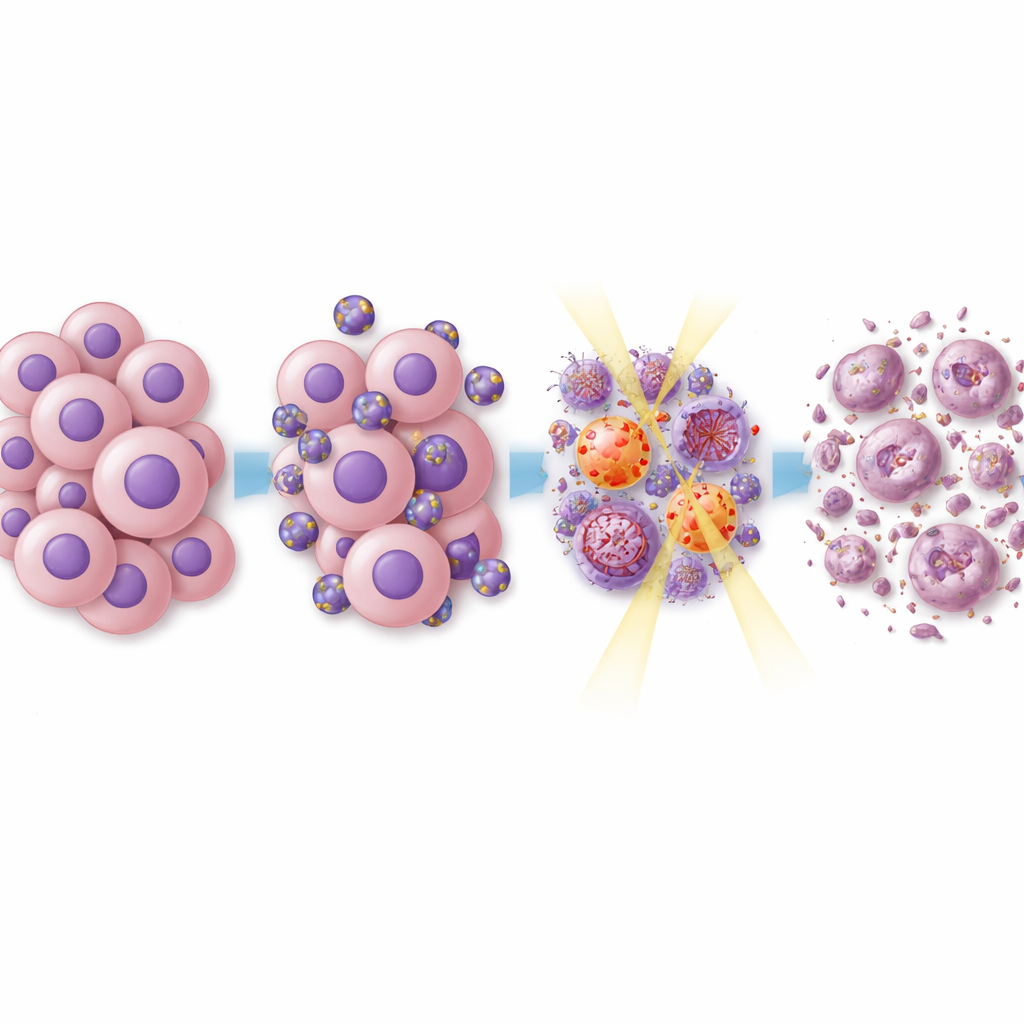
ما الذي يحدث داخل خلايا السرطان
لفهم لماذا جعل هذا النهج الأورام أكثر حساسية للعلاج، فحص الفريق نظم الإشارة الأساسية داخل خلايا السرطان. يُعرف أن الإيفروليموس والرابامايسين يثبطان مسارًا يُسمى mTOR، الذي يساعد الخلايا على النمو ومقاومة الإجهاد. كبحت الليبوزومات الحاملة لدوائين الإشارات المرتبطة بـ mTOR، وكذلك مسارات نمو أخرى تدفع انقسام وحركة خلايا الورم الأرومي الدبقي. عند إضافة الإشعاع، خفتت أيضًا البروتينات المشاركة في إصلاح تلف الحمض النووي. هذا يعني أن خلايا الورم كانت أقل قدرة على تصليح الأذى الجيني الناتج عن الإشعاع، مما يدفعها نحو الموت بدلًا من التعافي. أظهرت تحليلات تفصيلية لنشاط الجينات في الأورام المعالجة تغييرات واسعة في الشبكات المرتبطة بالتحكم في دورة الخلية وإصلاح الحمض النووي وتفاعل الورم مع الجهاز المناعي، وتم قمع العديد من الجينات المرتبطة بمقاومة العلاج.
ماذا قد يعني هذا لمرضى المستقبل
تُظهر هذه الدراسة أن جسيمات نانوية مُهندسة بعناية وراصدَة للأورام يمكنها حمل دوائين متعاونين عبر الحاجز الواقي للدماغ، وتركيزهما داخل الورم الأرومي الدبق، وجعل العلاج بالإشعاع أكثر فاعلية. في الفئران، أبطأت هذه الاستراتيجية نمو الورم ومدة البقاء دون سمّية مضافة واضحة. وبينما لا تزال هذه النتائج قبل سريرية وهناك حاجة لمزيد من الاختبارات قبل التطبيق البشري، تشير الدراسة إلى مسار عملي لدمج توصيل دوائي مستهدف مع العلاجات الحالية لتفادي سرطان شديد المقاومة. إذا تكررت فوائد مماثلة في البشر، فقد تقدم ليبوزومات محمّلة بعقارَين يومًا ما حياة أطول وجودة حياة أفضل لمرضى الورم الأرومي الدبقي.
الاستشهاد: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
الكلمات المفتاحية: الورم الأرومي الدبقي, جسيمات نانوية, ليبوزومات, علاج سرطان الدماغ, تحسيس لأشعة الإشعاع