Clear Sky Science · ar
الإمضاء البنيوي لبروتينات البلازما يصنف حالة مرض ألزهايمر
لماذا يهم اختبار دم لفقدان الذاكرة
عادةً ما يكون مرض ألزهايمر في مراحل متقدمة قبل أن تظهر مشاكل الذاكرة بشكل واضح، لكن الاختبارات الحالية لرصده مبكراً قد تكون غازية أو مكلفة أو يصعب الوصول إليها. تستكشف هذه الدراسة فكرة مختلفة: هل يمكن لتغيّرات طفيفة في الأشكال الثلاثية الأبعاد للبروتينات المتداولة في الدم أن تكشف موقع الشخص على المسار من الشيخوخة الصحية إلى النسيان الطفيف ثم إلى مرض ألزهايمر الكامل؟ إذا نجحت، قد يجعل مثل هذا الاختبار القائم على الدم فحص الأشخاص أبسط، ويدعم العلاج المبكر ويساعد الباحثين على تتبُّع من يستفيدون من علاجات جديدة.
ننظر إلى شكل البروتين، لا إلى كميته فقط
تقيس معظم اختبارات الدم مقدار جزيء معين. هنا ركز العلماء بدل ذلك على شكل البروتين. داخل خلايانا، يوجد نظام رقابة جودة يحافظ على طي البروتينات بشكل صحيح؛ عندما يضعف هذا النظام مع التقدم في السن، يمكن للبروتينات غير المطوية أن تتراكم وتلحق ضرراً بخلايا الدماغ. تساءل الفريق عما إذا كان هذا الانهيار في «صيانة البروتين» يترك بصمة بنيوية في بروتينات الدم. من بين 520 متطوعاً كانوا إما سليمين إدراكياً أو يعانون من ضعف إدراكي طفيف (MCI) أو مصابين بمرض ألزهايمر، سحبوا عينات دم واستخدموا تقنية كيميائية تسمى تحديد ملفات البروتين التساهمية لوضع علامة على الأجزاء المكشوفة من البروتينات. كلما كان الموضع أكثر انكشافاً، كان من السهل وسمه، ما يعطي قراءة رقمية لشكل البروتين مستقلة إلى حد كبير عن كمية البروتين الحاضرة.
العثور على بصمات بنيوية في الدم
عبر ما يقرب من 900 قطعة بروتينية موسومة، لاحظ الباحثون نمطاً دقيقاً لكن ثابتاً: مع انتقال الأشخاص من السليمين إلى MCI ثم إلى ألزهايمر، أصبحت أسطح بعض البروتينات أقل انكشافاً وأكثر تفاوتاً بين الأفراد. يتوافق هذا النمط مع فكرة أن رقابة طي البروتينات في الجسم تتدهور مع تقدم المرض. كما فحص الفريق كيف يؤثر عامل خطر جيني رئيسي للمرض، متغير APOE ε4، على شكل البروتين. وجدوا أن حاملي نسختين من ε4 أظهروا تحوّلات بنيوية مميزة في عدة بروتينات تتفاعل مع بروتين APOE، مما يوحي بأن هذا الجين الخطر لا يغير فقط أي البروتينات موجودة، بل كيف تُطوى وتترتب.
ربط بروتينات الدم بالمزاج والسلوك
يؤثر ألزهايمر بأكثر من الذاكرة؛ فالأعراض مثل الهياج والاكتئاب والهلوسة شائعة وغالباً ما تختلف بين الرجال والنساء. جمع الباحثون تقييمات سريرية لـ 12 نوعاً من الأعراض النفسية العصبية مع قياساتهم لشكل البروتين. في كلا الجنسين، كان سوء الأعراض يميل لأن يرافقه تحول البروتينات نحو أن تصبح أكثر «انغلاقاً» بنيوياً. بعض البروتينات، بما في ذلك الكلوسترين وعدة بروتينات أخرى مرتبطة بتراكم الأميلويد، رصدت شدة الأعراض بشكل مشابه لدى الرجال والنساء، بينما أظهرت بروتينات أخرى أنماطاً خاصة بكل جنس. تلمّح هذه النتائج إلى أن بنية بروتينات الدم قد تعكس ليس فقط وجود المرض، بل أيضاً كيف يظهر في السلوك والمزاج.
مجموعة من ثلاثة بروتينات لتصنيف مرحلة المرض
لتحويل هذه القياسات المعقَّدة إلى شيء مفيد سريرياً، أدخل الفريق البيانات البنيوية في 18 نهجاً مختلفاً لتعلم الآلة. اعتمد النموذج الأكثر أداءً، المبني على التعلم العميق، على ثلاث قطع بروتينية فقط مأخوذة من C1QA والكلوسترين (المسمى أيضاً CLUS) والأبوليبوبروتين ب (ApoB). باستخدام قراءات البنية لهذه القطع الثلاث فقط، صنف النموذج الأشخاص بشكل صحيح إلى مجموعات السليمين وMCI وألزهايمر بنحو 83% من الوقت في مجموعة اختبار مستقلة. وعند طرح أسئلة ثنائية أسهل — مثل التمييز بين السليم وMCI، أو بين MCI وألزهايمر — كان أداء اللوحة أقوى، مع مقاييس دقة قابلة للمقارنة أو أفضل من العديد من الطرق الحالية المعتمدة على مقدار البروتين بدلاً من بنيته.
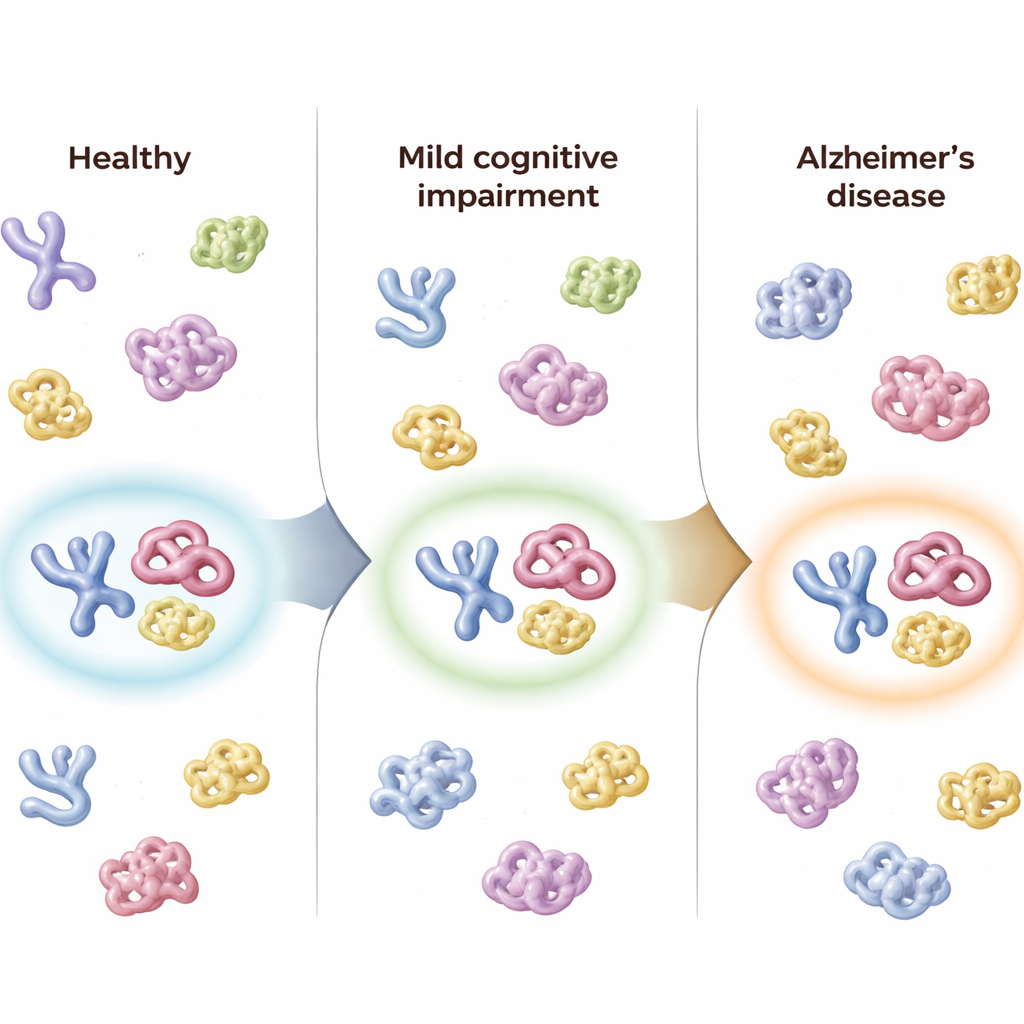
متابعة الأشخاص عبر الزمن
كان لدى الباحثين أيضاً عينات متابعة من 50 مشاركاً أُخذت حتى نحو ثمانية أشهر لاحقاً. في الأشخاص الذين ساء تشخيصهم — مثلاً من سليم إلى MCI، أو من MCI إلى ألزهايمر — انحرفت النتيجة المركبة من لوحة الثلاثة بروتينات في نفس الاتجاه، معكسة تقدم المرض. بالمقابل، أظهر الأفراد الذين بقيت حالتهم السريرية على حالها تغيراً طفيفاً في درجات اللوحة. كما أن «درجة الثقة بألزهايمر» الإجمالية للوحة توافقت عن كثب مع اختبارات الإدراك المعيارية، ومع مقاييس الوظائف اليومية، ومع ضمور الدماغ المرصود في تصوير الرنين المغناطيسي، ومع مؤشرات السائل الشوكي المعروفة للأميلويد والتاو، مما يوحي بأن الإشارة البنيوية في الدم تعكس التغيرات الأساسية في الدماغ.
ماذا قد يعني هذا للمرضى
تُظهر النتائج مجتمعة أن تغيّرات صغيرة ومنسقة في أشكال عدد قليل فقط من البروتينات الوفيرة في الدم يمكن أن تشير بشكل موثوق إلى ما إذا كان الشخص سليماً إدراكياً أو مصاباً بضعف طفيف أو بمرض ألزهايمر. ولأن الاختبار يستخدم الدم بدلاً من السائل الشوكي أو تصوير الدماغ، فإنه يمكن، من الناحية النظرية، توسيعه للفحص الروتيني أو لاختيار ومراقبة المشاركين في التجارب السريرية. يحذر المؤلفون من أن هناك حاجة لدراسات أكبر وأطول أمداً، وأن الكيمياء المستخدمة لا تزال متخصصة. ومع ذلك، تشير نتائجهم إلى أن بنية البروتين — وليس مستويات البروتين فحسب — مصدر واعد جديد للمعلومات للكشف عن مرض ألزهايمر وتتبع تطوره في وقت أبكر وبشكل أدق.
الاستشهاد: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
الكلمات المفتاحية: مؤشرات مرض ألزهايمر الحيوية, اختبار دم للخرف, تغيرات طي البروتين, تشخيص بتعلم الآلة, كلوسترين و C1QA