Clear Sky Science · ar
تحفيز الشيخوخة الخلوية أثناء ارتخاء الغدة الثديية بعد الولادة يدعم إعادة تشكيل النسيج ويعزز تكون الأورام بعد الولادة
لماذا يهم هذا للأمهات الجدد
بعد الولادة، يجب أن تتحول الثدي بسرعة من إنتاج الحليب إلى حالة راحة. هذا التحول الدرامي، المسمى الارتخاء، ارتبط منذ فترة بارتفاع مؤقت في خطر سرطان الثدي في السنوات التي تلي الحمل، لكن الأسباب البيولوجية كانت غير واضحة. تكشف هذه الدراسة في الفئران أن حالة خاصة من «التقاعد» الخلوي، تُعرف بالشيخوخة الخلوية، تساعد الثدي على التعافي بعد الفطام — ومع ذلك يمكن للبرنامج نفسه أن تُستغله الأورام الناشئة للنمو والانتشار. فهم هذه العملية ذات الحدين قد يفتح آفاقًا لطرق جديدة لحماية النساء من سرطان الثدي بعد الولادة.
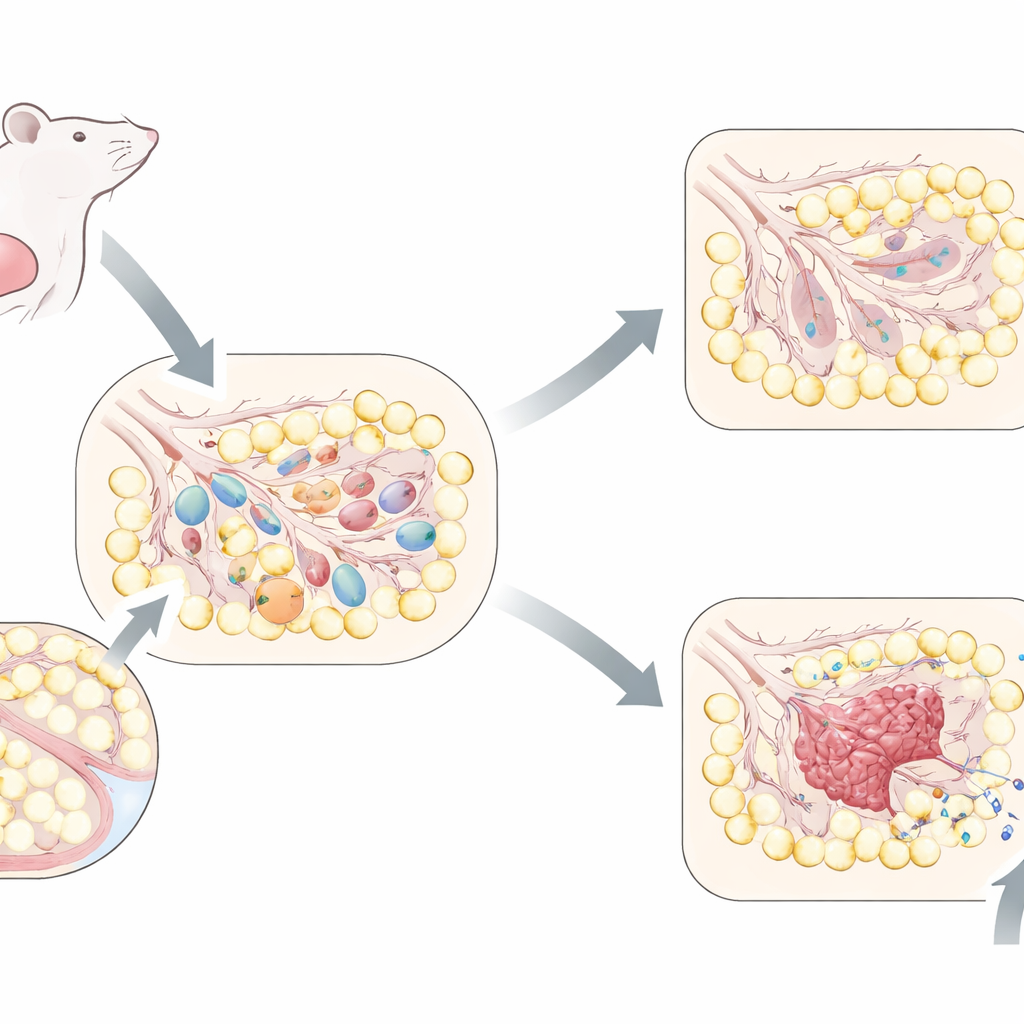
إعادة تشكيل دراماتيكية بعد انتهاء الرضاعة
أثناء الحمل والرضاعة، تتوسع الغدة الثديية لتكوّن شبكة كثيفة من الحويصلات الصغيرة التي تنتج وتخزن الحليب. بمجرد توقف الرضاعة، لم تعد معظم هذه الهياكل المنتجة للحليب ضرورية. في الفئران، يمر النسيج بتسلسل مضبوط زمنياً: أولاً يموت عدد كبير من الخلايا المنتجة للحليب، ثم يُعاد بناء الغدة مع امتلاء الفراغات بالخلايا الدهنية وإعادة تشكيل الهياكل الداعمة. تتبع المؤلفون هذه العملية عبر نقاط زمنية متعددة ووجدوا أنه بعد أيام قليلة من الفطام يظهر موجة من الخلايا التي تحمل سمات الشيخوخة الخلوية بشكل خاص في وحدات إنتاج الحليب. تختفي هذه الخلايا تدريجياً مع اكتمال عودة الغدة إلى شكلها قبل الحمل، مما يشير إلى أن الشيخوخة الخلوية هي جزء مبرمج وقصير الأمد من إعادة التشكيل الطبيعي وليس تراكمًا مرتبطًا بالعمر.
خلايا متقاعدة تساعد في إعادة تشكيل الثدي
غالبًا ما تُعتبر الخلايا المسنة مجرَّمَةً في الشيخوخة لأنها تتوقف عن الانقسام وتفرز العديد من الجزيئات الإشارية التي قد تُلهم أو تُلحق الضرر بالأنسجة المجاورة. هنا، مع ذلك، تبدو الخلايا المسنة أنها تؤدي وظيفة بناءة. باستخدام أدوات جينية، عطّل الباحثون مفتاحًا ناظمًا للشيخوخة، الجين p16، فقط في الخلايا المنتجة للحليب. كما استخدموا دواءً يقتل الخلايا المسنة انتقائيًا. في كلا الحالتين، عندما قلّت الشيخوخة، تباطأت المراحل المبكرة من الارتخاء: استمرت هياكل إنتاج الحليب لفترة أطول من المعتاد، وامتلأت الخلايا الدهنية بكفاءة أقل، واستغرق الهيكل العام للغدة وقتًا أطول لإعادة الضبط. وأظهر الفريق أيضًا أن هذه الخلايا المسنة تُطلق إشارات تجذب خلايا مناعية تُدعى البلاعم، المعروفة بمساعدتها في تنظيف الخلايا الميتة وتوجيه إصلاح الأنسجة. في هذا السياق، تتصرف الشيخوخة الخلوية كـ«مقدّم عمل» مؤقت ينظم التنظيف وإعادة البناء بعد الإرضاع.
كيف تصبح الإصلاحات مفيدة للسرطان
السمات نفسها التي تجعل الخلايا المسنة منسقين أقوياء للإصلاح تجعلها أيضًا محفوفة بالمخاطر عندما تكون هناك خلايا سرطانية حاضرة. يكون سرطان الثدي بعد الولادة أكثر احتمالًا للانتشار وأكثر فتكًا من الأورام المشخَّصة لدى النساء اللواتي لم يسبق لهن الحمل. في نماذج فأرية مهيأة لتطور أورام ثديية، تسبَّب حمل واحد متبوع بالارتخاء في ظهور الأورام أسرع. عندما قلل الباحثون الشيخوخة وراثيًا أو أزالوا الخلايا المسنة باستخدام الدواء السنوليتك ABT‑263 خلال فترة الارتخاء، ظهرت الأورام لاحقًا وبمعدل أقل. في أورغانويدات ورمية مزروعة مختبريًا، جعلت السوائل المجمعة من الغدد المرتخية والغنية بالخلايا المسنة خلايا السرطان أكثر عدوانية، في حين أن السوائل من غدد ذات شيخوخة مخففة كان لها تأثير أضعف. تشير هذه التجارب إلى أن الخلايا المسنة، من خلال مزيج العوامل التي تفرزها، تزيد من لَدونة وخطورة الخلايا المبدئية للورم المجاورة.
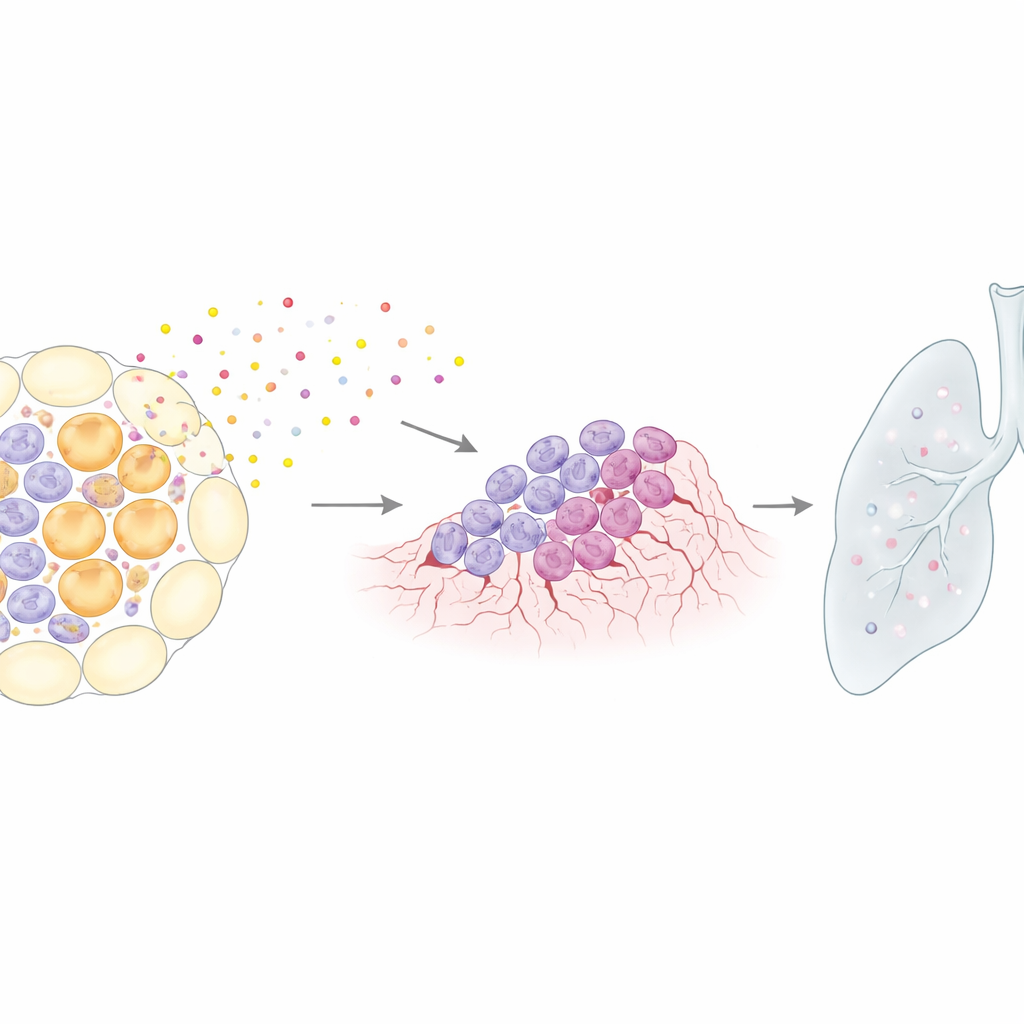
من التغيرات المحلية إلى الانتشار البعيد
بعد ذلك فحص الفريق ما إذا كان هذا الوسط المدفوع بالشيخوخة يمكن أن يشجع خلايا السرطان على الانتقال خارج الثدي. زرعوا خلايا ورم ثديي عدوانية في غدد ثديية إما في حالة راحة أو في حالة ارتخاء. في الغدد المرتخية، كانت النقائل الرئوية شائعة، لكن عندما أُزيلت الخلايا المسنة بواسطة ABT‑263 أثناء الارتخاء، انخفضت نقائل الرئة والأعضاء الأخرى بشكل ملحوظ، على الرغم من أن الدواء لم يضر الخلايا الورمية مباشرة في الحيوانات غير المرتخية. يشير هذا إلى أن فترة إعادة تشكيل ما بعد الولادة تخلق نافذة عابرة تتمكن فيها الخلايا المسنة من مساعدة الأورام على زرع والاستعمار في مواقع بعيدة. ومن المثير للاهتمام، أنه عندما حملت الإناث مرة أخرى أثناء الإرضاع — وبالتالي أُجِّل اكتمال الارتخاء وموجة الشيخوخة — خفت التسريع المعتاد لتكوّن الأورام بعد الحمل، ما يتوافق مع فكرة أن مرحلة إعادة التشكيل المرتبطة بالشيخوخة هي الفترة الخطرة.
ماذا يعني هذا لسرطان الثدي بعد الولادة
بالمجمل، تكشف الدراسة أن الشيخوخة الخلوية أثناء ارتخاء الثدي بعد الولادة هي خطوة مبرمجة تعتمد على الهرمونات تساعد الغدة على الانتقال بأمان من مصنع للحليب إلى عضو في حالة راحة. ومع ذلك، إذا كانت هناك خلايا عرضة للسرطان أو غير طبيعية بالفعل، فيمكن للخلايا المسنة نفسها أن تغذي نمو الورم وغزوه وانتشاره عن طريق تغطية النسيج بعوامل إشارية قوية. للقراء غير المتخصصين، الخلاصة أن أدوات الجسم لإصلاح الجروح يمكن أن تختطفها السرطان في لحظات ضعف مثل ما بعد الولادة. في المستقبل، قد تحافظ العلاجات الموقوتة بعناية التي تستهدف الخلايا المسنة — أو الإشارات التي تطلقها — على فوائد الإصلاح النسيجي الطبيعي مع خفض الخطر المرتفع لسرطان الثدي بعد الولادة.
الاستشهاد: Chiche, A., Djoual, L., Charifou, E. et al. Induction of senescence during postpartum mammary gland involution supports tissue remodeling and promotes postpartum tumorigenesis. Nat Aging 6, 541–559 (2026). https://doi.org/10.1038/s43587-025-01058-y
الكلمات المفتاحية: سرطان الثدي بعد الولادة, الشيخوخة الخلوية, ارتخاء الغدة الثديية, انبثاث الورم, العلاج القاتل للخلايا المسنة