Clear Sky Science · ar
مقاومة العلاج بالمستحضرات المحتوية على البلاتين في سرطان الرئة والمبيض مدفوعة بإفرازات الشيخوخة الخلوية القابلة للاستهداف عبر TGFβ
عندما ينقلب علاج السرطان ضد المريض
يعد العلاج الكيميائي القائم على البلاتين واحدًا من أعمدة علاج السرطان الحديث، لا سيما في حالات سرطاني الرئة والمبيض. فهدفه إحداث تلف شديد في حمض نووي الورم بحيث تعجز الخلايا السرطانية عن الانقسام. ومع ذلك، يلاحظ كثير من المرضى تقلص الأورام في البداية ثم عودتها أقوى من قبل. تطرح هذه الدراسة سؤالًا بسيطًا لكنه مزعجًا: هل يمكن أن تكون الأدوية نفسها التي تنقذ الأرواح أيضًا سببًا في استعادة الخلايا السرطانية الناجية لقدرتها على النمو؟ يجد المؤلفون أن الجواب يكمن في مجموعة خاصة من الخلايا التالفة المشابهة للخلايا المسنة والرسائل الكيميائية القوية التي تطلقها.
الحياة المزدوجة لخلايا السرطان المسنة
لا يعامل العلاج الكيميائي جميع خلايا الورم بالطريقة نفسها. فبعضها يُقتل تمامًا، لكن البعض الآخر يدخل حالة تسمى الشيخوخة الخلوية — حالة توقف دائم عن الانقسام، ومع ذلك الخلايا لا تزال حية. تنتفخ هذه الخلايا المسنة وتبدأ في إفراز كوكتيل من البروتينات والإشارات المعروف باسم النمط الإفرازي المرتبط بالشيخوخة الخلوية (SASP). باستخدام خلايا سرطان الرئة والمبيض البشرية في المختبر، وكذلك نماذج الفأر، أظهر الباحثون أن أدوية البلاتين مثل سيزبلاتين وكاربوبلاتين تولد خلايا مسنة ذات قدرة إفرازية قوية بشكل خاص. عندما وُضعَت خلايا سرطانية جديدة في وسط مأخوذ من هذه المستعمرات المسنة، نمت بشكل أسرع، وتحركت بسهولة أكبر، وشكلت تجمعات وكرات أكبر وأكثر عدوانية مقارنة بالخلايا الضابطة.
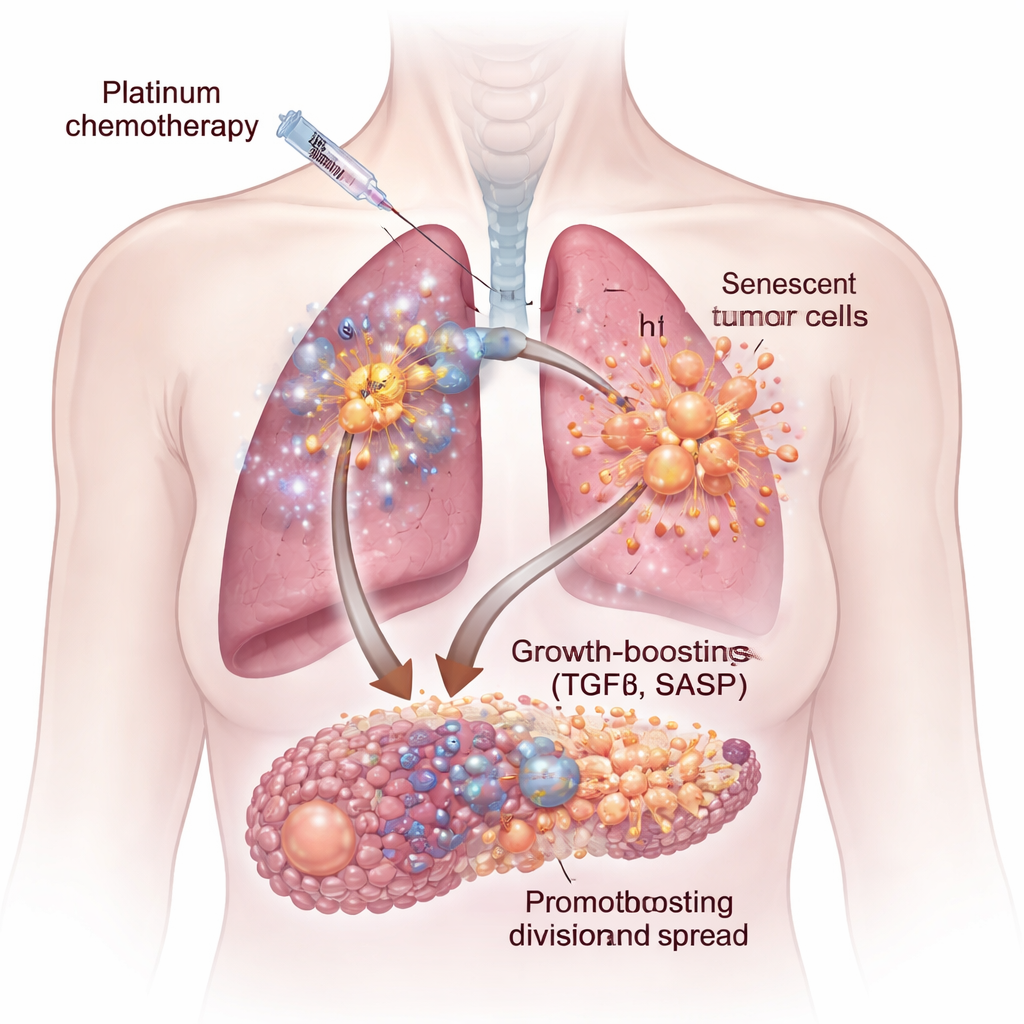
إشارة نمو مخفية: TGFβ
لم تُحفز كل العلاجات الكيميائية نفس الإفرازات الضارة. عندما قارن الفريق أدوية البلاتين بعاملين شائعين آخرين، دوكسيتاكسيل وبالبوسيكليب، كانت خلايا المعالجة بالبلاتين فقط هي التي أنتجت SASP يعزز نمو الورم بقوة. من خلال دمج دراسات التعبير الجيني وقياسات البروتين ومصفوفة ميكروبيئة عالية الإنتاجية، حددوا الجاني الرئيسي: جزيء الإشارة المعروف بتحويل عامل النمو بيتا (TGFβ). كانت الخلايا المسنة المحفزة بسيزبلاتين غنية بأشكال متعددة من TGFβ والمسارات المرتبطة به. إضافة TGFβ منقى إلى الخلايا السرطانية نقشت تأثير النمو المشاهد مع سوائل الخلايا المسنة، ما يبرز هذه العائلة من السيتوكينات كسائق مركزي للإفرازات المؤيدة للورم.
كيف تعيد الإشارة برمجة الخلايا السرطانية
ثم تتبعت الدراسة كيف تغير هذه الإشارات الغنية بـTGFβ سلوك الخلايا الورمية المجاورة. على سطح الخلايا المستقبلة، يرتبط TGFβ بمستقبل يسمى TGFBR1. هذا بدوره يشغل سلسلة داخلية من البروتينات — لا سيما مسارات AKT وmTOR — المعروفة بالتحكم في نمو الخلية والأيض والبقاء. في خلايا سرطان الرئة البشرية والفأرية، أدت التعرض لإفرازات مُشتقة من سيزبلاتين إلى زيادة سريعة في الأشكال النشطة (الفوسفورية) من AKT ومستهدفه التالي p70S6K، وعززت التعبير عن جينات دورة الخلية. حجب TGFBR1 بدواء يسمى جالونيسيرتيب، أو تثبيط mTOR مباشرة، أوقف إلى حد كبير هذا الطوفان الإشارِي وخفّض التكاثر الإضافي وتكوين المستعمرات ونمو الكرات الغازية المحفزة بواسطة الإفرازات المسنة.
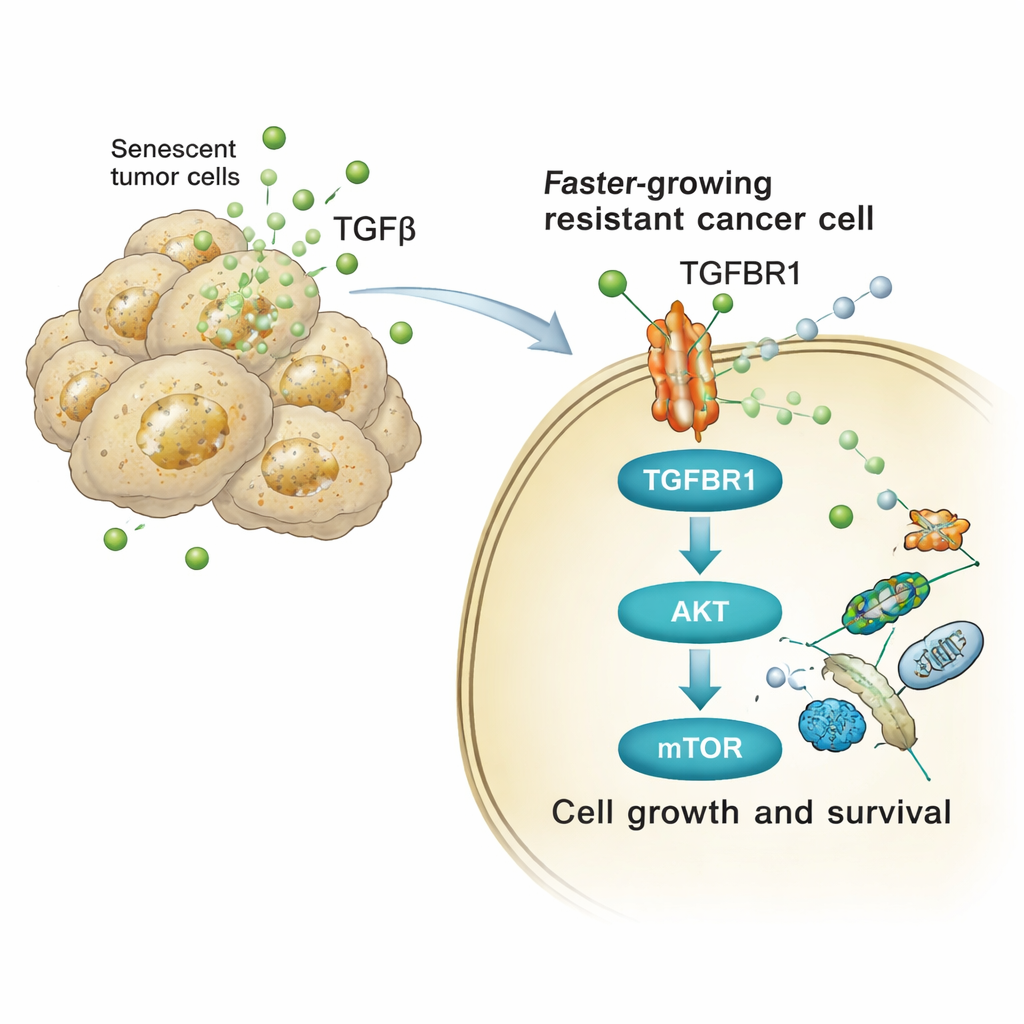
من الفئران إلى المرضى: نقطة ضعف مشتركة
لم تقتصر هذه الآليات على أطباق بتري. في فئران تحمل أورام رئوية، أدى خلط خلايا سرطانية مسنة وغير مسنة إلى أورام تنمو بسرعة أكبر وبقاء أقصر، بينما قلصت إزالة الخلايا المسنة أو حجب TGFBR1 هذا التأثير. عندما أعطيت جرعات سيزبلاتين القياسية لفئران مصممة وراثيًا للإصابة بسرطان الرئة، تراكمت علامات الشيخوخة جنبًا إلى جنب مع نشاط مرتفع لمسارات AKT/mTOR في الخلايا المجاورة التي لا تزال منقسمة. أدى الجمع بين السيزبلاتين وحجب TGFBR1 أو الأدوية السينية للشيخوخة (senolytics) — التي تقتل الخلايا المسنة انتقائيًا — إلى تقليل عبء الورم وتمديد البقاء مقارنة بالعلاج الكيميائي وحده. والأهم من ذلك، أظهرت تحليلات عينات بشرية من سرطان الرئة وسرطان المبيض المصاحب بدرجة عالية بعد العلاج القائم على البلاتين نمطًا مشابهًا: زيادة مؤشرات الشيخوخة وارتفاع إشارات AKT/mTOR في ميكروبيئة الورم، لا سيما في مناطق غنية بالخلايا المسنة.
تحويل نقطة ضعف إلى ميزة
خلاصة القول لغير المختص هي أن العلاج بالبلاتين يمكن أن يترك وراءه تجمعًا من الخلايا التالفة ولكن الخطرة — خلايا "الزومبي" المسنة. هذه الخلايا لا تنقسم بعد الآن، لكنها تفرز إشارات غنية بـTGFβ توقظ الخلايا السرطانية المجاورة، مما يساعد الأورام على النمو مجددًا ومقاومة العلاجات التالية. والخبر المشجع هو أن هذه النقطة الضعيفة قابلة للاستهداف. في نماذج ما قبل السريرية لسرطاني الرئة والمبيض، جعلت إضافة أدوية تحجب مستقبل TGFβ (TGFBR1) أو تزيل الخلايا المسنة العلاج بالبلاتين أكثر فعالية وحسّنت البقاء دون سمية إضافية واضحة. تشير الدراسة إلى تجارب سريرية مستقبلية قد تجمع بين العلاج بالبلاتين واستراتيجيات سنوليتك أو مضادة لـTGFβ، بهدف الحفاظ على فوائد العلاج الكيميائي مع تعطيل آثاره الجانبية الخفية المدفوعة بالشيخوخة الخلوية.
الاستشهاد: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
الكلمات المفتاحية: مقاومة العلاج الكيميائي, الشيخوخة الخلوية, إشارة TGFβ, سرطان الرئة, سرطان المبيض