Clear Sky Science · ar
تستهدف السموم المعمرة الشيخوخة عبر خصوصية ربط الدهون، خلل الأيونات وإعادة تشكيل الليبيدوم
لماذا قد يجعل قتل خلايا «الزومبي» علاج السرطان أكثر فعالية
مع التقدّم في العمر — أو بعد تعرّضنا لعلاجات قاسية مثل العلاج الكيميائي — تتوقف بعض الخلايا عن الانقسام لكنها ترفض الموت. هذه الخلايا «الزومبي»، المعروفة بالخلايا المعمرة (senescent cells)، تفرز جزيئات التهابية تضر الأنسجة وقد تساعد الأورام على الظهور مجدداً. تستكشف هذه الدراسة طريقة مفاجئة جديدة لاستهداف هذه الخلايا الانتقائية باستخدام بروتين مستمد من سم، مما قد يجعل علاجات السرطان أقوى وأكثر أماناً.
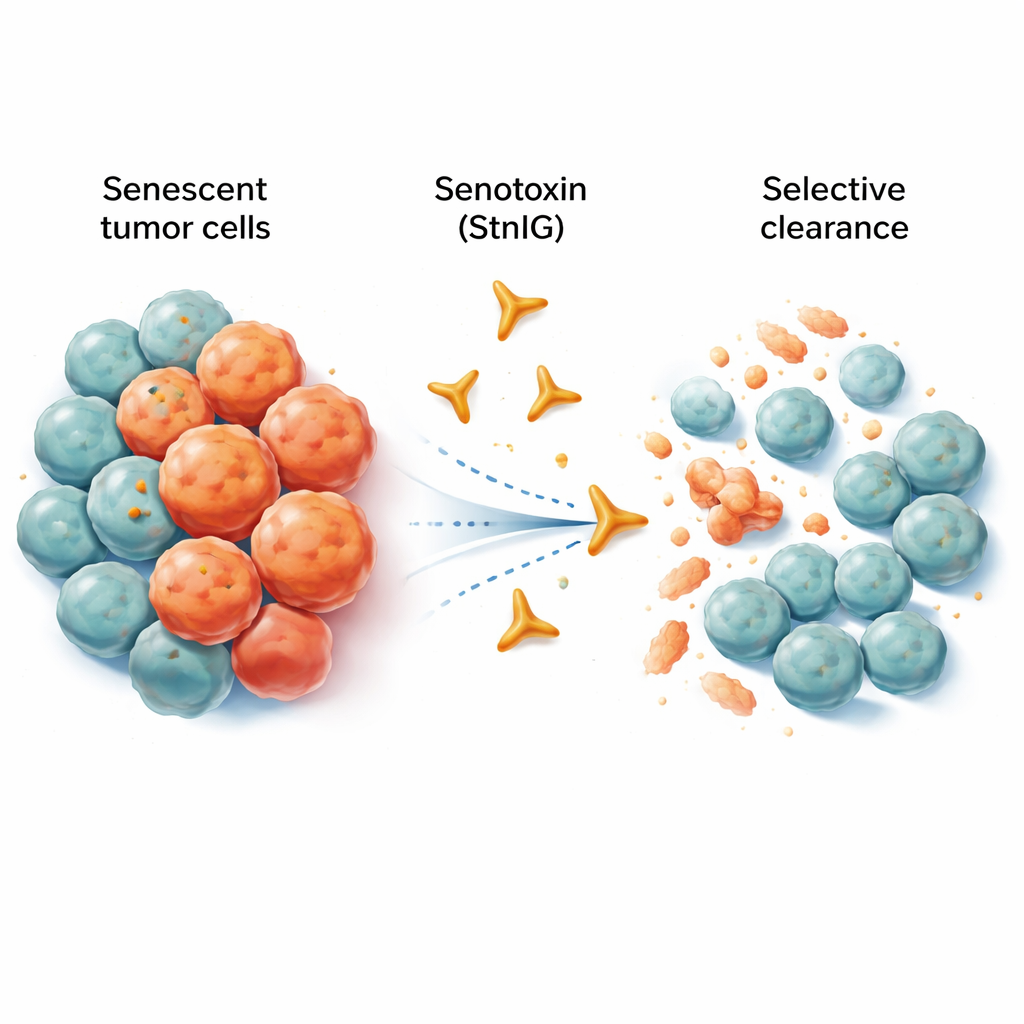
خلايا مسنّة لا تريد الرحيل
الخلايا المعمرة تشبه عمالًا متقاعدين لا يزالون يحتلون مكاتبهم ويعطّلون العمل في المكان. لم تعد تتكاثر، لكنها تُطلق مزيجاً من الإشارات الالتهابية التي يمكن أن تضعف الأنسجة المجاورة، تسرّع الشيخوخة، وحتى تدعم نمو الأورام وانتشارها. بينما يقتل العلاج الكيميائي العديد من خلايا السرطان، غالباً ما يترك وراءه مجموعة من الخلايا المعمرة داخل الورم وحوله. هذه الخلايا المتبقية تُغذّي الالتهاب المزمن والأعراض الجانبية وقد تؤدي في النهاية إلى انتكاس المرض. تهدف الأدوية التجريبية المعروفة بالمزيلات الخلوية المعمرة (senolytics) إلى إزالة هذه الخلايا، لكن العديد منها يؤثر أيضاً على الخلايا السليمة، أو يعمل ضمن نطاق جرعات ضيق جداً، أو يصعب امتصاصه في الجسم.
تحويل سم شقائق النعمان إلى أداة دقيقة
اتّجه الباحثون إلى متخصصي الطبيعة في قتل الخلايا: سموم الحيوانات. ركّزوا على بروتين مكوّن للمسام يدعى ستيكوليسين I (StnI) الموجود في شقائق نعمان بحر الكاريبي. يمكن لهذا البروتين أن يفتّح ثقوباً صغيرة في أغشية الخلايا. اكتشف الفريق أن StnI، والنسخة المصمّمة والمحسّنة التي ابتكروها والمسمّاة StnIG، أكثر فعالية بشكل لافت في قتل الخلايا السرطانية المعمرة مقارنة بجيرانها غير المعمرين. عبر عدة أنواع من خلايا سرطانية بشرية (الميلانوما والكبد والرئة والأورام المشتقة من الأعصاب) التي دُفعَت إلى الحالة المعمرة بواسطة أدوية كيميائية، قضى StnI وخاصة StnIG على الخلايا المسنة بجرعات أقل بكثير مما يلزم للتأثير على الخلايا النامية بنشاط. كانت StnIG أكثر انتقائية من دواء تجريبي رائد للمزيلات الخلوية يسمى نافيتوكلكس (navitoclax)، ما يشير إلى أن السموم المولفة بعناية يمكن أن تتفوق على النهج الحالية.
كيف تصبح الأغشية الخلوية المتغيرة نقطة ضعف
الخلايا المعمرة لا تتغير فقط داخلياً؛ غشاؤها الخارجي — البشرة الدهنية المحيطة بكل خلية — يعيد ترتيب مكوناته أيضاً. في الخلايا السليمة، توجد دهون معينة أساساً على الجانب الداخلي للغشاء، مخفية عن العالم الخارجي. في الخلايا المعمرة ينهار هذا التوازن، وتنكشف هذه الدهون على السطح. باستخدام تحليلات كيميائية مفصّلة ومحاكاة حاسوبية، أظهر الفريق أن StnIG يتعرّف ويلتصق بهذا المشهد الليبيدي المعدّل. بنيته مناسبة بشكل خاص للارتباط بأنواع محددة من الدهون التي تكشفها الخلايا المعمرة على سطحها. بمجرد الالتحام، يشكّل StnIG مسامات تسمح بتدفق الذرات المشحونة، أو الأيونات، داخل وخارج الخلية بطريقة شديدة الاختلال.
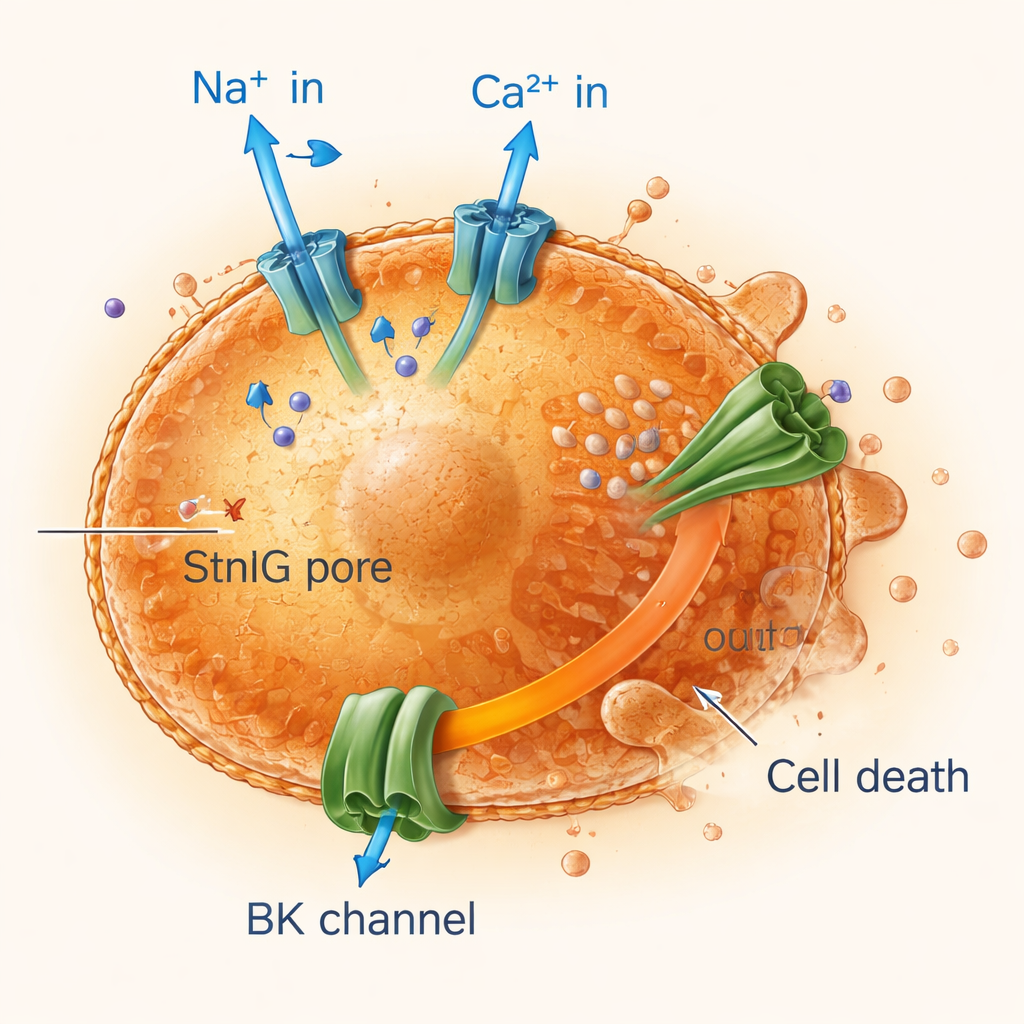
قطع دارات الخلايا المسنة عبر اختلال الأيونات
بمتابعة الكهرباء وحركة الأيونات عبر أغشية الخلايا، وجد الباحثون أن مسامات StnIG تسمح بتدفق أيونات الصوديوم والكالسيوم إلى داخل الخلايا المعمرة بينما يتسرّب البوتاسيوم إلى الخارج باستمرار. يؤدي اندفاع الكالسيوم إلى تفعيل قنوات بوتاسيوم كبيرة، مما يضاعف فقدان البوتاسيوم، الذي يعدّ بالغ الأهمية للحفاظ على حجم الخلية وبقائها. الخلايا المعمرة، التي هي بالفعل أقل مرونة وأكثر هشاشة من الخلايا السليمة، لا تستطيع التعامل مع هذا الاضطراب الأيوني المستمر. تفقد ميتوكوندرياها — محطات الطاقة الخلوية — شحنتها الكهربائية، وتنخفض إنتاجية الطاقة، وتدخل الخلايا في أشكال مبرمجة من الموت، بما في ذلك الاستماتة (apoptosis) وموت التهابي حارق يُعرف بالبيروبتوسيس (pyroptosis). حجب دخول الكالسيوم أو قنوات البوتاسيوم حمى الخلايا المعمرة، مؤكداً أن هذا الاضطراب الأيوني محوري في آلية السم.
من أطباق الخلايا إلى الكائنات الحية
اختبر الفريق بعد ذلك ما إذا كانت هذه الاستراتيجية تنجح في كائنات حية. في أجنة السمك الزيبرا التي حملت خلايا ميلانوما بشرية معمّرة، خفّضت جرعات منخفضة من StnIG عدد هذه الخلايا بفعالية مماثلة لدواء نافيتوكلكس، دون سُمّية واضحة. في نماذج فأرية للميلانوما وسرطان الكبد، أبطأ العلاج الكيميائي باستخدام دواء يوقف دورة الخلية (بالبيسيسليب) نمو الورم بدفع العديد من خلايا السرطان إلى الحالة المعمرة. عندما أضاف الباحثون StnIG متقطعاً، تقلصت الأورام أو دخلت في هدنة أفضل من العلاج الكيميائي وحده، وبما يتوافق مع مجموعة العلاج الكيميائي–نافیتوكلکس. من المهم أن الفئران المعالجة بـStnIG أظهرت آثاراً جانبية محدودة ولا أضرار واضحة في الأعضاء الرئيسية، رغم أن البوتاسيوم في الدم ارتفع لدى الحيوانات التي كانت تحمل أوراماً معمّرة — وهو ما يعكس على الأرجح الإفراج الضخم للبوتاسيوم نتيجة تدمير خلايا الورم.
ماذا يعني هذا لعناية السرطان المستقبلية
تقدّم هذه الدراسة مفهوم «السموم المعمرة»: بروتينات مُهندَسة مستوحاة من السم تستغل خصائص الغشاء ومناولة الأيونات الفريدة للخلايا المعمرة. عبر التركيز على الدهون المتغيرة وإحداث اختلالات أيونية قاتلة، يمكن لـStnIG إزالة الخلايا المعمرة الضارة انتقائياً مع الحفاظ على معظم الأنسجة السليمة. مستخدمة إلى جانب العلاج الكيميائي، قد تساعد مثل هذه السموم في المستقبل على تنظيف خلايا الزومبي التي تغذّي الانتكاس والالتهاب المزمن، مما يجعل علاجات السرطان أكثر دواماً وقد يخفّف بعض الآثار الجانبية طويلة المدى.
الاستشهاد: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
الكلمات المفتاحية: الشيخوخة الخلوية, مزيلات الخلايا المعمرة, علاج السرطان, أدوية مشتقة من السموم, قنوات الأيونات