Clear Sky Science · ar
تخليق وتطبيق جسيمات النانو من فيبروين الحرير لتوصيل الدواء
قريب حرير العنكبوت كحامل دوائي أذكى
تخيل لو أن المادة نفسها التي تصنع شرنقة دودة الحرير يمكن أن تساعد الأدوية على الوصول إلى الأنسجة المريضة مع حماية بقية الجسم. تستعرض هذه المقالة كيف يمكن تحويل فيبروين الحرير — البروتين الرئيسي في حرير دودة القز — إلى جسيمات صغيرة تنقل الأدوية مباشرة إلى الأورام والأمعاء الملتهبة والجروح. للقارئ، إنها لمحة عن كيفية تحويل مادة طبيعية مألوفة بهدوء علاج السرطان وصحة الأمعاء وإصلاح الأنسجة.
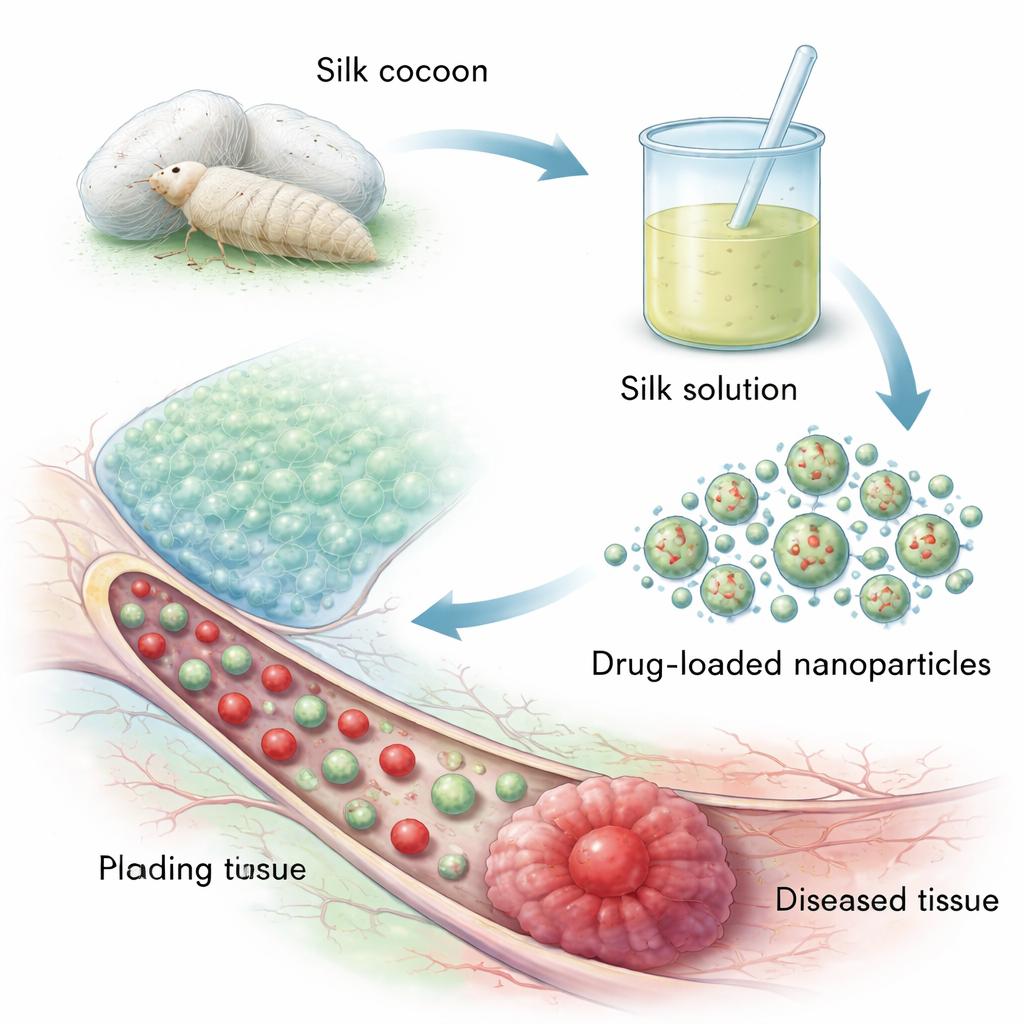
من خيوط الشرنقة إلى عبوات دوائية صغيرة
يُستخرج فيبروين الحرير من شرانق دودة القز المُروَّضة، وهو مصدر يمكن تربيته بسهولة مقارنةً بحرير العنكبوت. تحتوي الشرنقة على نواة قوية من فيبروين مغلفة ببروتين آخر، السيريسين، الذي قد يثير استجابات مناعية. لإنتاج حرير بمواصفات طبية، يزيل المصنعون أولاً السيريسين في عملية تُسمى «إزالة الغبار»، ثم يذيبون وينقّون ويجففون الفيبروين. على المستوى الجزئي، يتكوّن فيبروين الحرير من سلاسل طويلة ومتكررة من أحماض أمينية بسيطة مثل الغليسين والألانين التي يمكن أن تطوى إلى مناطق مكثفة منظمة تعرف بصفائح بيتا. هذه المناطق المرتبة تمنح الحرير قوته وتتيح للعلماء ضبط سرعة ذوبانه في الجسم، وهي خاصية أساسية للتحكم في مدة إطلاق الدواء.
طرق تشكيل الحرير إلى جسيمات نانوية
طور الباحثون عدة طرق لتحويل محاليل الحرير السائلة إلى جسيمات نانوية بعرض عشرات إلى بضع مئات من النانومترات. في طرق الإزالة المذيبة، تُسقط محاليل الحرير في مذيب غير مناسب مثل الإيثانول، مما يدفع سلاسل البروتين إلى الطي إلى صفائح بيتا والتجمع الذاتي إلى كرات صلبة. تقنيات الاستحلاب تخلق قطرات ماء‑في‑زيت تتصلب لتصبح جسيمات، مفيدة لحمل الأدوية الزيتية لكنها تتطلب إزالة المذيب بعناية. الرش الكهربائي يستخدم جهدًا عاليًا لتفتيت محلول الحرير إلى قطرات مشحونة رفيعة تجف في الهواء لتصبح جسيمات، بينما تخلط رقائق الميكروفلويب «الحرير» و«المضادات مذيب» في قنوات صغيرة لتوليد جسيمات نانوية موحدة وقابلة للتكرار. كل نهج يوازن بين التكلفة، والتحكم بحجم الجسيمات، وسهولة التصنيع على نطاق واسع.
ضبط الحرير للإطلاق المستهدف والموقوت
بما أن فيبروين الحرير غني بمجموعات كيميائية تفاعلية، يمكن تعديله مثل قطع الليغو بإضافة عناصر إضافية. يربط الكيميائيون جزيئات صغيرة أو بوليمرات أو «علامات» بيولوجية لتغيير تفاعل الجسيمات مع الماء، وسرعة تحللها، أو الخلايا التي تلتصق بها. على سبيل المثال، إضافة بولي إيثيلين غليكول (PEG) يمكن أن يجعل الجسيمات أكثر استقرارًا في الدم وأقل ظهورًا للجهاز المناعي، بينما يساعد ربط شظايا بروتينية قصيرة أو فيتامينات على ارتباطها بمستقبلات خلايا الورم. والأهم من ذلك أن محتوى صفائح بيتا والوصلات المضافة يمكن تعديله بحيث تستجيب جسيمات الحرير للبيئة: قد تنحل في ظروف حمضية، أو بوجود إنزيمات معينة، أو في مناطق مؤكسدة، مطلقةً الدواء تحديدًا حيث تكون الأنسجة مريضة.
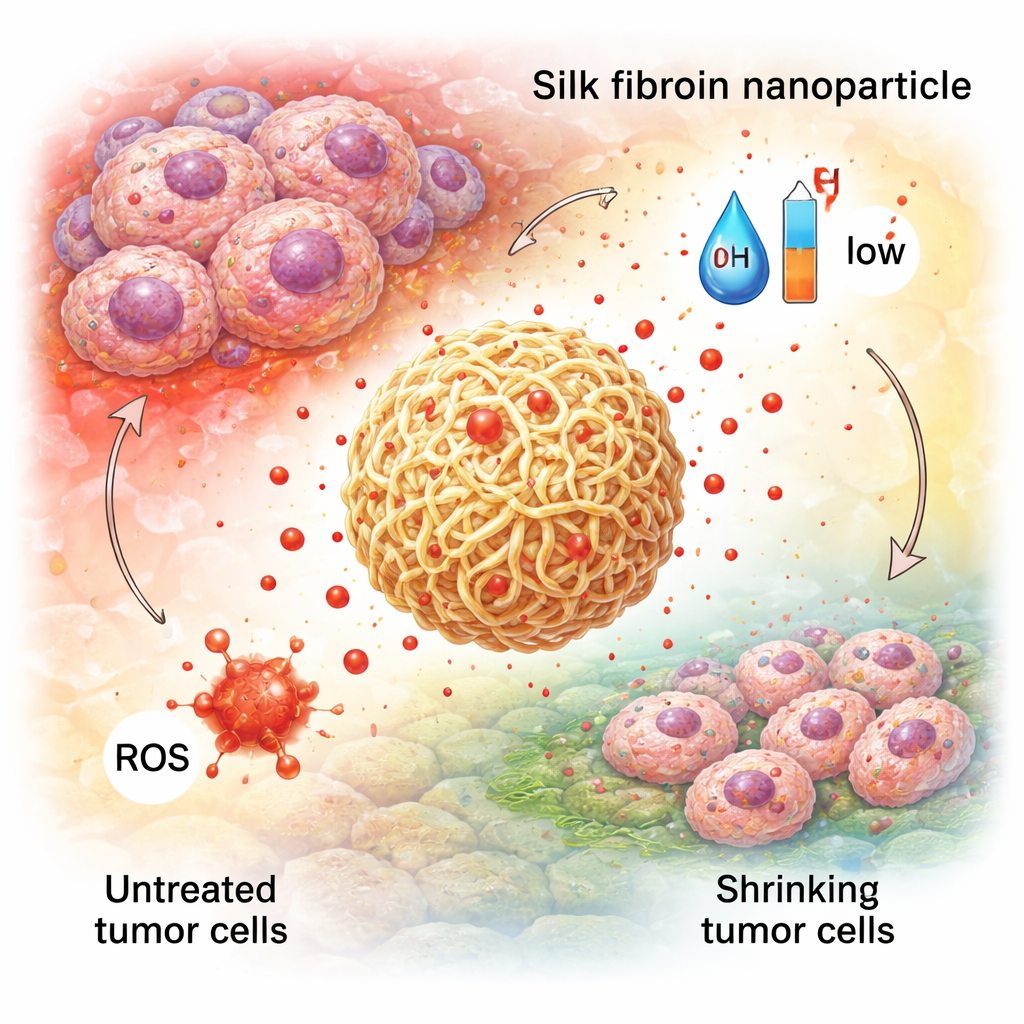
نجاحات مبكرة في السرطان وأمراض الأمعاء وإصلاح الجروح
اختُبرت هذه الجسيمات المصممة في نماذج مرضية متنوعة. في السرطان، حملت جسيمات الحرير أدوية كيماوية وحتى مجموعات من الأدوية إلى جانب عوامل نشطة بالضوء، مظهرة تراكمًا أفضل في الأورام وإطلاقًا أكثر دقة في بيئة الورم القاسية وتأثيرات جانبية أقل مقارنةً بالأدوية الحُرّة. في أمراض الأمعاء الالتهابية، يمكن للجسيمات الحريرية التي تُؤخذ عن طريق الفم والمحمّلة بمضادات أكسدة طبيعية أو مركبات مضادة للالتهاب أن تلتصق بمخاط الأمعاء، وتتنقل خلاله، وتطلق حمولتها استجابةً لمستويات مرتفعة من الجزيئات التفاعلية، مما يساعد على تهدئة الالتهاب وإصلاح حاجز الأمعاء. في هندسة الأنسجة وشفاء الجروح، يُخلط الجسيمات مع الهياكل الداعمة والهلاميات المائية لإطلاق عوامل نمو أو مضادات حيوية ببطء، مما يقوّي المواد الشبيهة بالعظم ويسرع إغلاق الجروح وشفاء الجلد بشكل نظيف.
سد الفجوة من منصة المختبر إلى سرير المستشفى
على الرغم من الوعد، تظل جسيمات فيبروين الحرير في المرحلة قبل السريرية. تبرز المراجعة عقبات رئيسية: اختلافات بين الدفعات الناتجة عن طرق معالجة الحرير، وبقايا بروتينات أو مذيبات قد تؤثر على الأمان، وصعوبة إنتاج كميات كبيرة وفق قواعد جودة صيدلانية صارمة. يوفر التصنيع بالميكروفلويد تحكمًا أفضل لكنه حاليًا مكلف ومعقّد للتوسع. كما سيطلب المنظمون فهماً واضحاً لكيفية تحلل هذه الجسيمات في الجسم، وكيفية إزالتها، ومدى إمكانية تصنيعها بشكل موثوق. يرى المؤلفون أن طرق معالجة أكثر صداقة للبيئة، وبروتوكولات موحدة، ومراقبة مستمرة لجودة الجسيمات، وتعاونًا وثيقًا بين المختبرات الأكاديمية والصناعة يمكن أن ينقل تدريجيًا جسيمات الحرير من عروض مختبرية أنيقة إلى أدوات طبية يومية.
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، تهدف جسيمات فيبروين الحرير إلى إيصال مزيد من الدواء حيث يُحتاج وقليل منه حيث لا يُحتاج. باستخدام بروتين متوافق حيويًا وقابل للتحلل يمكن تشكيله وضبطه على مستويات متعددة، يأمل العلماء في تقليل الآثار الجانبية القاسية للعلاج الكيميائي، وتوفير علاج طويل الأمد أكثر فعالية لالتهابات الأمعاء، وتسريع إصلاح الأنسجة بعد الإصابة. وبينما لا تزال العديد من التحديات الهندسية والتنظيمية قائمة، تشير الأعمال الملخّصة في هذه المقالة إلى أن حوامل الأدوية «الذكية» غدًا قد تُنسَج ليس من مركبات اصطناعية غريبة بل من نفس الحرير الذي لبسَه البشر لآلاف السنين.
الاستشهاد: Bao, S., Yang, X., Reis, R.L. et al. Synthesis and application of silk fibroin nanoparticles for drug delivery. Commun Mater 7, 66 (2026). https://doi.org/10.1038/s43246-026-01108-x
الكلمات المفتاحية: جسيمات نانوية من فيبروين الحرير, توصيل دوائي مستهدف, النانوطب في علاج السرطان, داء الأمعاء الالتهابي, هندسة الأنسجة