Clear Sky Science · ar
أكسيسابتاجين سيلوليوسيل بالاشتراك مع ريتوكسيماب لليمفوما كبيرة الخلايا البائية المقاومة: تجربة ZUMA-14 الطور 2 أحادي الذراع
لماذا يهم هذا العلاج الجديد لليمفوما
بالنسبة للأشخاص المصابين بسرطان دم عدواني يسمى الليمفوما كبيرة الخلايا البائية، لا تعمل الكيميائيّات القياسية دائمًا، وحتى العلاجات الخلوية القوية قد تفقد فعاليتها مع الوقت. اختبرت هذه الدراسة استراتيجية جديدة: دمج علاج مناعي خلوي مخصص مع دواء مضاد أجسام استخدم طويلاً لمعرفة ما إذا كان مهاجمة السرطان من واجهتين يمكن أن يمنع عودته ويحدث ذلك دون إضافة آثار جانبية غير آمنة.
دواءان يتعاونان ضد سرطان واحد
ركزت التجربة على البالغين الذين لم تستجب لمعارضهم السابقة من العلاجات، وهي مجموعة تواجه عادة نتائج سيئة. تلقى جميع المشاركين أكسيسابتاجين سيلوليوسيل، أو أكسي‑سيل، وهو نوع من علاج خلايا CAR T المعدّ من خلايا T الخاصة بالمريض والمصمَّمة لمطاردة الخلايا الحاملة لعلامة تسمى CD19. بالإضافة إلى ذلك، أعطي لهم ريتوكسيماب، وهو دواء مضاد أجسام يربط علامة مختلفة على نفس خلايا السرطان تُدعى CD20. الفكرة كانت بسيطة لكنها قوية: بضرب هدفين على خلايا الليمفوما في آن واحد، سيصعب على السرطان "الفرار" عن طريق فقدان إحدى هذه العلامات.
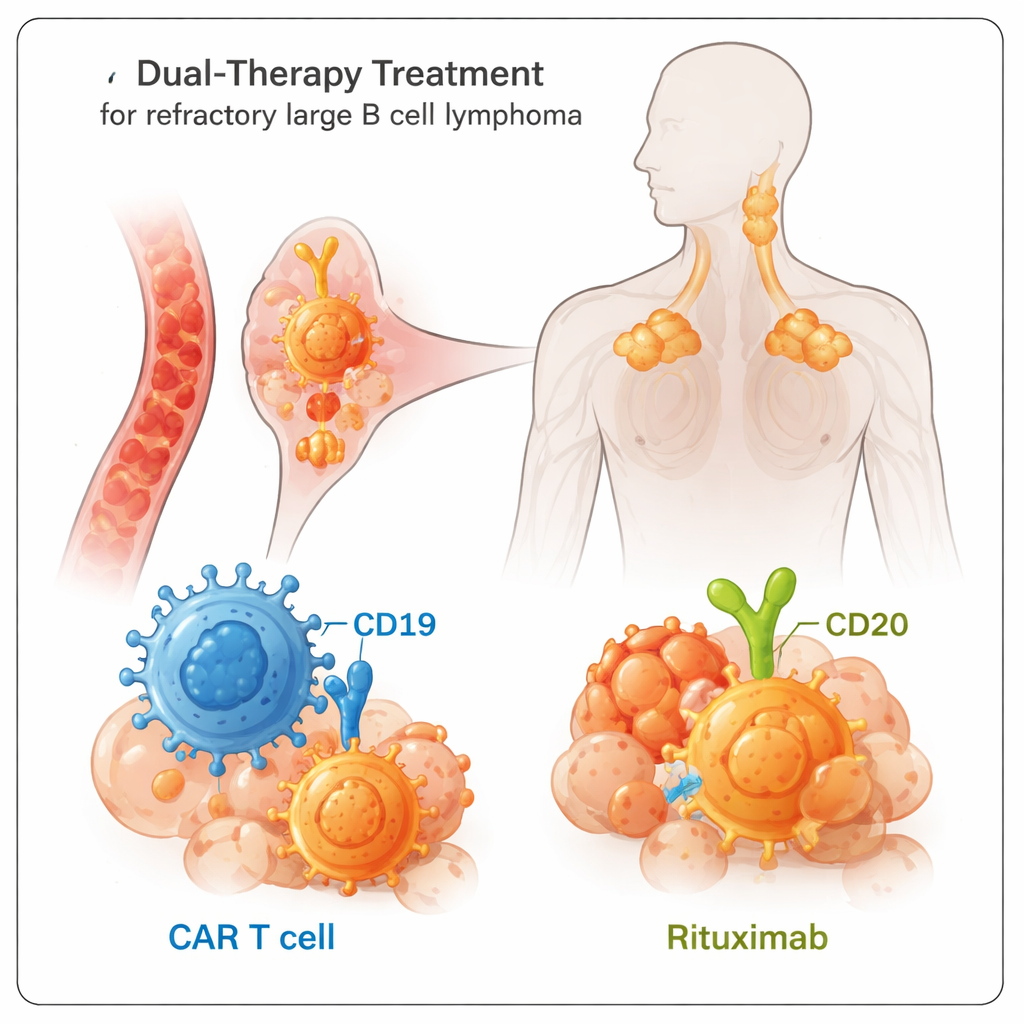
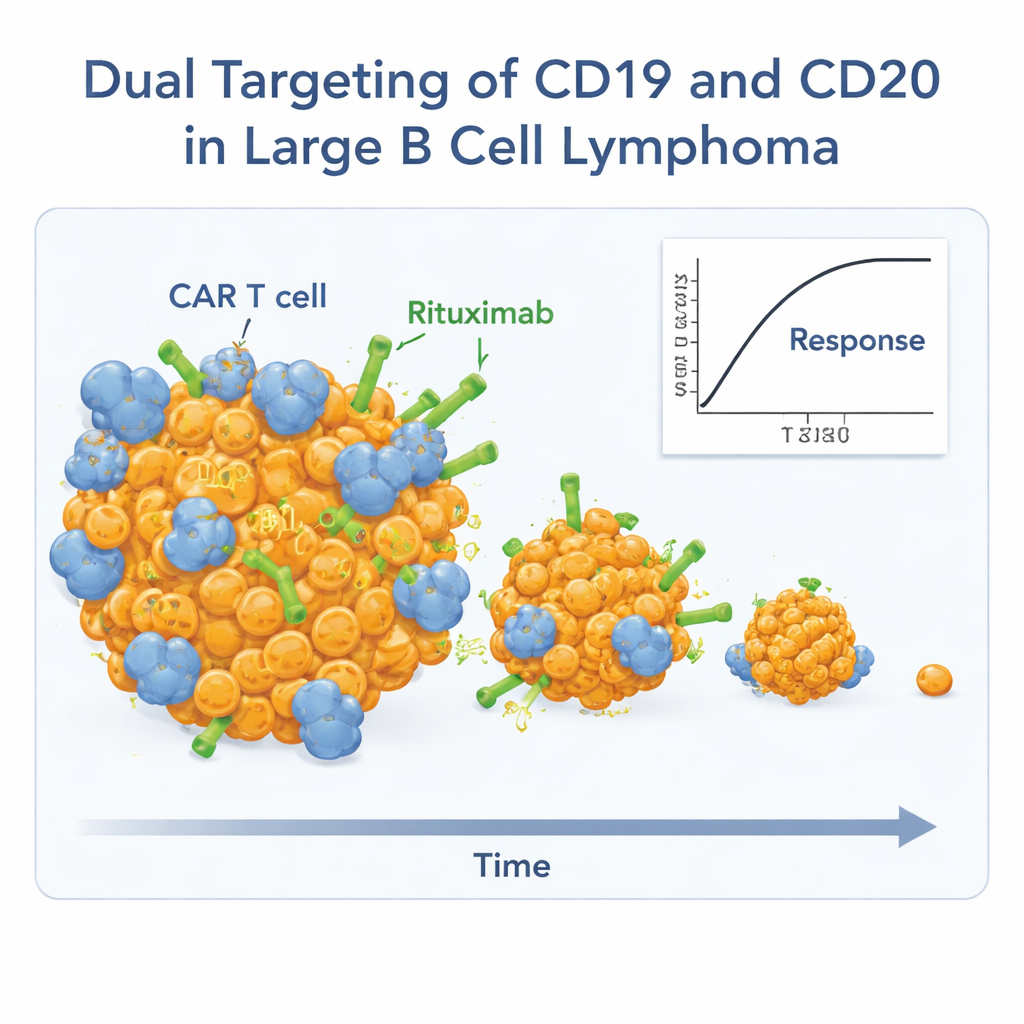
استجابات أقوى وأطول أمداً
من بين 26 شخصًا تلقوا العلاجين معًا، شهد تقريبًا 9 من كل 10 تقلصاً في أورامهم، وحصل ما يقرب من ثلاثة أرباعهم على غياب مؤشرات السرطان في الصور المقطعية، وهو ما يُعرف بالاستجابة الكاملة. لم تكن كثير من هذه الاستجابات العميقة مجرد نجاحات عابرة. بعد متابعة استمرت قليلاً لأكثر من عامين، ظل ما يقرب من نصف المشاركين لديهم استجابات مستمرة. كان الوسيط لمدة الاستجابة نحو 26 شهرًا، والوقت الوسيط للبقاء دون تدهور المرض حوالي عامين. لم يُسجل وقت البقاء الكلي عند تحليل البيانات، ما يعني أن أكثر من نصف المرضى ما زالوا على قيد الحياة.
الآثار الجانبية تبقى خطيرة لكنها قابلة للإدارة
نظراً لأن علاجات CAR T تنشط الجهاز المناعي، فقد تسبب آثارًا جانبية شديدة، خاصة تفاعلاً يُسمى متلازمة إطلاق السيتوكينات وأعراضًا عصبية مؤقتة. في هذه الدراسة، عانى تقريبًا الجميع من بعض درجات التفاعل المناعي، لكن المهم أنّه لم يُصَب أحد بأشد درجات متلازمة إطلاق السيتوكينات، ووقعت مشاكل عصبية خطيرة لدى نحو 15% من المرضى؛ وقد تعافت كل هذه الحوادث في نهاية المطاف. كانت حالات انخفاض تعداد الدم والالتهابات شائعة كما هو متوقع، لكن إضافة ريتوكسيماب لم تبدُ أنها زادت هذه المضاعفات بوضوح مقارنة بدراسات سابقة على أكسي‑سيل بمفرده. طوّر مريضان سرطان دم ثانٍ، وهي مخاطرة نادرة لكنها معروفة طويلة الأمد مع العلاجات المناعية القوية.
دلالات حول من يستفيد أكثر
استقصى الباحثون أيضًا البيولوجيا الكامنة وراء نجاح أو فشل هذا المزيج. كان الأشخاص الذين أظهرت دماؤهم مستويات أعلى من خلايا CAR T والتعرض لريتوكسيماب هم من يميلون إلى تحقيق أقوى الاستجابات وأكثرها دوامًا. قليلون جدًا من المرضى كان لديهم خلايا B طبيعية — النوع الذي يتحول إلى خلايا سرطانية في هذا المرض — طوال سنة كاملة بعد العلاج، ما يبيّن أن العلاج ظل نشطًا. أشارت عينات الورم المأخوذة قبل العلاج إلى أن السرطانات الغنية بالفعل بأنواع معينة من الخلايا المناعية، مثل الخلايا القاتلة الطبيعية وخلايا T من النوع الذاكِرة، كانت أكثر احتمالًا للبقاء في سكون طويل الأمد. كما دلّت فحوصات الدم لقطع الحمض النووي الورمي على أن الكشف المبكر عن حتى كميات صغيرة من المرض الباقي قد يتنبأ بالانتكاس لاحقًا.
ماذا يعني هذا للمستقبل
بالنسبة للمرضى الذين قاومت ليمفوماتهم عديد جولات العلاج، قدم مزيج أكسي‑سيل وريتوكسيماب معدلات استجابة عالية والعديد من حالات السكون الطويلة الأمد دون طرح مشكلات أمان غير متوقعة. ومع أن التجربة كانت صغيرة ولا تحتوي على ذراع مقارنة مباشرة، فإن نتائجها تدعم فكرة أن ضرب خلايا السرطان عبر كل من CD19 وCD20 قد يساعد في منع الورم من التهرب من علاج يستهدف هدفًا واحدًا. إن نهج الاستهداف المزدوج هذا يلهم الآن أجيالًا تالية من العلاجات الخلوية المصممة لبناء هجوم ذو شوكتيْن مماثلتين مباشرة في منتج واحد، على أمل جعل العلاجات القوية والدائمة أكثر سهولة وتوفراً على نطاق أوسع.
الاستشهاد: Strati, P., Leslie, L., Shiraz, P. et al. Axicabtagene ciloleucel in combination with rituximab for refractory large B cell lymphoma: the phase 2, single-arm ZUMA-14 trial. Nat Cancer 7, 304–315 (2026). https://doi.org/10.1038/s43018-025-01102-1
الكلمات المفتاحية: علاج خلايا CAR T, ليمفوما كبيرة الخلايا البائية, ريتوكسيماب, استهداف مضادين للمستضد, مقاومة العلاج المناعي