Clear Sky Science · ar
تشكُّل غليوما منتصف المحور الجديدة الناتجة عن H3.3K27M في عضويات جذعية دماغية بشرية لفحص وظيفة خلايا CAR T المستهدفة GD2
لماذا تهم هذه الدراسة عن سرطان دماغ الأطفال
غليوما منتصف المحور المنتشرة هي من أخطر سرطانات دماغ الأطفال، وتصيبه في الأطفال الصغار جداً في جذع الدماغ، مما يترك العائلات مع خيارات علاجية فعالة قليلة أو معدومة. وبما أن الأورام تقع عميقاً في الدماغ ونادراً ما تُستأصل جراحياً، فليس لدى الباحثين الكثير من الأنسجة للدراسة وقليل من السبل لاختبار علاجات جديدة بأمان. تبني هذه الدراسة "جذع دماغ مصغّر في طبق" واقعي وتستخدمه لمراقبة كيفية تصرُّف علاج مناعي واعد — خلايا CAR T المستهدفة GD2 — على مدى أسابيع، بما في ذلك لماذا تفشل أحياناً.
بناء جذع دماغ مصغّر في المختبر
بدأ الفريق بخلايا جذعية بشرية ووجّهها خطوة بخطوة لتنمو إلى عضويات دماغية ثلاثية الأبعاد تشبه منطقة جذع الدماغ المسماة البونس، حيث تنشأ هذه الأورام عادة. من خلال توقيت إشارات النمو بعناية، أنتجوا عضويات غنية بأنواع الخلايا الداعمة نفسها، أو الخلايا الدبقية، التي تعيش عادة في هذه المنطقة. أظهرت تحليلات جينية مفصَّلة أن أنواع الخلايا ونضجها اتبعت أنماطاً تُرى في تطور الدماغ البشري المبكر، لا سيما سلالات الخلايا الدبقية المميزة للبونس والنخاع المجاور. وهذا يعني أن العضويات يمكن أن تشكّل خلفية واقعية لدراسة كيفية بدء هذا السرطان ونموه.
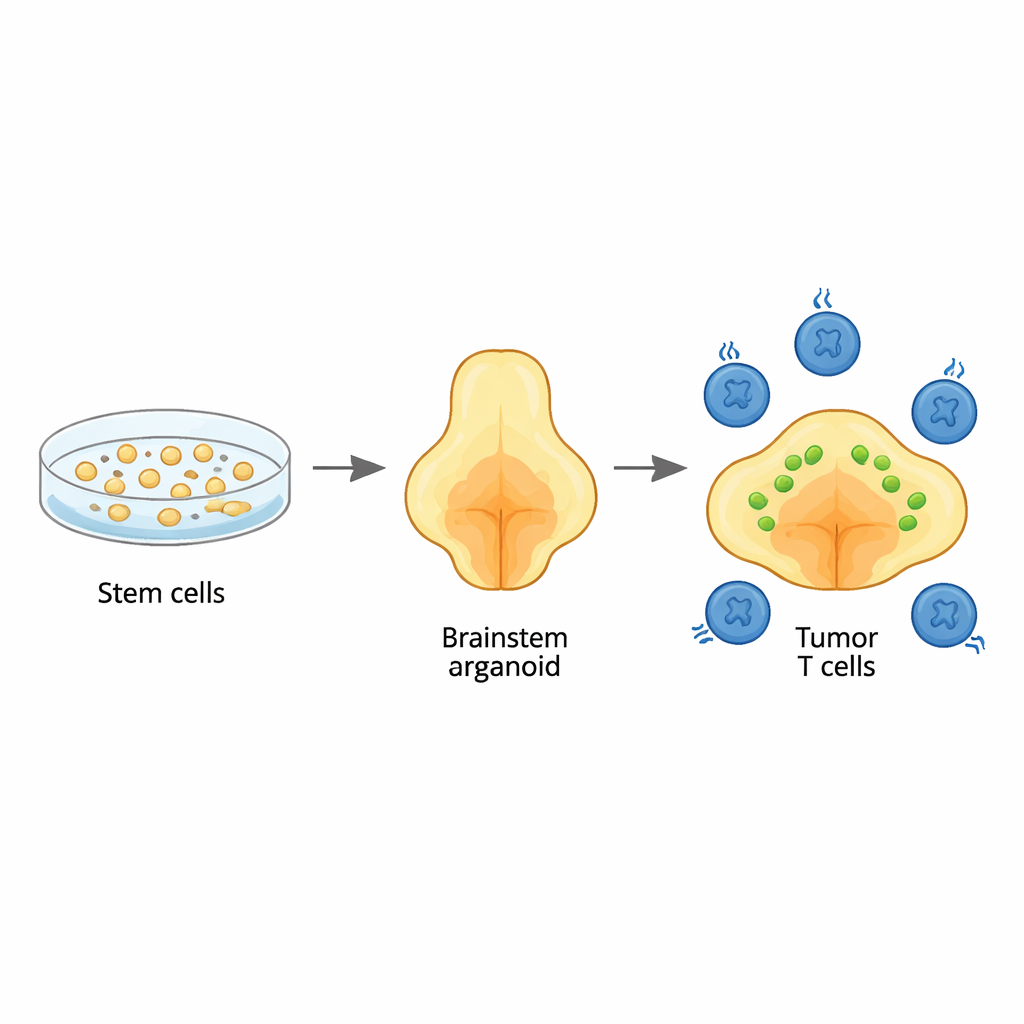
إعادة خلق ورم الطفل داخل العضوية
لتقليد غليوما منتصف المحور المنتشرة، أدخل الباحثون ثلاث تغييرات جينية رئيسية في العضويات الشابة: طفرة مميزة في بروتين الهيستون (H3.3K27M)، وفقدان مثبّط الورم TP53، وتغيير منشط في مستقبل النمو PDGFRA. عندما أدخِلت هذه التغيرات في مرحلة تطورية مبكرة جداً، تحولت خلايا دبقية محددة إلى خلايا سرطانية. انتشرت الأورام الناتجة بشكل منتشِر داخل العضويات، تماماً كما في جذوع أدمغة الأطفال، وحملت نفس التواقيع الواسعة للحمض النووي DNA والحمض النووي الريبي RNA التي تُرى في أورام المرضى. كشف التسلسل خلية واحدة عن خليط من حالات الخلايا السرطانية، بما في ذلك خلايا دبقية غير ناضجة ومحددة للبونس تطابق تلك الموجودة في أورام الأطفال الفعلية، مما يؤكد أن النموذج يعيد تمثيل المرض البشري بدقة.
مراقبة علاجات مناعية تقاتل — وتنهك — عبر الزمن
مع وجود نموذج الورم داخل جذع الدماغ، أضاف الفريق خلايا CAR T المستهدفة GD2 — وهي خلايا T من المرضى مُهندَسة للتعرف على جزيء يسمى GD2 على خلايا الورم — وتابع كل من حجم الورم وسلوك خلايا T لمدة تصل إلى شهر. أظهرت بعض العضويات تقلصاً قوياً للأورام، وأخرى سيطرة جزئية فقط، مما يعكس النتائج المتباينة الملاحظة في التجارب السريرية. كشف تسلسل RNA خلية واحدة لأكثر من 20,000 خلية CAR T المتعرضة للأورام عن تنوّع مفاجئ في حالات خلايا T. كانت بعض الخلايا قاتلة بشدة "منفّذة المهمة"، وكان بعضها منشطاً لكن غير قاتل تماماً، وعرضت مجموعة مميزة علامات الإرهاق، بتهدُّؤ في جينات قتل السرطان وارتفاع في تعبير "المكابح" المثبِّطة. تشابهت الخلايا المُنهَكة مع خلايا T المستهلكة التي تُرى في العدوى المزمنة والأورام البشرية، مما يشير إلى أن نظام العضويات يلتقط تعب خلايا T ذي صلة سريرياً نتيجة الاتصال المستمر مع السرطان.
اكتشاف خلايا T قوية لكنها قصيرة العمر
بالتعمق أكثر، حدّد الباحثون مجموعة فرعية من خلايا CAR T تميّزها بروتين سطحي يسمى NCAM1 وكانت قاتلة خاصة على المدى القصير. عندما عزلت هذه الخلايا الإيجابية لـ NCAM1 واستخدمت وحدها، سيطرت على الأورام بقوة أكبر في البداية مقارنة بنظيراتها السالبة لـ NCAM1. ومع ذلك، أصبحت أيضاً منهكة وتراجعت بسرعة أكبر، مما أدى إلى سيطرة أضعف مع مرور الوقت. هذا المقايضة بين القوة الفورية والثبات تساعد في تفسير لماذا يمكن لعلاجات CAR T أن تُنتج استجابات درامية لكنها مؤقتة، وتقترح أن الفرز المسبق أو إعادة تشكيل مجموعات خلايا T قد يحسّن ديمومة العلاج.
كيف يمكن لخلايا المناعة الدماغية أن تُضعف العلاج
في الدماغ الحقيقي، تحيط بالأورام ليس فقط الخلايا العصبية والخلايا الدبقية بل أيضاً الميكروغليا، وهي خلايا المناعة المقيمة في الدماغ. لالتقاط هذا المستوى من التعقيد، أضاف العلماء ميكروغليا مشتقة من الخلايا الجذعية إلى عضوياتهم. نضجت هذه الخلايا، واتخذت أشكالاً وأنماط تعبير جيني خاصة بالميكروغليا الموجودة في غليوما منتصف المحور المنتشرة، وأنتجت جزيئات مرتبطة ببيئة مثبطة للمناعة. عندما أُضيفت خلايا CAR T إلى عضويات حاملة للأورام تحتوي على ميكروغليا، اتجهت خلايا T أكثر نحو حالات منهكة ومنخفضة الفعالية، وساءت السيطرة على الورم. وفي الوقت نفسه، ارتفعت عوامل التهابية مرتبطة بآثار جانبية للعلاج، مثل IL-6، مما يشير إلى أن النموذج يمكنه أيضاً المساعدة في دراسة سمّيات علاجات CAR T.
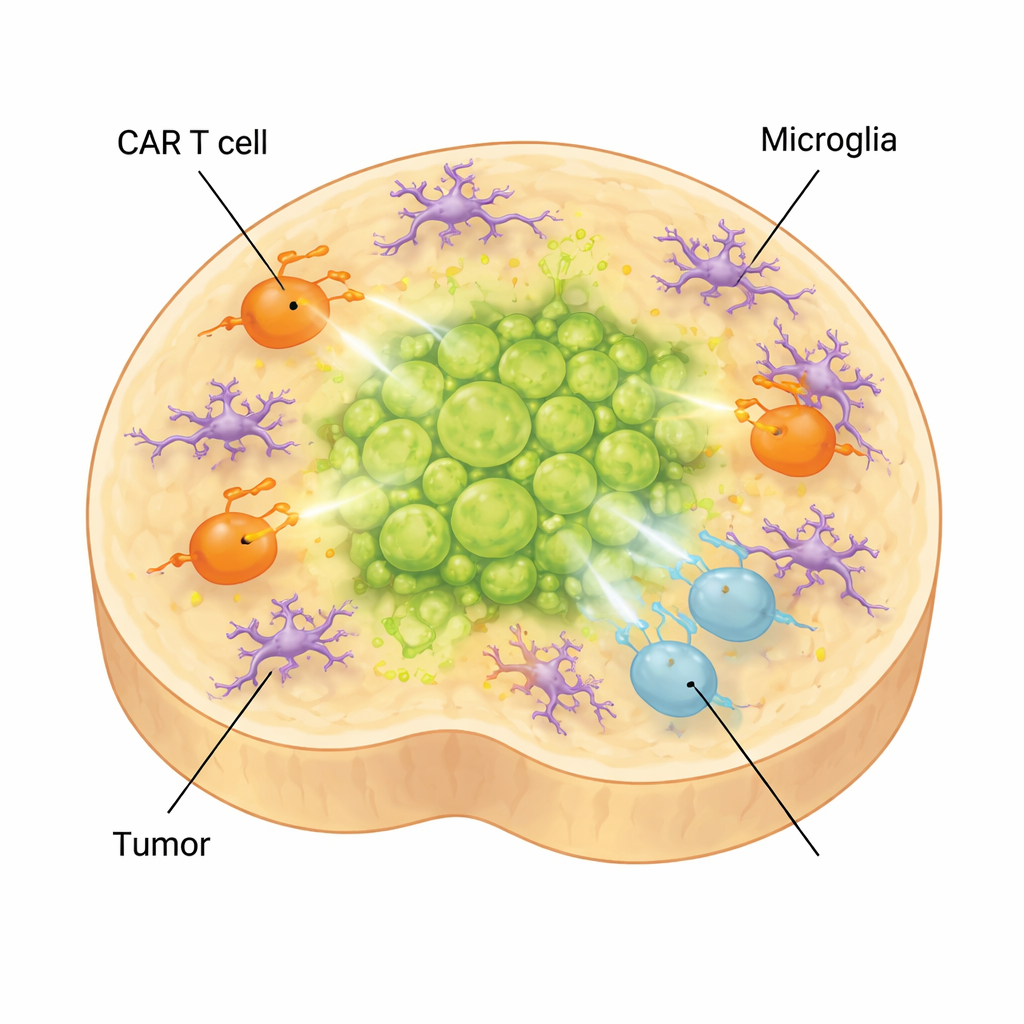
ما معنى هذا للأطفال المصابين بهذا السرطان
بالنسبة للعائلات التي تواجه غليوما منتصف المحور المنتشرة، لا يقدم هذا العمل علاجا جديدا بعد، لكنه يوفر ميدان اختبار قوي للوصول إلى ذلك بسرعة أكبر. من خلال إعادة خلق بيئة جذع دماغ الطفل والورم في طبق، يمكن للعلماء الآن ملاحظة في الوقت الحقيقي كيف تتفاعل خلايا الورم المختلفة وأنواع خلايا CAR T والميكروغليا عبر أسابيع. يتيح لهم ذلك تحديد أيّ خلايا T المهندسة هي الأكثر فعالية، كيف ومتى تصاب بالإرهاق، وكيف تقوّض خلايا المناعة المقيمة في الدماغ جهودها. في النهاية، قد تُخصَّص مثل هذه النماذج العضوية للمرضى الأفراد وتُستخدم لضبط العلاجات المناعية قبل إعطائها، مما يحسن فرص أن تكون علاجات CAR T المستقبلية أكثر أماناً وفعالية للأطفال.
الاستشهاد: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
الكلمات المفتاحية: غليوما منتصف المحور المنتشرة, عضويات دماغية, خلايا CAR T, سرطان دماغي أطفال, الميكروغليا