Clear Sky Science · ar
الانتشار الشرطي مع محاذاة نمطية واعية بالمحلية لتوليد مجموعات حالية بروتينية متنوعة
لماذا تهم حركة البروتينات
البروتينات داخل خلايانا ليست تماثيل جامدة؛ بل تتصرف مثل آلات صغيرة ومرنة تتغير أشكالها باستمرار. يمكن لتلك التغيرات في الشكل التحكم في كيفية قيام الإنزيمات بتحفيز التفاعلات، وكيف تستجيب المستقبلات للأدوية، وكيف تنتقل الإشارات داخل الخلايا. ومع ذلك، تُظهر معظم الصور المألوفة للبروتينات «لقطة» واحدة فقط، فتغفل عن المجموعة الغنية من الأشكال التي توجد بالفعل. تقدم هذه الورقة طريقة تُسمى Mac-Diff، وهي تقنية ذكاء اصطناعي قادرة على توليد العديد من الأشكال الواقعية لبروتين معين بسرعة، مما يساعد العلماء على رؤية ليس فقط كيف يبدو البروتين، بل كيف «يتنفس» ويتحرك.
من لقطات مفردة إلى مجموعات متحركة
على مدار عقود، اعتمد الباحثون على تجارب مرهقة أو محاكيات ديناميكا جزيئية طويلة لاستكشاف حركة البروتينات، وكلتاهما قد تكون بطيئة ومكلفة. أدوات ثورية مثل AlphaFold2 تتنبأ الآن بالبنية ثلاثية الأبعاد الأكثر احتمالاً للبروتين من تسلسل الأحماض الأمينية مباشرة، لكنها عادةً ما تُرجع شكلاً واحداً أو القليل من الأشكال المفضلة. العديد من البروتينات، وخصوصاً تلك المشاركة في الإشارات والتنظيم الاللوستيري، تحتل طبيعياً حالات متعددة وغير محددة بدقة. يجادل المؤلفون بأنه لفهم كيفية عمل هذه البروتينات فعلاً — ولتصميم أدوية ترتبط بأشكال عابرة وغير بديهية — نحتاج إلى طريقة لتوليد مجموعات كاملة من الت conformations المعقولة، وليس مجرد تخمين أفضل واحد.
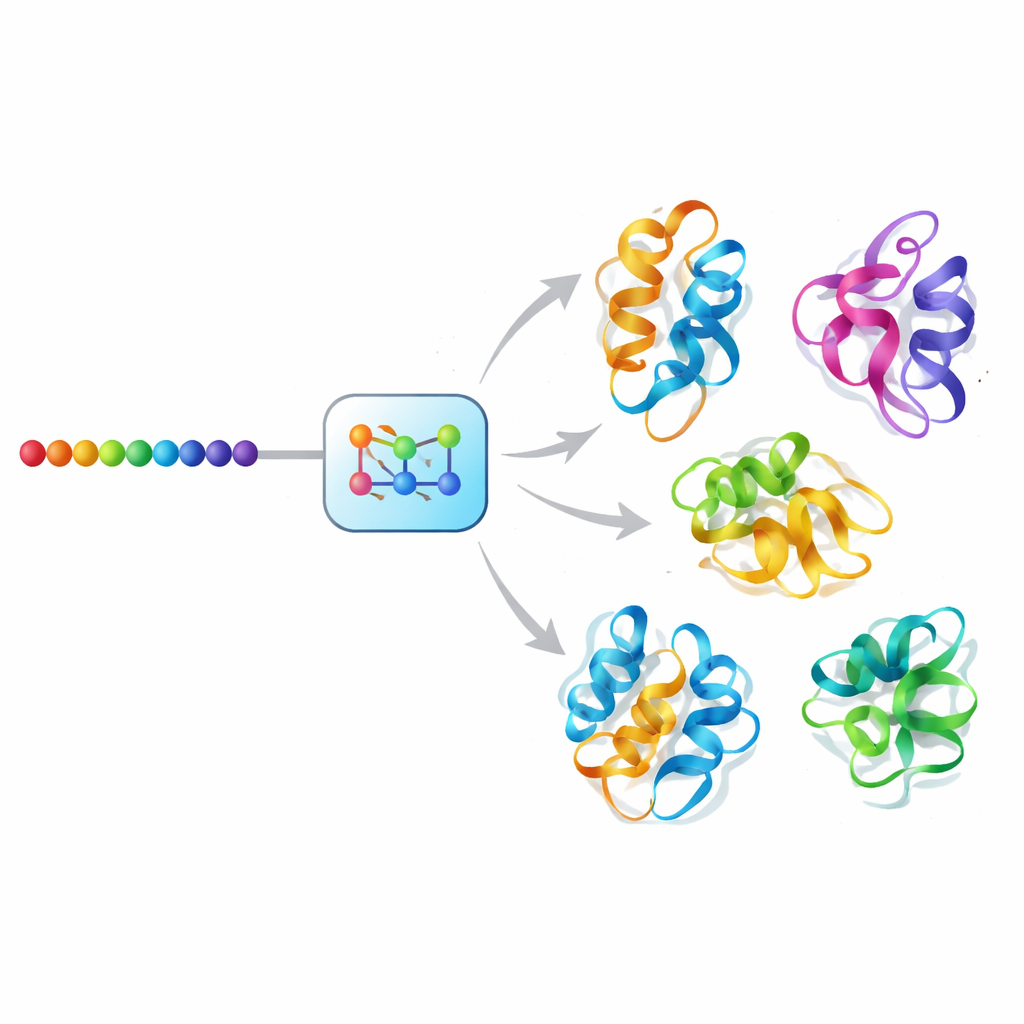
نهج «الانتشار» بالذكاء الاصطناعي لحركة البروتين
تتعامل Mac-Diff مع هذا التحدي باستخدام نموذج مولد على غرار الانتشار، فئة من الذكاء الاصطناعي التي دفعت طفرة حديثة في توليد الصور. بدلاً من إزالة الضوضاء من الصور الفوتوغرافية، تزيل Mac-Diff الضوضاء من أوصاف هندسية مجردة لهيكل العمود الفقري للبروتين. يمثل النموذج البروتين كشبكة من العلاقات الزوجية بين بقاياه — مسافات وزوايا غير حساسة لكيفية تدوير الجزيء أو نقله. في خطوة أمامية، يضيف النظام تدريجياً ضوضاء إلى هذه الأنماط الهندسية حتى تشبه تشويشاً عشوائياً. في الخطوة العكسية، يتعلم إزالة الضوضاء خطوة بخطوة، موجهًا بتسلسل الأحماض الأمينية للبروتين، حتى تعود هندسيات متوافقة ثلاثية الأبعاد بشكل متماسك، والتي يمكن بعد ذلك تحويلها إلى نماذج ذرية كاملة بواسطة برامج بناء البنية القياسية.
السماح للتسلسل بالتحدث إلى البنية محليًا
تكمن ابتكار رئيسي في كيفية ربط Mac-Diff لتسلسل خطي من البقايا بجيرانها ثلاثيي الأبعاد. السماح ببساطة لكل بقاية بالانتباه لكل بقاية أخرى، كما في نماذج تحويل النص إلى صورة، من شأنه أن يطمس قيودًا فيزيائية مهمة. بدلاً من ذلك، يقدم المؤلفون آلية انتباه «واعية بالمحلية» تركز كل بقاية على حيّ صغير محتمل من شركاء التفاعل. لتقدير هذه الأحياء، تستخدم Mac-Diff ثلاثة مكونات: نموذج لغة بروتينية يُسمى ESM-2 يشفر السياق الكيميائي الحيوي لكل بقاية؛ وخريطة تماس تشير إلى أزواج البقايا التي من المحتمل أن تكون قريبة من بعضها؛ وقاعدة بسيطة تُفضّل البقايا القريبة على طول السلسلة. تُجمع هذه الإشارات بحيث، أثناء عملية إزالة الضوضاء، يفضّل النموذج استخدام معلومات من البقايا التي تعد شركاءً فيزيائياً معقولين، مما يحسّن قدرته على إعادة بناء هياكل مرنة وواقعية.
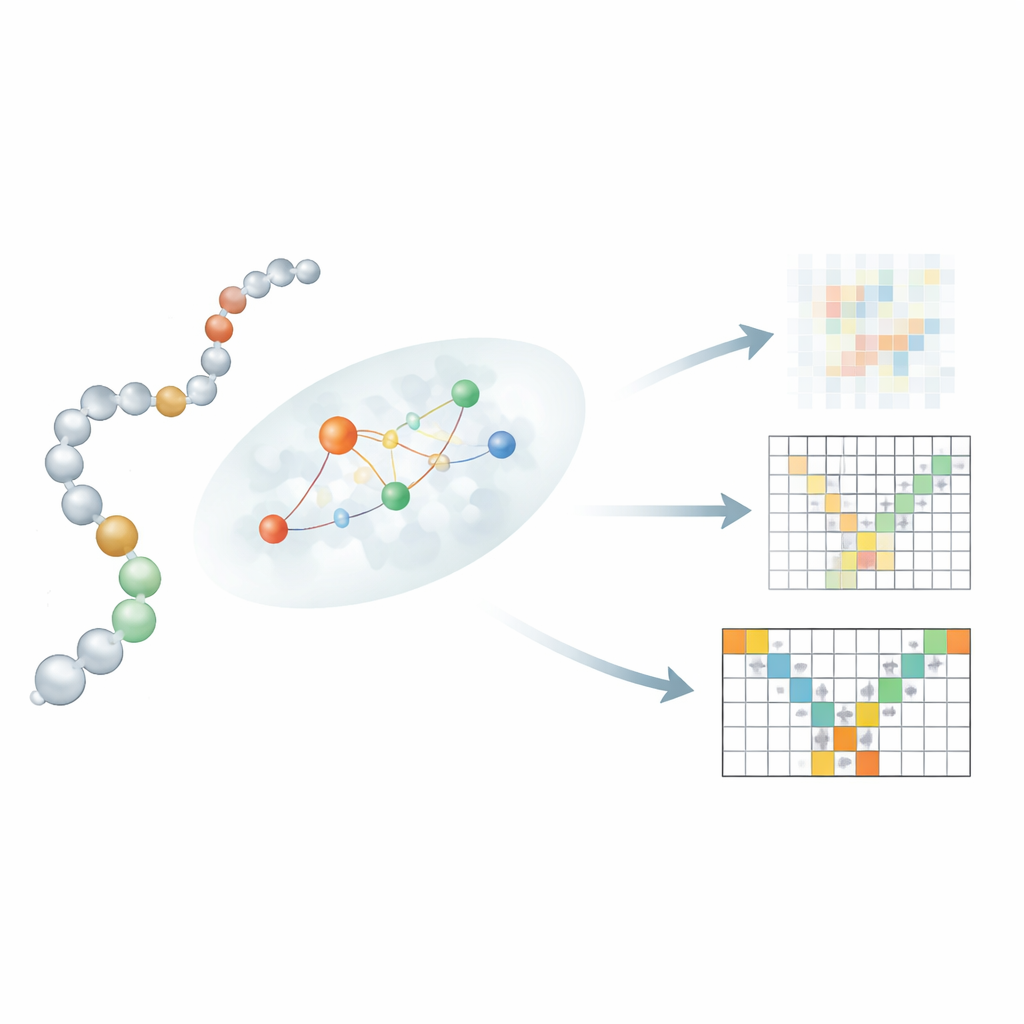
الاختبار مقابل المحاكيات الطويلة والبروتينات متغيرة الشكل
اختبر الباحثون Mac-Diff على جبهتين متطلبتين. أولاً، تساءلوا عمّا إذا كان يستطيع إعادة إنتاج التوزيع الواسع للأشكال المرصودة في محاكيات ديناميكا جزيئية طويلة ومحسوبة بعناية لبروتينات سريعة الطي وبروتين معياري كلاسيكي يعرف باسم BPTI. عبر عدة مقاييس تقارن الخصائص الإحصائية للمجموعات المولدة ببيانات المحاكاة — مثل توزيعات المسافات داخل البروتين ومدى الانضغاط العام — طابق Mac-Diff أو تفوق على طرق ذكاء اصطناعي منافسة، مع توليد مجموعة أوسع من الت conformations. أمسك بمعظم الحالات «شبه المستقرة» الرئيسية المحددة في المحاكيات وأعاد إنتاج أنماط مرونة على مستوى البقايا بترابط عالٍ، مما يشير إلى أن مجموعاته تعكس كلّاً من الطيات العامة والرجفات المحلية بطريقة واقعية.
كشف الحالات الوظائفية المخفية
ثانياً، تحدى الفريق Mac-Diff ببروتينات معروفة بتبني أشكال مختلفة جداً أثناء أداء وظائفها، بما في ذلك الإنزيم أدينيلات كيناز، الذي يتبدل بين أشكال مفتوحة ومغلقة أثناء أيض الطاقة، ومجموعة مختارة من 40 بروتينًا لها حالتان متباينتان محددتان تجريبياً لكل منها. ولّد Mac-Diff فقط 100 بنية مرشحة لكل بروتين — أقل بكثير من مسارات المحاكاة النموذجية — ومع ذلك استعاد معظم الحالات المعروفة باتفاق هندسي جيد. في أدينيلات كيناز، على سبيل المثال، أنتج كلّاً من الت conformations المفتوحة والمغلقة بتشابه عالٍ مع هياكل البلورات، في حين أن عدة طرق شائعة كانت تميل إلى تفضيل حالة واحدة فقط. كما عمل النموذج أسرع بنحو ألف مرة من المحاكيات التقليدية على أجهزة مماثلة، مما يجعل الاستكشاف النظامي لتنوع الأشكال عملياً أكثر بكثير.
ماذا يعني هذا للبيولوجيا والطب
بعبارات يومية، يحول Mac-Diff تسلسل البروتين إلى معرض من الوضعيات المحتملة بدلًا من صورة مفردة، ويفعل ذلك مع فهم أي الأجزاء من المرجح أن تدفع أو تتشابك مع بعضها في الفراغ ثلاثي الأبعاد. من خلال أخذ عينات دقيقة وفعالة من هذه المجموعات، يوفر الأسلوب وسيلة لاستكشاف كيف تقوم التغيرات الطفيفة في الشكل بتحديد الوظيفة، لاكتشاف الحالات النادرة لكنها مهمة، وللبحث عن جيوب ارتباط للأدوية التي تظهر فقط في حالات عابرة. وعلى الرغم من أنه لا يلتقط بعد الأفلام الزمنية المرتبة بالكامل التي توفرها المحاكيات، يجلب Mac-Diff المشهد الديناميكي للبروتينات ضمن متناول العديد من الأنظمة، مبشراً برؤى جديدة في البيولوجيا الهيكلية وتصميم الأدوية وهندسة البروتين.
الاستشهاد: Wang, B., Wang, C., Chen, J. et al. Conditional diffusion with locality-aware modal alignment for generating diverse protein conformational ensembles. Nat Mach Intell 8, 415–434 (2026). https://doi.org/10.1038/s42256-026-01198-9
الكلمات المفتاحية: ديناميكا البروتين, نماذج الانتشار, مجموعات الت conformations, البروتينات التحفيزية (الاللوستيرية), اكتشاف الأدوية