Clear Sky Science · ar
PFKM يتحكم في التحولات الأيضية طوال تمايز عضلات الهيكل العظمي
لماذا تحتاج خلايا العضلات إلى استخدام ذكي للسكر
عندما نمارس الرياضة أو ننهض ببساطة من الكرسي، تنطلق عضلاتنا الهيكلية للعمل، محرقة السكر لتغذية كل انقباض. لكن خلايا جذع العضلات الشابة والألياف العضلية المتكاملة لا تتعامل مع السكر بنفس الطريقة. تكشف هذه الدراسة عن نظام تبديل مدمج — يرتكز على إنزيم واحد يسمى PFKM — يقرر ما إذا كان الجلوكوز سيُحرق لإنتاج طاقة فورية أو يُعاد توجيهه لحماية وإصلاح الخلايا. فهم هذا المفتاح قد يفتح طرقًا جديدة لعلاج ضعف العضلات، وشيخوخة العضلات، والأمراض الأيضية الوراثية.
إشارة مرور لوقود الخلية
يمكن للجلوكوز الداخل إلى الخلية أن يسلك عدة مسارات. طريق رئيسي واحد، التحلل السكرّي (glycolysis)، يحول السكر بسرعة إلى طاقة ولبنات بناء للألياف العضلية النامية. مسار آخر، مسار فوسفات البنتوز، ينتج جزيئات تدافع عن الخلايا ضد الإجهاد التأكسدي وتدعم تخليق الحمض النووي والدهون. ركز الباحثون على PFKM، نسخة من إنزيم الفوسفوفركتوكيناز-1 التي تقع عند مفترق رئيسي في التحلل السكرّي. بقياس مئات المستقلبات خلال دقائق إلى ساعات بعد تنشيط إشارة نمو تسمى Wnt، وجدوا أن الخلايا تراكمت بسرعة في وسائط التحلل السكرّي المبكرة بينما انخفض منتج PFKM، وارتفعت مستقلبات مسار فوسفات البنتوز. هذا يوحي بأن الخلايا كانت تقوم بتقييد PFKM بنشاط لتحويل السكر نحو الكيمياء الوقائية بدلاً من إنتاج الطاقة الخالصة. 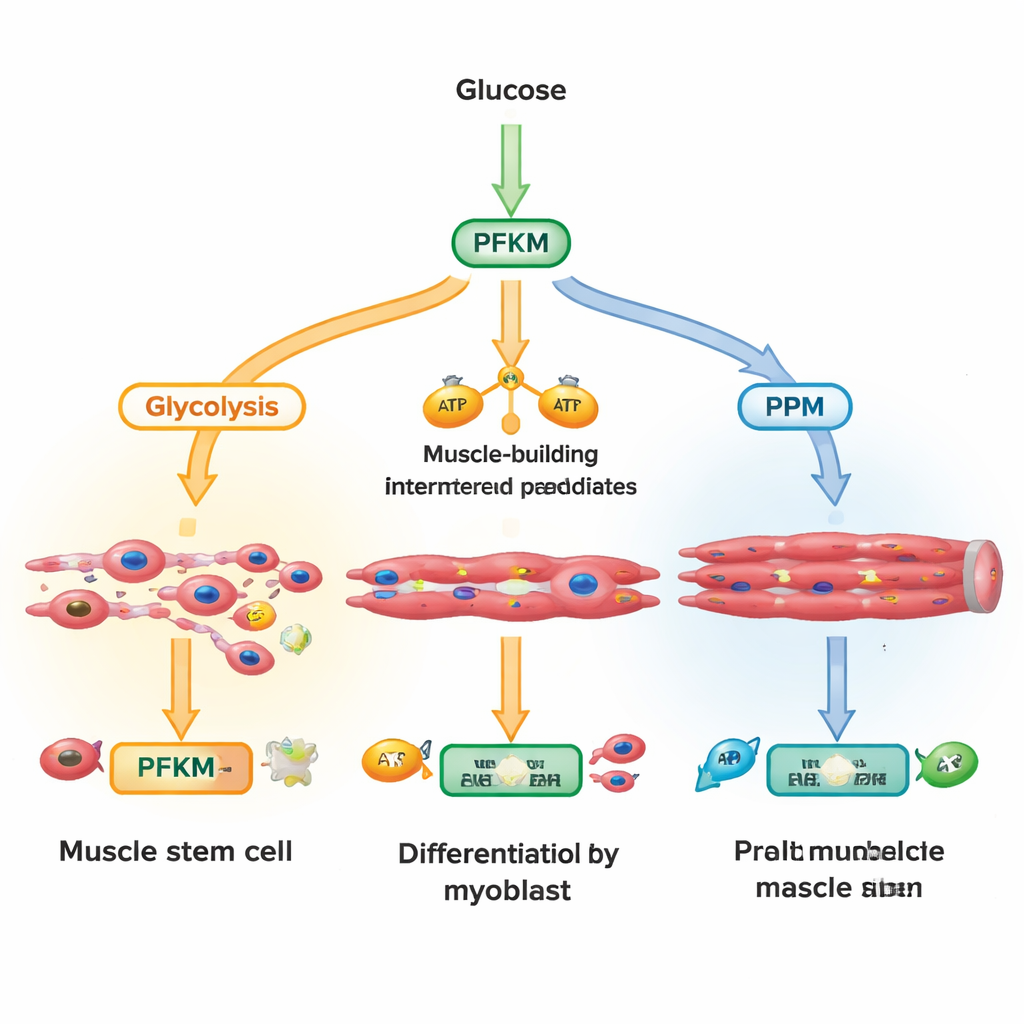
ووسم وإزالة إنزيم البوّاب
لمعرفة كيف يُتحكم في PFKM، تتبّع الفريق مكان وجود البروتين داخل الخلايا. في حالة الراحة، كان PFKM يسبح في السيتوبلازم. خلال دقائق من تحفيز Wnt، تجمّع في نقاط ساطعة تداخلت مع الليزوزومات، مقصورات تكسير البروتين في الخلية. إنزيمان شقيقان، PFKL وPFKP، لم يتحركا أو يتغيرت مستوياتهما، ما كشف أن نوع العضلات PFKM وحده هو المستهدف. أظهرت الاختبارات الكيميائية الحيوية أن حجب وظيفة الليزوزوم منع فقدان PFKM، بينما لم يؤثر تثبيط البروتيازوم — نظام التخلص من البروتين الآخر — على ذلك. كشف تحليل التسلسل عن محفز قصير "ميثيل-أرجينين ديجرون" فريد في PFKM. أضاف الإنزيم PRMT1 علامة ميثيل محددة على أرجينين داخل هذا المحفز، وهذا الوسم سمح لآلية الميكروأوتوفاجي، بما في ذلك البروتين VPS4، بسحب PFKM إلى الليزوزومات لهضمها. تعطيل PRMT1 أو VPS4 ثبت PFKM ومنع إزالته.
من خلية جذعية إلى ليف عضلي عامل
باستخدام مجموعات بيانات أحادية الخلية بشرية كبيرة، رسم المؤلفون مستويات PFKM عبر العديد من أنواع خلايا العضلات. كانت خلايا جذع العضلات، التي تبقى خاملة حتى الحاجة للإصلاح، تحتوي على قليل جدًا من PFKM لكنها عبّرت عن العديد من جينات مسار فوسفات البنتوز ومكونات الليزوزوم. مع التزام الخلايا بأن تصبح عضلة واندماجها لتكوّن ألياف متعددة النوى، ارتفعت نسخ وبروتين PFKM بشكل حاد، بينما خفت أهداف Wnt وجينات الليزوزوم. في خلايا عضلية بشرية وفأرية مزروعة، دفعت Wnt بسرعة PFKM إلى الليزوزومات في الخلايا المبكرة ذات النواة الواحدة ولكن ليس في الألياف متعددة النوى الناضجة. يدعم هذا النمط نموذجًا تفيد فيه الخلايا غير المتمايزة بالحفاظ على مستويات منخفضة من PFKM — عبر التحلل الليزوزومي — لتعزيز الأيض الوقائي، ثم تعيد التعبير عنه أثناء انتقالها إلى ألياف قابضة تستهلك طاقة كبيرة.
ماذا يحدث عندما يعلق المفتاح
لاختبار مدى أهمية PFKM في بناء العضلة، قلّل الفريق مستوياته بواسطة التدخّل RNAi. الخلايا ذات PFKM المنخفض كافحت لتشغيل جينات العضلة المميّزة، أنتجت بروتين الميوسين أقل، وشكلت عددًا أقل وأليافًا متعددة النوى أصغر، على الرغم من أن أعداد الخلايا الإجمالية لم تتغير. كشفت ملفات المستقلبات عن انخفاض في وسائط التحلل السكرّي اللاحقة ووقود دورة حمض ثلاثي الكربوكسيل، لكن ارتفعت جينات وعلامات مسار فوسفات البنتوز، إلى جانب مقاومة محسّنة للإجهاد التأكسدي. والأهم من ذلك، أن تزويد الخلايا ب3‑فوسفوجليسيرات — وسيط تحلل سكرّي يقع عادةً بعد PFKM — عالج العديد من عيوب التمايز. تعافت مؤشرات العضلة وتكوّن الألياف، مما يدل على أن المستقلبات الناقصة، وليس فقدان بروتين PFKM بحد ذاته، كانت العائق الرئيسي. 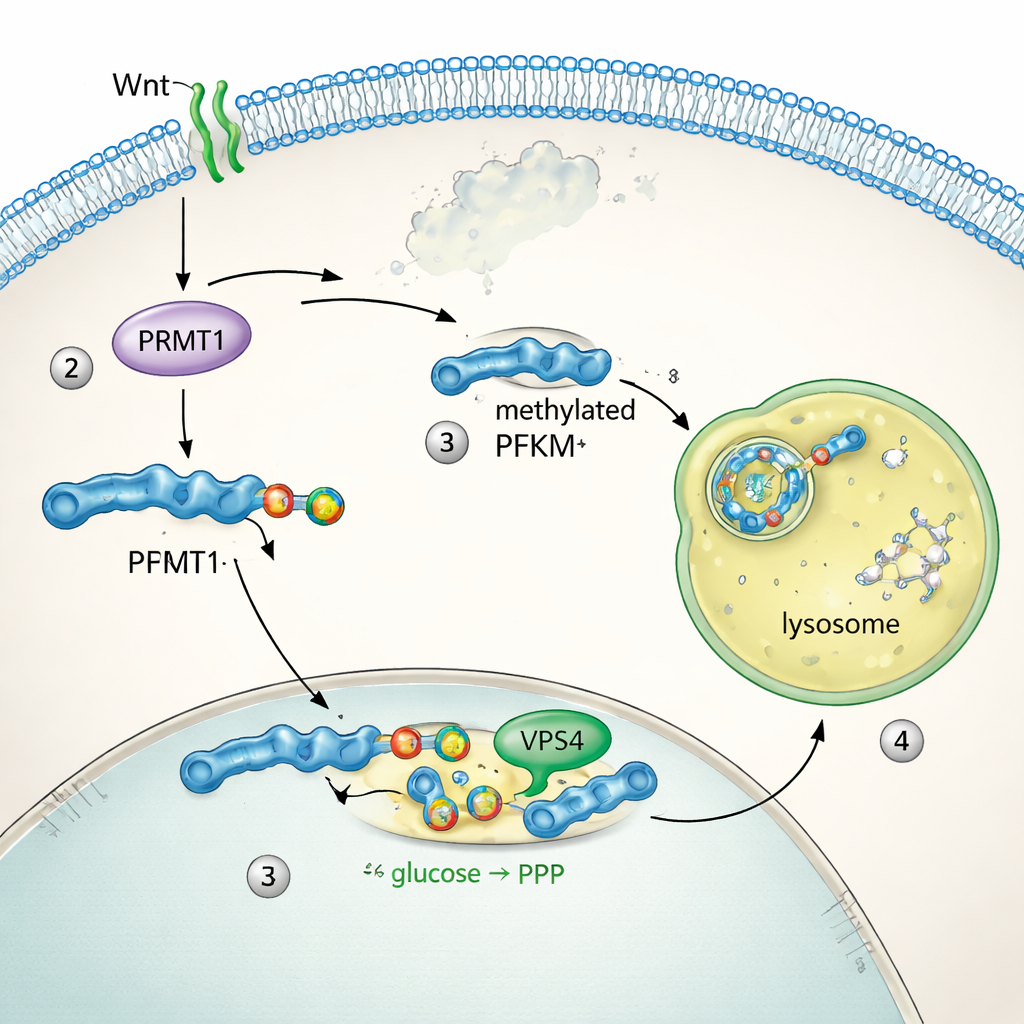
تداعيات على صحة العضلات والإصلاح
لغير المتخصص، الرسالة المركزية هي أن خلايا العضلات لا "تحرق السكر" ببساطة أكثر أو أقل؛ بل تعيد توجيهه بعناية بين إنتاج الطاقة وحماية الخلية اعتمادًا على مرحلة حياتها. يعمل PFKM كصمام يمكن التحكم به عند هذا المفترق. في الخلايا الشبيهة بالجذع، يؤدي الوسم المدفوع بـWnt وتدمير الليزوزوم لـPFKM إلى إعادة توجيه الجلوكوز إلى مسار يحمي الخلايا ويهيئها للنمو المستقبلي. مع نضوج الخلايا إلى ألياف عاملة، تعيد بناء مخزون PFKM وتميل الأيض نحو استخدام طاقة عالي الإنتاج. يؤدي تعطيل هذا التوازن، كما يُرى في اضطرابات نادرة بنقص PFKM، إلى تعطيل التطور العضلي الطبيعي. من خلال كشف المقابض الجزيئية لهذا المفتاح، توحي الدراسة بأن العلاجات المستقبلية قد تضبط تجدد العضلات أو تحمي العضلات في الأمراض والشيخوخة عبر تعديل طفيف لنشاط PFKM أو بتقديم المستقلبات المناسبة بعد المسار.
الاستشهاد: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
الكلمات المفتاحية: تمايز عضلات الهيكل العظمي, استقلاب الجلوكوز, إنزيم PFKM, مسار فوسفات البنتوز, تحلل البروتين الليزوزومي