Clear Sky Science · ar
التعبير خارج موقعه لإنزيم DHODH السيتوزولي يفصِل تخليق البيريميدين الجديد عن سلسلة نقل الإلكترون الميتوكوندرية
لماذا يهم كسر رابط خفي داخل خلايانا
تحتاج كل خلية في جسمك باستمرار إلى نسخ وإصلاح حمضها النووي، وهي عملية تتطلب تزويداً ثابتاً من “الحروف” الكيميائية المسماة البيريميدينات. في معظم الحيوانات، يرتبط تصنيع هذه الحروف ارتباطاً وثيقاً بكيفية احتراق الميتوكوندريا—محطات طاقة الخلية—للوقود باستخدام الأكسجين. هذا الارتباط يعني أنه عندما يتعطل التنفّس الميتوكوندري، تنقص لبنات بناء الحمض النووي وتكافح الخلايا للنمو. تظهر الدراسة الملخّصة هنا أن استعارة جين واحد من خميرة الخبز يمكن أن يفصل بوضوح بين هذين العمليتين. هذه التعديل الجيني يسمح للخلايا الثديية بمواصلة صنع حروف الحمض النووي حتى عندما تتعرض ميتوكوندرياتها للضرر، ما يفتح طريقاً جديداً لفحص، وربما يوماً ما لعلاج، الأمراض الناجمة عن خلل في استقلاب الطاقة.
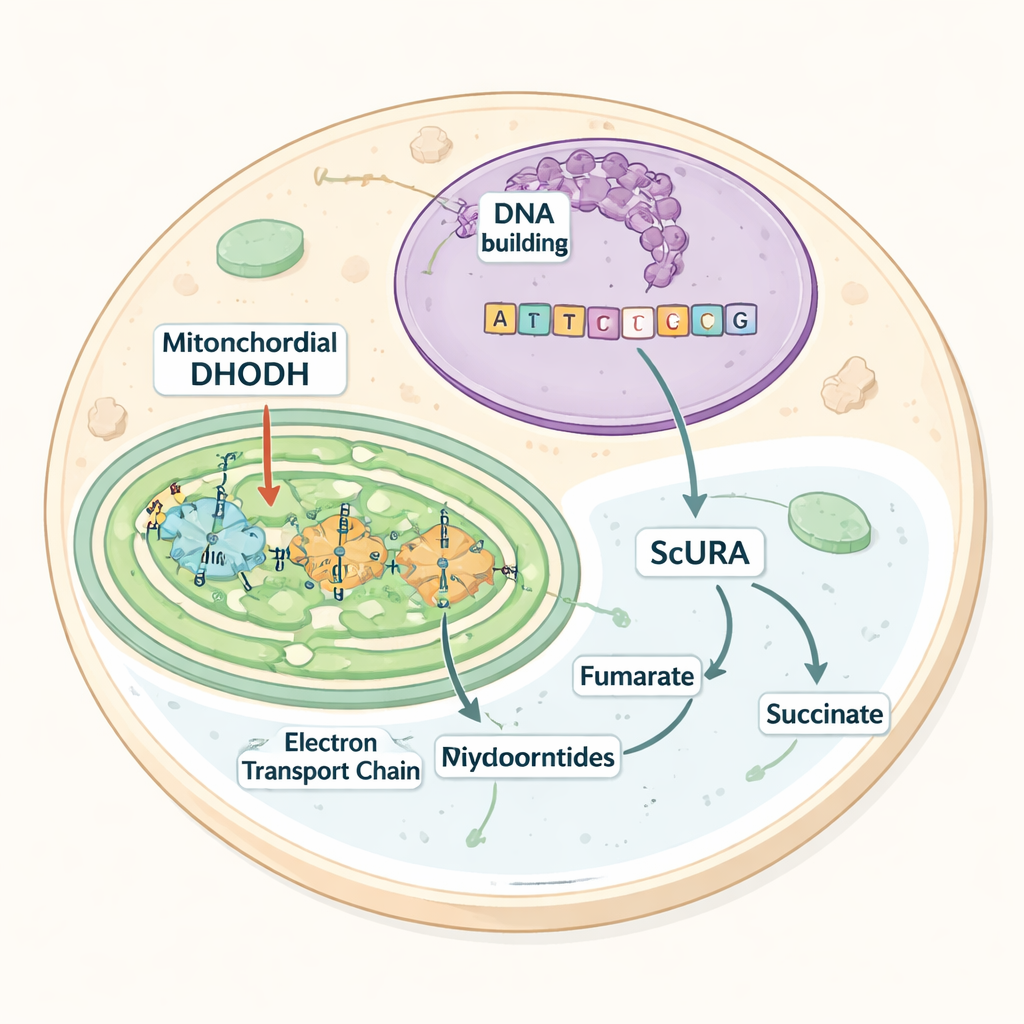
أداة مستعارة من الخميرة
تركز العمل على إنزيم يسمى ديهيدروأورات ديهيدروجيناز (DHODH)، الذي يؤدي خطوة رئيسية في بناء البيريميدينات. في الثدييات، يقع DHODH على الغشاء الداخلي للميتوكوندريا وينقل الإلكترونات إلى ناقل يغذي سلسلة التنفّس. إذا انقطع هذا التدفق الإلكتروني—على سبيل المثال بسبب مثبطات دوائية أو عيوب جينية—يتوقف عمل DHODH، ويتوقف إنتاج البيريميدين، وتصبح الخلايا معتمدة على اليوريدين المأخوذ غذائياً أو المضاف. العديد من الميكروبات التي تزدهر دون أكسجين تتجنب عنق الزجاجة هذا باستخدام نسخ بديلة من DHODH تطفو في سائِل الخلية وتستخدم مستقبلات إلكترون مختلفة. تساءل المؤلفون عما إذا كان بإمكانهم تركيب مسار مستقل عن الأكسجين مماثل في الخلايا الثديية.
إعادة توصيل طريقة صنع حروف الحمض النووي
أدخل الباحثون جين URA1 من خميرة Saccharomyces cerevisiae إلى خلايا بشرية. يشفر URA1 لإنزيم سيتوزولي أُطلق عليه ScURA، يؤدي نفس الخطوة الكيميائية مثل DHODH الميتوكوندري لكنه ينقل الإلكترونات إلى جزيء يُسمى الفورمات بدلاً من الناقل الميتوكوندري. أظهرت الاختبارات الكيميائية الحيوية أن ScURA شكل ثنائيات نشطة في السيتوسول وأضاف نشاط DHODH مقاوم للأدوية. في الظروف الطبيعية، لم يؤدِّ إدخال ScURA إلى اضطراب في بنية الميتوكوندريا أو في التنفّس أو في النمو، مما يشير إلى أنه يعمل كمسار احتياطي بدلاً من أن يكون عبئاً إضافياً.
خلايا تتجاهل عوائق الميتوكوندريا
لمعرفة ما إذا كان هذا المسار الاحتياطي يمكن أن يحل محل النظام الأصلي، عرّض الفريق الخلايا لكبح كيميائي إما لـ DHODH نفسه أو لسلسلة نقل الإلكترون الميتوكوندرية، وهي علاجات عادة ما توقف انقسام الخلايا ما لم يُزوَّد اليوريدين. واصلت الخلايا المعبرة عن ScURA التكاثر دون أي مساعدة، حتى تحت تثبيط قوي للمجمع التنفّسي الثالث أو بعد حذف جيني لجين DHODH الداخلي. أظهر تتبع مفصّل لذرات النيتروجين والكربون من الغلوتامين الموسوم أن الخلايا المعبرة عن ScURA استمرت في تركيب نوكليوتيدات البيريميدين على الرغم من هذه العوائق. وكشفت قياسات المستقلبات أنه بدلاً من تراكم سواتق سامة، قننت خلايا ScURA الإلكترونات إلى الفورمات، منتجة سوكسينات وعاكسة بشكل طفيف دورة حمض ثلاثي الكربوكسيل (TCA) لدعم ناقل الفورمات–سوكسينات بين السيتوسول والميتوكوندريا.
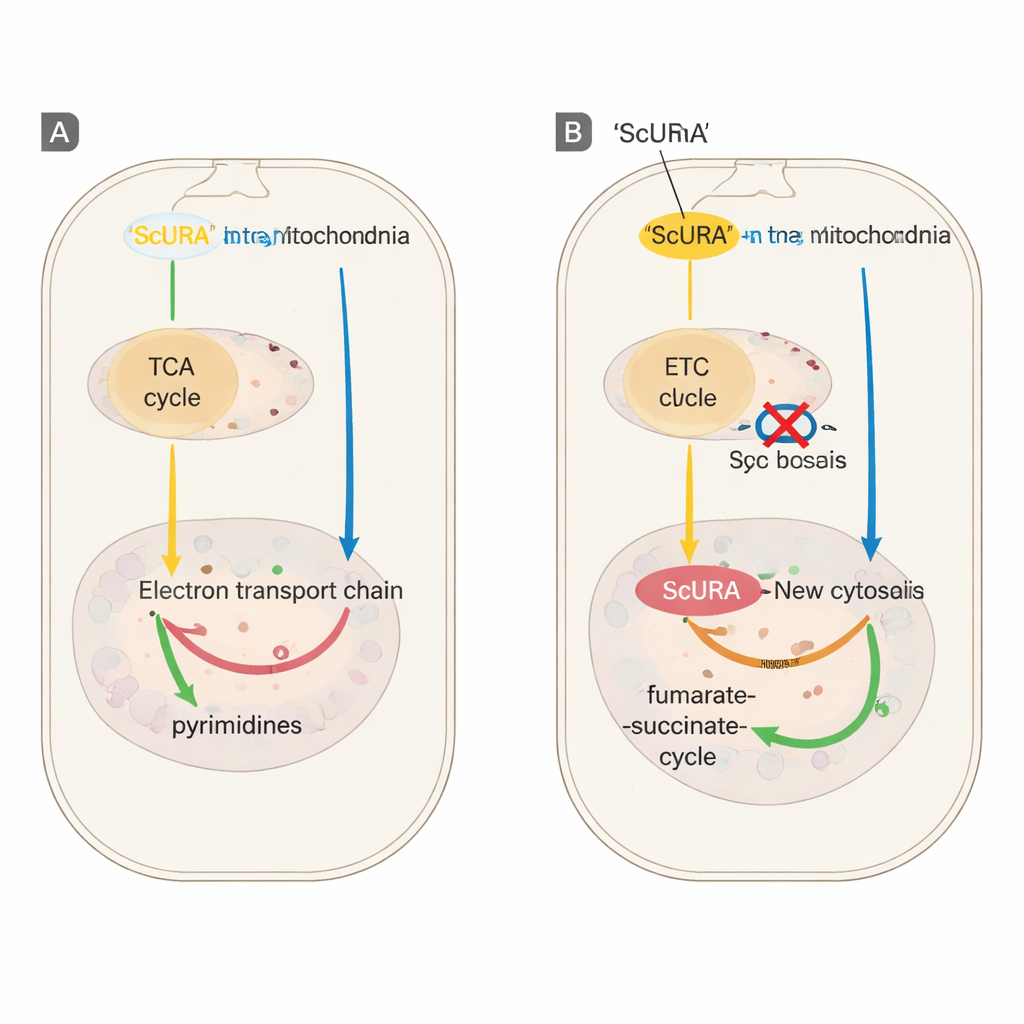
إنقاذ خلايا ذات محطات طاقة متضررة
اختبر المؤلفون بعد ذلك ScURA في نماذج خلوية لأمراض الميتوكوندريا. الخلايا الخالية من الحمض النووي الميتوكوندري، أو التي تحمل طفرات تُقوّض المجاميع التنفسية الثالثة أو الرابعة، تعتمد عادة على اليوريدين المضاف للنمو. بعد تعديلها للتعبير عن ScURA، تمكنت هذه الخلايا الطافرة المتنوعة من التكاثر دون اليوريدين، على الرغم من أنها لا تزال تحتاج إلى البيروفات، مما يعكس حاجة متبقية لبعض نشاط الميتوكوندريا. وعلى مستوى التعبير الجيني، منع ScURA أيضاً إيقاف جينات بروتينات الريبوسوم الذي يحدث عادة عقب تثبيط مزمن لسلسلة نقل الإلكترون، من خلال إبقاء إمدادات لبنات البيريميدين كافية للحفاظ على إنتاج الرنا.
ماذا يعني هذا للصحة والمرض
من خلال فصل تخليق البيريميدين عن التنفّس الميتوكوندري بشكل واضح، يوفر ScURA للباحثين ذراعاً قوية جديدة: يمكنهم الآن أن يسألوا، في العديد من السياقات، ما إذا كان عيب معين أو تأثير دواء ما نابعاً فعلاً من فقدان إنتاج الطاقة أم من نقص لبنات بناء الحمض النووي والرنا. على المدى البعيد، قد تكمل استراتيجيات مماثلة العلاجات الجينية الحالية لاضطرابات الميتوكوندريا، أو تساعد في تفسير لماذا تعتمد بعض الأورام اعتماداً كبيراً على استعادة وظيفة ميتوكوندرية. ومع أن تحويل إنزيم خميري إلى علاج بشري سيتطلب حذراً بالغاً، تُظهر هذه الدراسة أن جيناً واحداً مختاراً بعناية يمكنه إعادة كتابة رابط استقلّ التطور على مرّ الزمن.
الاستشهاد: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
الكلمات المفتاحية: تمثيل البيريميدين, وظيفة الميتوكوندريا, سلسلة نقل الإلكترون, إعادة توصيل التمثيل الغذائي, أمراض الميتوكوندريا