Clear Sky Science · ar
تدفق تحلل السيستئين المنظم بواسطة لامين A/C يغير مصير الخلايا الجذعية عبر إعادة برمجة الشيفرة فوق الجينية
كيف يتواصل هيكل الخلية مع أيضها
لماذا تبقى بعض الخلايا شابة ومرنة في ما يمكن أن تتحول إليه بينما تتقدم أخرى في العمر أو تُقفل على هوية خاطئة؟ تكشف هذه الدراسة عن حوار مفاجئ داخل خلايانا بين "السقالة" النووية التي تشكل الحمض النووي ومغذٍ يحتوي على الكبريت، السيستئين. من خلال إظهار كيفية توجيه هذا الحوار للخلايا الجذعية نحو مصائر صحية — أو نحو شيخوخة مبكرة — تلمّح الدراسة إلى أن ما "تأكله" الخلايا وكيف تعالجه قد يُمكن ضبطه يوماً ما لمنع بعض الأمراض الجينية وربما إبطاء جوانب من الشيخوخة.
الدور الخفي للغلاف النووي
في عمق كل خلية، يُضغط الحمض النووي على شبكة بروتينية تُسمى اللِّمينة النووية، مبنية جزئياً من بروتينات تُدعى لامين A ولمين C. لا تمنح هذه اللّامين فقط النواة شكلها، بل تساعد أيضاً في تحديد أي الجينات تُقفل وأيها تبقى متاحة. درس المؤلفون خلايا جذعية جنينية للفأر في حالتها الأكثر مرونة أو "البدئية" ووجدوا أن لامين A/C عادةً يكبح نشاط إنزيمين أيضيين، CBS وCTH، اللذين يساعدان في تصنيع وتحليل السيستئين. عندما يكون لامين A/C موجوداً وفعالاً، تُكبَح هذه الإنزيمات ويظل مسار معالجة السيستئين منخفضاً، ما يدعم حالة خلوية جذعية مستقرة وشابة. 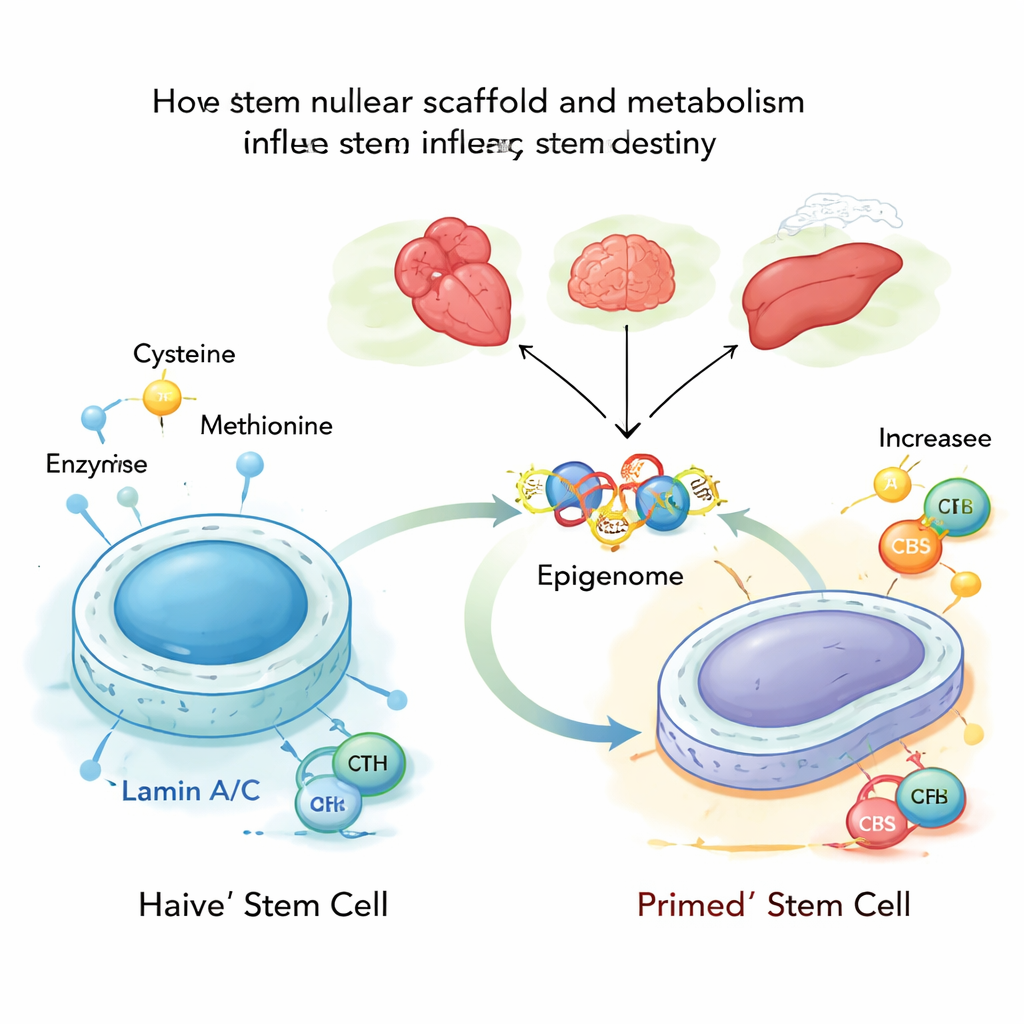
عندما ينهار التركيب، يتسارع الأيض
بعد ذلك، أزال الباحثون لامين A/C أو أدخلوا طفرة مرتبطة بمرض تُحاكي اضطراب شيخوخة مبكرة بشري يُسمى مرض هاتشينسون–غيلفورد بروغيريا. من دون لامين A/C الطبيعي، تصبح جينات CBS وCTH أكثر قابلية للوصول ويزداد ارتباطها بعامل نسخ يسمى SP1، فتُفعل. هذا التحول يدفع مزيداً من السيستئين عبر مسار أيضي ينتهي بخلية ناقلة صغيرة تسمى أسيتيل‑CoA، التي تحمل مجموعات أسيتيل تُستخدم لفك تكدس الحمض النووي. مع تزايد توجيه السيستئين نحو أسيتيل‑CoA، تُضاف مجموعات الأسيتيل تفضيلياً إلى بقع محددة على بروتينات الهيستون — خصوصاً موضعين على الهيستون H3 المعروفين باسم K9 وK27 — مما يجعل الجينات المجاورة أسهل في التفعيل.
من الوسوم الكيميائية إلى قرارات مصير الخلية
تعمل هذه التغيرات في "وسوم" الهيستون كإعادة ضبط عالمية للوحات التحكم الخلوية. في الخلايا الجذعية البدئية، يؤدي تعزيز CBS وCTH، أو ببساطة تزويد الخلايا بمزيد من السيستئين، إلى دفع الخلايا نحو حالة أكثر تقدماً و"متهيئة" تقترب أكثر من تكوين أنسجة حقيقية. تُفعّل جينات متورطة في تطور القلب وخطوط نَسجية أخرى، ويتغير الطي ثلاثي الأبعاد للحمض النووي ليُفضّل هذه البرامج. على النقيض، فإن خفض نشاط CBS وCTH أو تقييد السيستئين يساعد على استعادة هوية أكثر بدائية وشباباً حتى عندما يتضرر الغلاف النووي. في نماذج جنينية، أدى هذا الخلل الأيضي إلى تشكيل منحاز للطبقات الجرثومية الثلاث — اللبنات الأولية لكل الأعضاء — وتحول غير طبيعي نحو خلايا عضلة القلب ما لم تُعاد معايرة CBS وCTH. 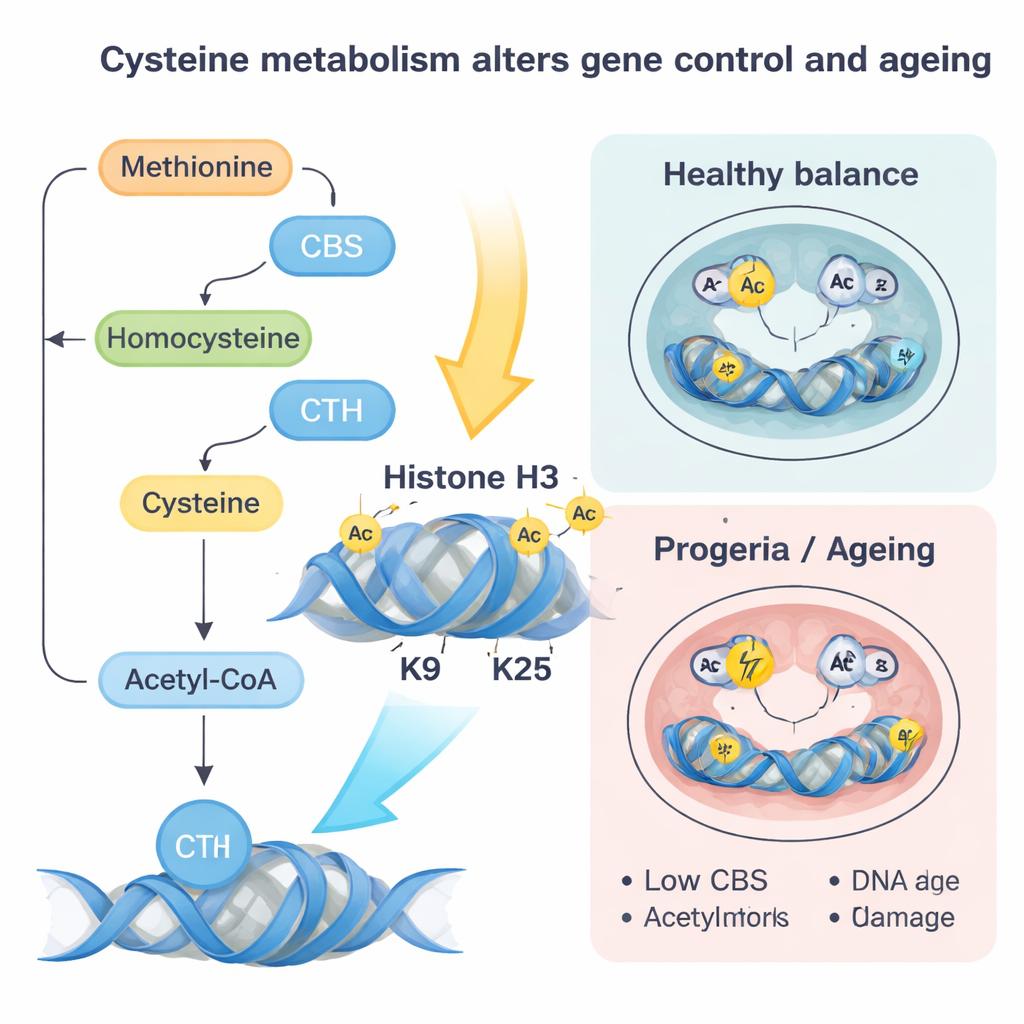
الأيض، علامات الحمض النووي والشيخوخة المبكرة
رَوت طفرة اللامين الشبيهة بالبروغيريا قصة مكملة. هنا، تنخفض مستويات CBS وCTH، مما يقلل من تدفق السيستئين وأسيتيل‑CoA من هذا المسار. وفي الوقت نفسه، يُعاد توجيه الهوموسيستئين إلى دورة الميثيونين، ما يرفع مستويات SAM، الناقل العالمي لمجموعات الميثيل. هذا يُفضّل زيادة الوسوم الميثيلية، خاصة علامة تُدعى H3K9me3 التي يضعها إنزيم SUV39H1، والتي تضيق الكروماتين وترتبط بتدهور إصلاح الحمض النووي. أظهر المؤلفون أن إعادة توازن لطيفة لـ CBS أو تقييد الميثيونين خفضت SAM، وقلّلت هذه الوسوم القمعية، وحسّنت إصلاح الحمض النووي، وخفّضت مؤشرات الإجهاد التأكسدي والشيخوخة الخلوية، وأنقذت جزئياً تمايز خلايا القلب. لوحظت هبوط مماثل في CBS وارتفاع في الوسوم القمعية في قلوب الفئران المسنة الطبيعية وفي خلايا ليفية بشرية من أشخاص كبار وفي مرضى البروغيريا، ما يقترح أن هذه الدائرة تعمل أيضاً في الشيخوخة الطبيعية.
ماذا يعني هذا للصحة والشيخوخة
لغير المتخصصين، الرسالة أن الإطار البنيوي للخلية وأيضها مرتبطان ارتباطاً وثيقاً: عندما يتعرّض الغلاف النووي المصنوع من لامين A/C للخلل، يتغير استخدام السيستئين، والذي بدوره يعيد كتابة الوسوم الكيميائية على بروتينات تغليف الحمض النووي. هذه الوسوم تقرر أي الجينات تُشغّل أثناء بناء الخلايا الجذعية للجسم وتساهم في تحديد مدى كفاءة الخلايا في إصلاح الضرر طوال الحياة. عبر ضبط إنزيمات مثل CBS وCTH بعناية — أو تعديل إمداد المغذيات مثل الميثيونين والسيستئين — قد يصبح من الممكن تصحيح بعض الأخطاء في كتابة هذه الوسوم في أمراض مرتبطة باللمين وربما التخفيف من جوانب الشيخوخة المبكرة أو الطبيعية.
الاستشهاد: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
الكلمات المفتاحية: الخلايا الجذعية, الغلاف النووي, تمثيل السيستئين, علم فوق الجينات, الشيخوخة