Clear Sky Science · ar
عمق وضعية الارتباط يغير فعالية الليجندات القابلة للتبديل بالضوء عند مستقبل 5-HT2A
تسليط الضوء على أدوية قابلة للتبديل في الدماغ
تخيل دواء يمكنك تشغيله وإيقافه بوميض ضوئي، موجهًا مستقبلات الدماغ بدقة مع تقليل الآثار الجانبية. تبحث هذه الدراسة في هذه الفكرة بالتحديد لمستقبل سيروتونيني رئيسي مرتبط بالمزاج والإدراك والمخدرات المهلوسة. لقد تحقق الباحثون من سبب تباين سلوك جزيئين حساسَين للضوء متقاربي الشكل—أحدهما يتصرف تقريبًا كمفتاح تشغيل/إيقاف مثالي، والآخر يرفض الإغلاق تمامًا. يكمن جوابهم في عامل بسيط مدهش: مدى عمق الجزيء داخل المستقبل.
أدوية يقودها الضوء في الدماغ
تصمم الأدوية النشطة بالضوء، المعروفة أيضًا كأدوات الفارماكولوجيا الضوئية، بحيث يقلب شعاع الضوء جزءًا من الجزيء بين شكلين، مثل نسخة منحنية وأخرى مستقيمة. يمكن لتلك الأشكال أن تغير قوة ارتباط الدواء بهدفه. في هذا العمل، الهدف هو مستقبل 5-HT2A البشري، بروتين على خلايا الدماغ يستجيب للسيروتونين وله دور أساسي في التأثيرات المضادة للذهان والهلوسة. الجزيئات المدروسة مشتقات لـ N,N-ديميثيلتريبتامين (DMT)، مُعدَّلة بوحدة أزوبنزينية حساسة للضوء. يختلف الإصداران فقط في موضع مجموعة ميثوكسي صغيرة على حلقة—إما في موضع «بارا» أو «مِتا»—ومع ذلك يتباين سلوكهما البيولوجي تحت الضوء اختلافًا كبيرًا.
جزيئتان شبه توأمتين، مفاتيح مختلفة جدًا
في اختبارات خلوية، يتصرف الإصدار البارا، المسمى المركب 1، تقريبًا كمفتاح رقمي. في الظلام، شكلُه «ترانس» يكاد لا ينشط المستقبل بل ويمنعه قليلًا، متصرفًا كمضاد ضعيف. عندما يقلبه الضوء إلى الشكل «سيس»، يتحول نفس الجزيء إلى منشط معتدل، يدرِك المستقبل جزئيًا. الإصدار مِتا، المركب 2، يرفض التعاون بهذه الطريقة: كلا شكليه الضوئي والداكن يبقيان المستقبل نشطًا إلى حد ما، دون أن يقدمَا حالة «إيقاف» حقيقية. اللغز المركزي في هذه الورقة هو لماذا يغير تعديل كيميائي ضئيل جدًا—مجرد تحريك مجموعة صغيرة حول حلقة—استجابة المستقبل بشكل قوي للغاية.
الاطلاع الداخلي بأفلام على مستوى الذرات
لحل هذا، استخدم الفريق محاكيات ديناميكا جزيئية شاملة على مستوى جميع الذرات، مجريين عمليًا أفلامًا مفصلة لكل ذرة في المستقبل والغشاء المحيط والماء وكل ليجند على مدى إجمالي يقارب 80 ميكروثانية. حاكونا الجزيئين في كل من أشكالهما المحكومة بالضوء، وفي كلٍ من الحالات غير النشطة والنشطة لمستقبل 5-HT2A. بواسطة تتبع «المفاتيح الدقيقة» البنيوية المعروفة داخل البروتين—مثل تريبتوفان محوري يقلب موضعه، جسر ملحي ينكسر، وحركة الصوديوم والماء في النواة—تمكنوا من معرفة متى يميل المستقبل إلى حالة إيقاف أو تشغيل. كما قارنوا مدى محاكاة الجزيئات الجديدة لوضعية ارتباط الـ LSD، وهو منشط جزئي معروف، باستخدام تداخل أنظمة الحلقات كمرشد.
العمق أهم من الشكل وحده
الفكرة الأساسية هي أن فعالية الجزيئات تُحكم أساسًا بمدى عمقها داخل جيب الارتباط في المستقبل. في المستقبل غير النشط، شكل الترنس للمركب بارا يشكل مجموعة خاصة من روابط الهيدروجين التي تسحبه إلى عمق غير عادي، أسفل المنطقة التي تحدث فيها الاتصالات المنشِّطة النمطية. هذا «الانغراس المفرط» يمنعه من لمس بقايا قطبية أساسية تساعد على تشغيل المستقبل، فيثبت بالتالي حالة الإيقاف. شكل الترنس لمركب مِتا لا يمكنه تكوين نفس روابط التثبيت ويجلس بدلًا من ذلك أعلى في وضع يشبه LSD ومتوافق مع التنشيط، ما يفسر نشاطه المتبقي. عندما يقلب الضوء كلا الجزيئين إلى أشكال السيس، فإنهما عمومًا يتحركان إلى أوضاع أضحل وأكثر شبهًا بالمنشطات. ومع ذلك، تظل الهندسة مهمة: في المستقبل النشط، يمكن للمركب السيس 2 الانزلاق أعمق في نفق محب للدهون بين حلزونيْن وتشكيل رابطة هيدروجينية مستمرة تعزز سلوكه كمنشط قوي، بينما يُحجب المركب السيس 1 بمحددات مكانية من القيام بذلك.
التحكم الدقيق بالماء والأيونات الداخلية
تُظهر المحاكاة أيضًا أن عمق الارتباط يضبط بدقة جيبًا داخليًا للصوديوم ومسارًا مائيًا معروفين بتأثيرهما على تنشيط المستقبل. يَحافظ الارتباط العميق والثابت للمركب بارا في شكل الترنس على أيون صوديوم محبوس بإحكام والمنطقة المحيطة جافة نسبيًا، وهي سمات مرتبطة بحالة الإيقاف. بالمقابل، يسمح الارتباط الأكثر حركةً للمركب مِتا أو لأشكال السيس بدخول المزيد من الماء وإرخاء بيئة الصوديوم، ممهِّدًا المستقبل للتنشيط. يمكن لبقايا عطرية تعمل كـ«مفتاح تبديل» أن تقلب اتجاهها بسهولة أكبر عندما تكون الليجندات مرنة وغير مفرطة التثبيت، مما يدفع المستقبل نحو حالة شبيهة بالتشغيل، خاصة مع المركب السيس 2.
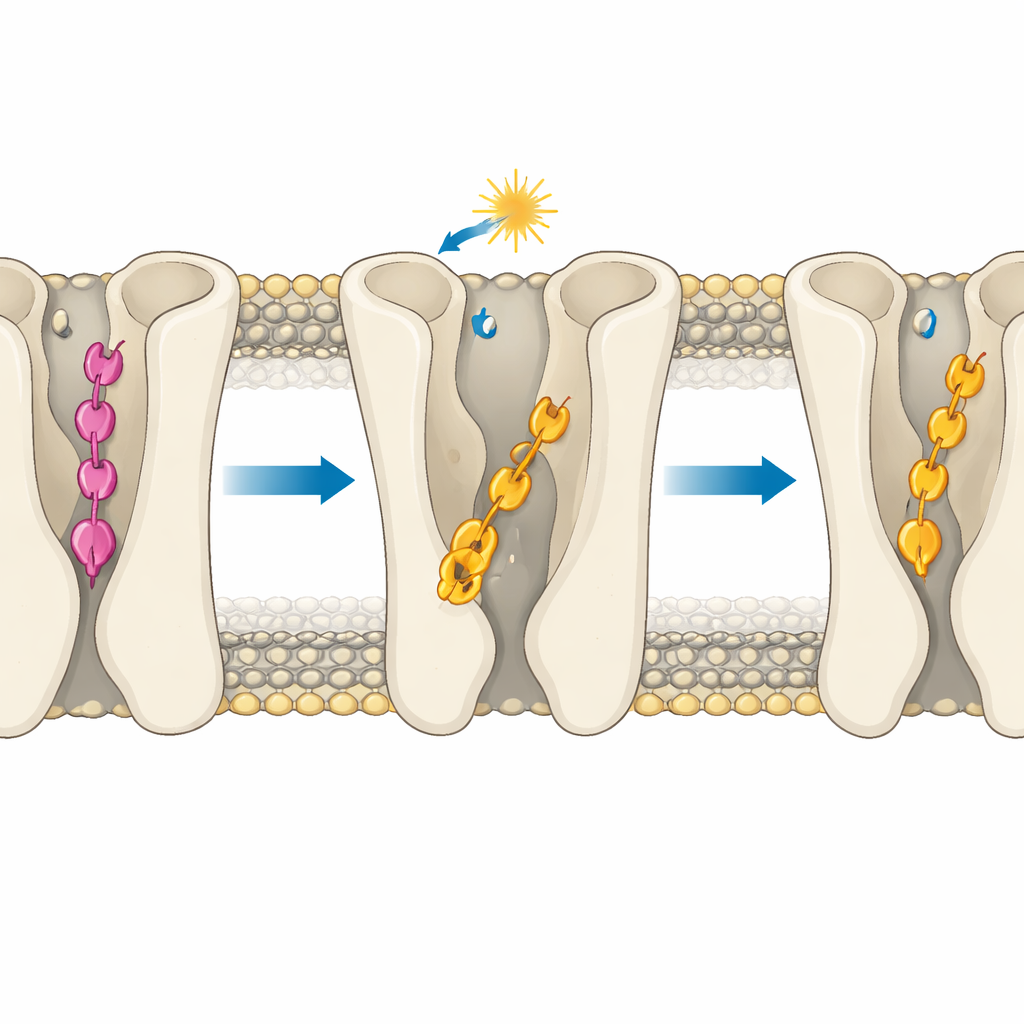
قواعد تصميم لأدوية مستقبلية مسيطرة بالضوء
لغير المتخصصين، الرسالة أن العمق الدقيق الذي يستقر عنده الدواء في جيب المستقبل يمكن أن يصنع الفارق بين إيقاف، تشغيل جزئي، وتشغيل قوي—حتى عندما يبدو التغيير الكيميائي ضئيلًا على الورق. من خلال إظهار كيف يمكن لليجند قابل للتبديل بالضوء أن ينغرس بشكل مفرط ويقفل المستقبل بإيقافه، بينما يبقى نظيره القريب عند عمق ملائم للتنشيط، تقدم الدراسة قاعدة تصميم واضحة: تحكم في عمق الانغراس بنفس درجة التحكم في تغيّر الشكل الناتج عن الضوء. يمكن أن توجه هذه الرؤى إنشاء مركبات حساسة للضوء من الجيل القادم تعالج اضطرابات الدماغ بدقة غير مسبوقة، رافعةً أو مخفِّضة إشارات الطرق الخلوية بطريقة قابلة للعكس ومضبوطة مع تقليل الآثار الجانبية.
الاستشهاد: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
الكلمات المفتاحية: الفارماكولوجيا الضوئية, مستقبل السيروتونين 5-HT2A, ليجندات قابلة للتبديل بالضوء, تنشيط مستقبلات GPCR, محاكاة الديناميكا الجزيئية