Clear Sky Science · ar
سلوك القالب والعميل والتنظيم البنيوي في تكاثفات البروتين متعددة المكونات كما تكشفها دراسة قطيرات tau/TDP-43
بروتينات تتصرّف مثل قطرات زيت صغيرة
داخل خلايانا، العديد من البروتينات لا تبقى مخلوطة بشكل متجانس في السائل الداخلي. بدلاً من ذلك، تتجمع في قطرات سائلة صغيرة، شبيهة إلى حد ما بالزيت في الماء. تدرس هذه الدراسة كيفية تجمّع بروتينين من هذا النوع، تاو وTDP-43، المرتبطين ارتباطًا وثيقًا بمرض ألزهايمر وأشكال أخرى من الخرف، داخل القطيرات معًا. من خلال كشف كيفية تشكّل هذه القطيرات واندماجها وتنظيمها، يقدم العمل دلائل حول سبب ظهور تجمعات بروتينية ضارة في أدمغة الشيخوخة وكيف قد نتمكن في المستقبل من السيطرة عليها.
لماذا هذان البروتينان مهمان للدماغ
من المعروف أن تاو وTDP-43 يشكلان تراكمات سامة في الأمراض التنكسية العصبية. تقليديًا درس العلماء كل منهما على حدة، لكن تشريح الجثث لأدمغة بشرية أظهر بشكل متزايد أن كلا البروتينين يمكن أن ينتهي بهما الأمر في المناطق نفسها المتضررة. يثير ذلك سؤالًا جوهريًا: عندما يتواجدا معًا في الخلايا، كيف يتشاركان المساحة داخل القطيرات وهل يشجّع هذا التشارك على تكوّن تراكمات ذات صلة بالمرض؟ اختار الباحثون نموذجًا مبسطًا لكن واقعيًا باستخدام تاو وذيل TDP-43 ذي التعقيد المنخفض (LCD)، وهو الجزء الأكثر مسؤولية عن تشكّل القطيرات وتصلّبها اللاحق.
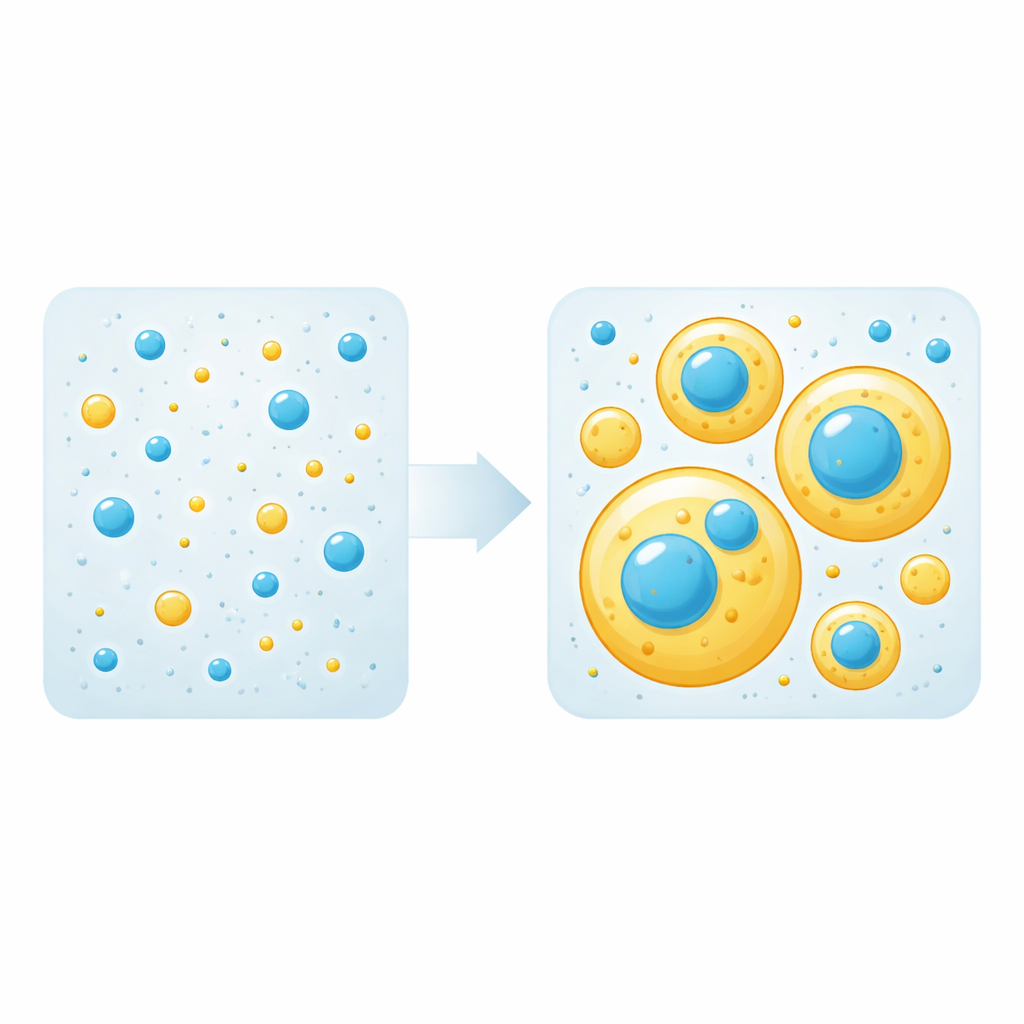
قطيرات، «هياكل داعمة»، و«عملاء»
تتشكل مثل هذه القطيرات السائلة عندما تفوق التجاذبات بروتين–بروتين تجاذبات بروتين–ماء، مما يتسبب في انقسام المحلول إلى طور كثيف (القطيرات) وطور مخفف. في الخلطات، يحتاج بناء القطيرات إلى بعض البروتينات فقط؛ تُسمى هذه «هياكل داعمة» (scaffolds). أما الأخرى فتركب فقط داخل القطيرات كـ«عملاء» (clients). قيّس الفريق أولاً عتبة التركيز التي يبدأ عندها كل بروتين بمفرده بتشكيل قطيرات. ثم مزجوا كميات مختلفة من تاو وLCD الخاص بـTDP-43 وراقبوا، باستخدام مجهر الفلورسنس، ما إذا كانت القطيرات ستظهر وكيف ترتبّت البروتينات داخلها. وعلى نحو لافت وجدوا أن أيًا من البروتينين يمكن أن يلعب دور الهيكل الداعم أو العميل اعتمادًا فقط على تركيزه: فوق عتبة تكوّنه يبني القطيرات، وتحت تلك العتبة يُتجنّب على نحو س пасيفي داخل قطيرات يشكلها الآخر.
قطيرات متعددة الطبقات وهالة غامضة
عندما كان كلا البروتينين وفيرين بما يكفي لتشكيل قطيرات كلٌ بمفرده، لم يمتزجا في قطيرة موحدة متجانسة. بدلًا من ذلك، غلّفت قطرات كبيرة غنية بتاو قطرات أصغر غنية بـTDP-43، مكونة بنية متعددة الأطوار وذات طبقات. أظهرت قياسات كيف تنتشر القطيرات على الزجاج أن قطرات TDP-43 لها توتر سطحي أعلى، لذا فمن الناحية الطاقية من المفضل أن تجلس داخل قطرات تاو الأكثر بللاً. وبرزت سمة ملفتة عند هذه الواجهات: تراكمت تاو بمستويات مرتفعة بشكل خاص كـ«هالة» ساطعة تغطي سطح قطرات TDP-43، حتى عندما كان تركيز تاو نفسه أقل من عتبة تشكيله للقطيرات. مع مرور الوقت، مالت المناطق الغنية بـTDP-43 إلى التصلب إلى مادة أشبه بالصلابة، بينما بقيت المناطق الغنية بتاو سائلة، مما يشير إلى ميول مختلفة للتحول إلى تجمعات طويلة الأمد.
ضبط التفاعلات واستقصاء الآلية المجهرية
اختبر الباحثون بعد ذلك كيف تتحكم قوى جزيئية محددة في أي البروتينين يتصرف كهيكل داعم أو كعميل. أخفَّفوا انتقائياً التفاعلات الكارهة للماء (المدفوعة بالخشونة الهيدر وحيدروفوبيّة) التي تدفع تكاثف LCD الخاص بـTDP-43 باستخدام 1,6-هيكسانديول، وبشكل منفصل أضعفوا التفاعلات الكهربائية (المبنية على الشحنة) التي تدفع تكاثف تاو برفع مستويات الملح. في كل حالة، أدى تعطيل تفاعلات أحد البروتينين الرئيسة إلى منعه من تشكيل القطيرات وتحويله إلى عميل داخل قطيرات الآخر، محاكيًا ما يحدث عند خفض تركيزه. لفهم الهالة بعمق أكبر، غيّروا الملح ليروا مقدار دخول تاو إلى قطرات TDP-43 واستخدموا محاكاة حاسوبية تمثل كل حمض أميني كخرزة مبسطة. أعادت هذه المحاكاة إنتاج الهالة وأظهرت أن أول نحو 40 حمضًا أمينيًا من المنطقة الطرفية النيو-نهائية سالبة الشحنة في تاو تثبت على سطح القطيرة، بينما يمتد باقي الجزيء إلى الخارج في السائل المحيط، مكونًا قشرة «أمفيبيلية» (جزء محب للقطيرة، وجزء محب للماء). أكدت تجارب بقطعة مختصرة من تاو تفتقر إلى هذا الجزء النيو-نهائي أن الهالة تختفي بدونه.

ماذا يعني هذا لمرض الدماغ
تُظهر النتائج معًا مجموعة عامة من القواعد لكيفية تجميع وتنظيم قطيرات البروتين متعددة المكونات. في نظام تاو/TDP-43 هذا، الذي يعكس حالات في الخلايا العصبية المريضة، يحدد كل من التركيز وقوة التفاعل معًا أي البروتينات تبني القطيرات وأيّها يشغلها ببساطة. ثم يشكل التوتر السطحي والترتيبات الأمفيبيلية قطيرات متعددة الطبقات وهالات يمكن أن تركّز بروتينات مرتبطة بالأمراض المتعددة في نفس المساحة المحصورة، مما قد يشجعها على التصلب إلى تجمعات. للمتلقي العام، الرسالة الأساسية هي أن تاو وTDP-43 لا يتكتّلان بشكل عشوائي؛ بل ينظّمان أنفسهما داخل قطيرات سائلة منظمة تحكمها مبادئ فيزيائية بسيطة. إن فهم هذه المبادئ والتلاعب بها في المستقبل قد يفتح طرقًا جديدة لإبطاء أو منع تراكم البروتينات الضارة في الأمراض التنكسية العصبية.
الاستشهاد: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
الكلمات المفتاحية: تكاثفات البروتين, انفصال الطور السائل-السائل, تاو, TDP-43, تنكّس عصبي