Clear Sky Science · ar
جلوكوزيدات يانوس أمفيبيلية أيونية مموّهة بالأزوبينزين لتوصيل pDNA يمكن التحكم فيه بالضوء، بمكوّن واحد وقابل لتعديل العضو
تسليط الضوء على توصيل الجينات الأذكى
تعد علاجات الجينات بقدرتها على معالجة الأمراض من جذورها عبر توصيل أجزاء من الشفرة الوراثية مباشرة إلى خلايانا. لكن توجيه هذه الحمولة الهشة بأمان عبر مجرى الدم، إلى الأعضاء الصحيحة، وداخل الخلايا المستهدفة لا يزال عقبة كبيرة. تُقدّم هذه الدراسة فئة جديدة من الجسيمات الصغيرة المبنية على السكريات والتي يمكن تغيير سلوكها بالضوء قبل دخولها الجسم، مما يتيح للباحثين إعادة توجيه مكان وصول الجين العلاجي ومدى تعبيره، مع الحفاظ على سلامة الخلايا إلى حد كبير. 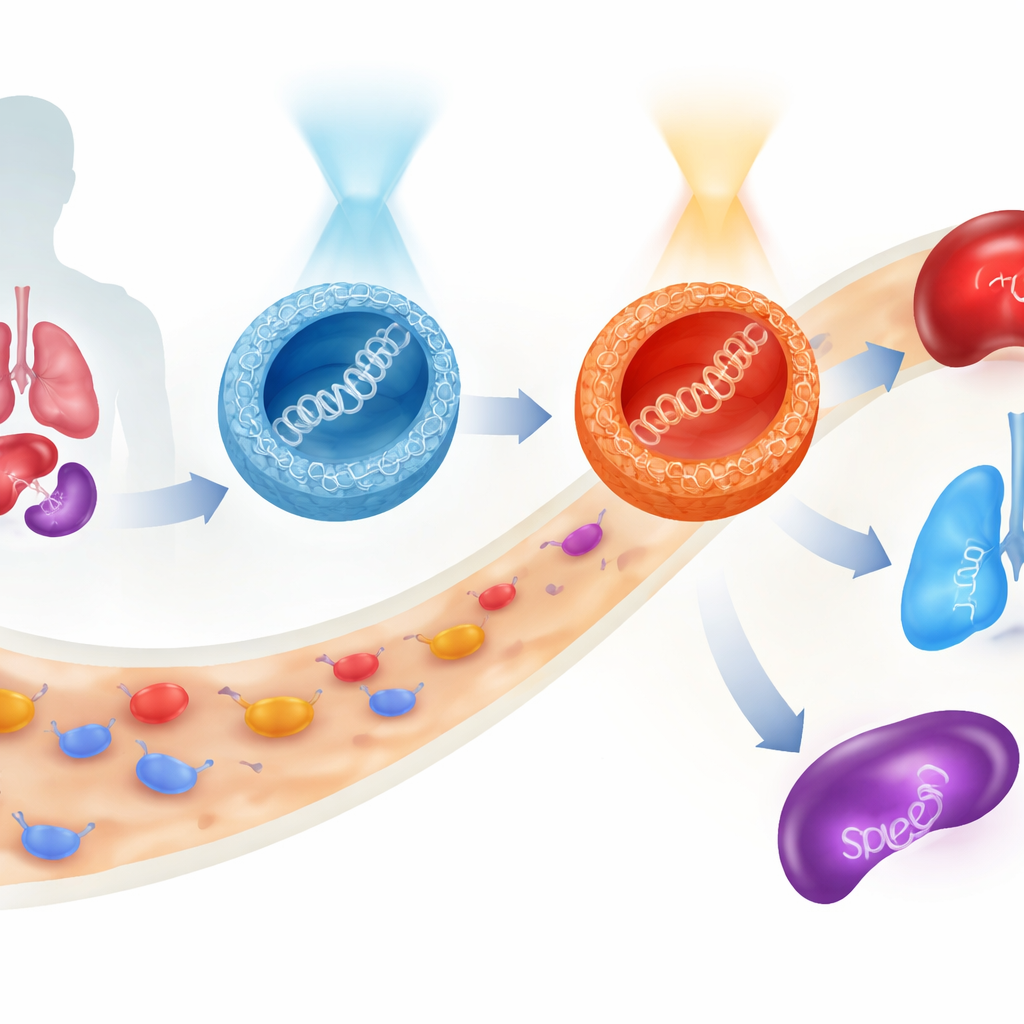
الحاجة إلى ناقلات جينية دقيقة
أكثر وسائل توصيل الجينات نجاحًا اليوم هي الجسيمات النانوية الدهنية، التي ساعدت في تمكين لقاحات mRNA ضد كوفيد-19. هذه القطرات متعددة المكونات تغلف وتحمي الأحماض النووية، لكنها تميل إلى التراكم بشكل رئيسي في الكبد وتفرج جزءًا صغيرًا فقط من حمولتها داخل الخلايا. يمكن لتعديل تراكيبها أن يغير الأعضاء التي تفضلها، ومع ذلك تظل الخلائط معقدة ويصعب التحكم بها بدقة. سعى فريق العمل هنا بدلاً من ذلك إلى تصميم جزيئات مفردة محددة جيدًا تتجمع لتشكل جسيمات نانوية ذات أشكال وسلوكيات متوقعة — وقابلة للتعديل فعليًا من الخارج بواسطة زناد ضوئي بسيط.
ميزان جزيئي يتحكم به الضوء
في قلب النظام الجديد توجد جلوكوزيدات «يانوس» المزدوجة: جزيئات مبنية من وحدتين من الجلوكوز، مزوّدة برؤوس مشحونة محبة للماء وذيول محبة للدهون، ومتحدة عبر «مفصل» مركزي من الأزوبينزين. يمكن للأزوبينزين أن ينقلب بين شكلين متعاكسين مرآتين، يُسمّيان E وZ، عند تعريضه لألوان مختلفة من الضوء. في الماء بوجود الحمض النووي، تتجمع نسخ عديدة من هذه الجزيئات تلقائيًا إلى جسيمات لينة متعددة الطبقات تغلف خيوط الحمض النووي البلازميدي. قام الباحثون بتحضير نسختين — إحداهما بجسور أكسجين وأخرى بجسور كبريت بين السكر والمفصل — لضبط الاستقرار والسلوك البيولوجي بدقة طفيفة. عبر تسليط الضوء على المحاليل مسبقًا، أمكنهم إغناء حالة E أو Z ودراسة كيف يَشكّل كل حال الجسيمات الناقلة للجين الناتجة.
كيف تتصرف الجسيمات المتغيرة الشكل
أظهرت قياسات حجم الجسيمات وشحنة السطح والهيكل الداخلي أن التحويل الضوئي بين حالتي E وZ له تبعات فيزيائية واضحة. عمومًا أنتجت حالة Z جسيمات نانوية أصغر وأكثر تجانسًا ذات داخل أكثر ترتيبًا وطبقاتًا مقارنةً بحالة E. كشفت الميكروسكوبية أن هذه التراكيب الداخلية تشبه صفائح متبادلة من مادة شبيهة بالدهون والحمض النووي. والأهم أن كلا الحالتين حمائتا الحمض النووي من التحلل الإنزيمي. في خلايا مزروعة من الكلى والكبد والأنسجة المناعية، ولّدت حالات الإيزومر المختلفة مستويات تعبير جيني متباينة بشكل ملفت، رغم أن الحمض النووي نفسه كان متماثلاً. دفعات ضوئية متكررة طُبقت بعد دخول الجسيمات إلى الخلايا عزّزت التعبير الجيني عدة أضعاف، مما يشير إلى أن الصدمة الميكانيكية الناتجة عن التحويل تساعد الجسيمات على الارتخاء وإطلاق حمولتها، وقد تساعدها أيضًا على الهروب من الحويصلات داخل الخلية. 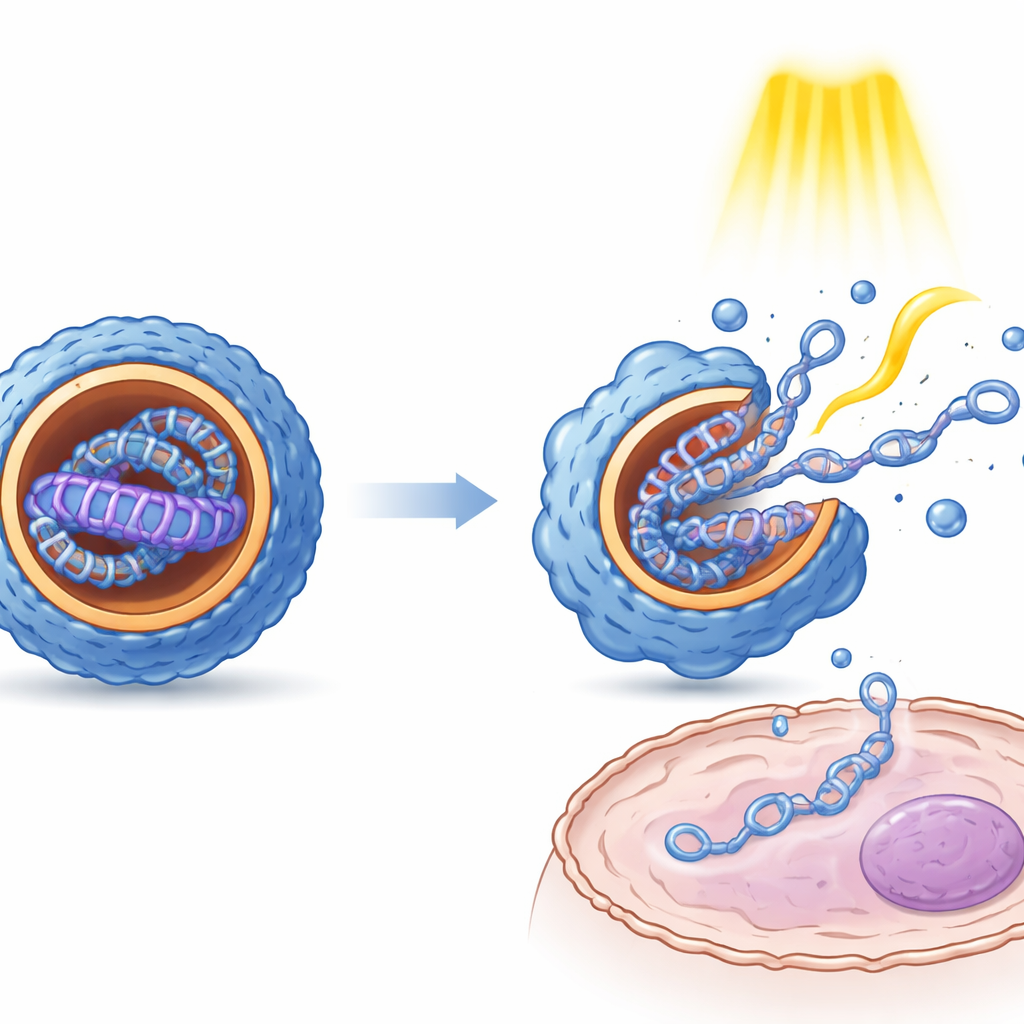
توجيه الجينات إلى أعضاء محددة
أبرز السلوكيات المفاجئة ظهرت في الفئران. عندما أُعطيت الجسيمات ذات الجسور الأكسجينية في شكلها الغني بحالة E، حدث تعبير عن جين مؤشر بشكل رئيسي في الكبد وبعضه في الرئتين. تحويلها مسبقًا إلى شكل Z قبل الحقن لم يزددِ التعبير الكلي فحسب، بل حوّل التوازن تجاه الرئتين. جسيمات الجسور الكبريتية سردت قصة مختلفة: شكلها Z فضل الطحال، وهو عضو مناعي رئيسي. وهكذا، ضمن نفس الإطار الجزيئي الأساسي — ودون تغيير الحمولة من الحمض النووي — استطاع الباحثون توجيه النشاط الجيني بشكل رئيسي إلى الكبد أو الرئتين أو الطحال ببساطة عن طريق اختيار الوصلة (أكسجين أو كبريت) والشكل المنشط بالضوء (E أو Z) للناقلة. طوال هذه الاختبارات، بقيت حيوية الخلايا مرتفعة، مما يوحي بأن النظام لطيف نسبيًا.
طريق قابل للضبط بالضوء نحو أدوية جينية مستقبلية
بعبارات يومية، بنى الفريق ناقلة صغيرة قابلة للتبديل بالضوء للحمض النووي. قبل الحقن، تُبرمج الناقلات عبر علاج ضوئي قصير إلى أحد الشكلين. يجتمع كل شكل ليكوّن جسيمات نانوية ذات حجم وإحساس سطحي مميزين، والذي بدوره يحدد مدى التصاقها بأنواع خلايا مختلفة ومكانها في الجسم. وبما أن نفس السقالة الكيميائية يمكن تعديلها بطرق صغيرة عديدة، وأن التحويل قابل للعكس ولا يغيّر الحمض النووي نفسه، فإن هذه المنصة توفر وسيلة مرنة لضبط مكان وطريقة تأثير علاجات الجينات. وبينما يبقى الكثير من العمل قبل الاستخدام السريري، تُظهر الدراسة أن ناقلات أحادية الجزيء المصممة بعناية والمتحكم بها بالضوء يمكن أن تصبح أدوات قوية لأدوية جينية أكثر أمانًا ودقة.
الاستشهاد: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
الكلمات المفتاحية: توصيل الجينات, جسيمات نانوية مستجيبة للضوء, مفاتيح الأزوبينزين, العلاج الموجَّه للحمض النووي, الطب النانوي