Clear Sky Science · ar
بروتياز S9 WprP2 يحفز قطعًا موحدًا في الببتيد السلفي في تخليق RiPP
لماذا تهم أدوات القص الصغيرة داخل الخلايا
داخل البكتيريا، تقص مقصات جزيئية متخصصة سلاسل طويلة من الأحماض الأمينية إلى قطع أصغر ونشطة غالبًا ما تصبح مضادات حيوية أو منتجات طبيعية مفيدة أخرى. تكشف هذه الدراسة عن أداة قطع مجهولة سابقة — بروتياز يُدعى WprP2 — يقص الببتيد المستهدف بدقة غير معتادة. فهم آلية عمل هذا الإنزيم قد يساعد العلماء على تصميم ببتيدات بيولوجية جديدة ومضادات حيوية من الجيل القادم.
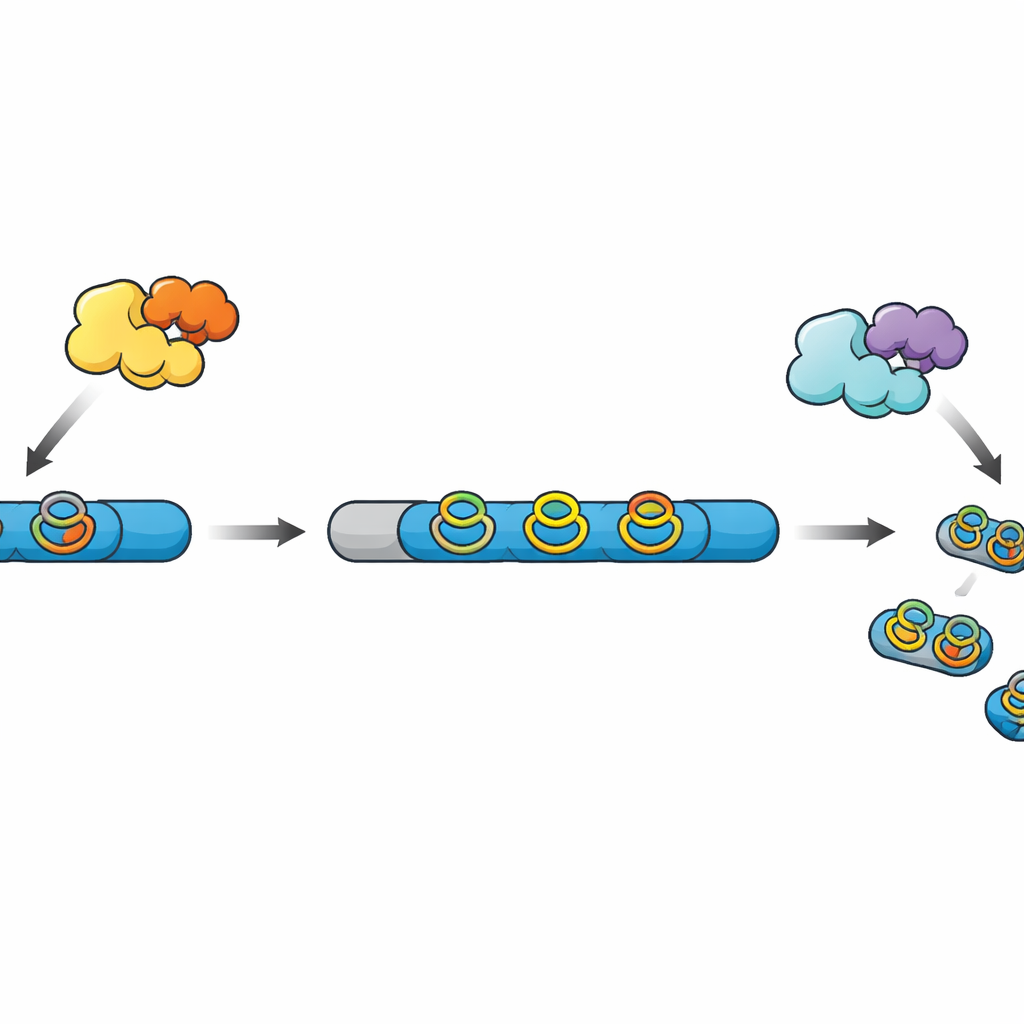
من السلاسل الخام إلى الأدوية الصغيرة المكتملة
تبدأ العديد من المنتجات الطبيعية القائمة على الببتيد، والمعروفة مجتمعة باسم RiPPs، كسلاسل بسيطة تُبنى على الريبوسوم. تحتوي هذه السلاسل على منطقة قائد تعمل كمقبض ومنطقة جوهرية ستصبح المنتج النهائي بعد سلسلة من التعديلات الكيميائية. تضيف إنزيمات أخرى وصلات عرضية وحلقات تجعل الببتيد أكثر استقرارًا ونشاطًا، وأخيرًا يقطع بروتياز الجزء القائد ويطلق الجزيء الناضج. في عائلة RiPPs المكتشفة حديثًا، تبني إنزيمات radical SAM حلقات "cyclophane" مدمجة تشمل أحماضًا أمينية عطرية، لكن في معظم مجموعات الجينات المعروفة يختفي البروتياز الملائم، مما يترك خطوات المعالجة النهائية غامضة.
تتبع شريك إنزيمي مفقود
درس المؤلفون سابقًا إنزيم radical SAM باسم WprB1 الذي ركب وصلات متطابقة عند ثلاث مقاطع WPR متكررة في الببتيد السلفي. في العمل الجديد، بحثوا في جينومات بكتيرية عن أقارب لهذا الإنزيم ونظروا بالقرب منه عن أي جينات قد ترمز لبروتياز. في Streptomyces venezuelae وجدوا مجموعة واعدة تضمنت إنزيمًا مشابهًا للتركيب العرضي، وبروتين مساعد له، وببتيدًا سلفيًا مطابقًا يحتوي على ثلاث تكرارات WPR، وبروتياز سيرين من عائلة S9 رشحوا تسميته WprP2. جعل ذلك النظام مثالًا مناسبًا لكشف كيفية قطع الببتيد أخيرًا لإطلاق الشظايا النشطة.
مراقبة قطع الببتيد
لفحص WprP2، أنتج الفريق الببتيد السلفي في بكتيريا، سواء بوجود إنزيم التركيب العرضي أو بدونه، نقّوه ثم مزجوه مع البروتياز في تفاعلات مخبرية محكومة. كشفت طيفية الكتلة أن WprP2 أولًا يقص السلسلة مباشرة بعد كل مقطع WPR، ثم يُجري قطعًا ثانيًا على مسافة ثابتة قبل بقاعدة برولين معينة أبعد في التسلسل. تخلق هاتان الخطوتان سلسلة من الشظايا الأصغر المتساوية. ومن اللافت أن WprP2 نفذ نمط القص هذا سواء كانت حلقات cyclophane قد رُكبت بالفعل أم لا، مما يظهر أن الحلقات ليست مطلوبة للتعرف. بالمقارنة مع التربسين التجاري، الذي لا يستطيع القطع في مواقع معينة مترابطة، ظل WprP2 فعالًا، مما يبرز متانته غير الاعتيادية.
فك شيفرة ما يتعرف عليه الإنزيم
بعد ذلك سأل الباحثون ما السمات التي يقرأها WprP2 في الببتيد. عن طريق تغيير الأحماض الأمينية الفردية حول مواقع القطع بشكل منهجي، وجدوا أن تغيير العديد من البقايا المجاورة كان له تأثير طفيف، لكن تغيير أرجينين رئيسي داخل مقطع WPR أو غلوتامين أو برولين عند موقع القطع الثاني قد يعيق تلك الخطوة المعينة. أظهرت تجارب بببتيد سلفي ذي بقايا محيطة مختلفة أن البروتياز لا يزال يقطع بعد تكرارات WPR لكنه لا يُجري القطع الثاني إلا بوجود زوج غلوتامين‑برولين. دعمت النماذج الهيكلية المولدة حاسوبيًا باستخدام AlphaFold3 هذه الصورة: في المجمعات المتوقعة، يصطف كل من مواقع WPR وموقع غلوتامين‑برولين بدورهما مع المركز التحفيزي للإنزيم، متسقًا مع آلية متتابعة من خطوتين.
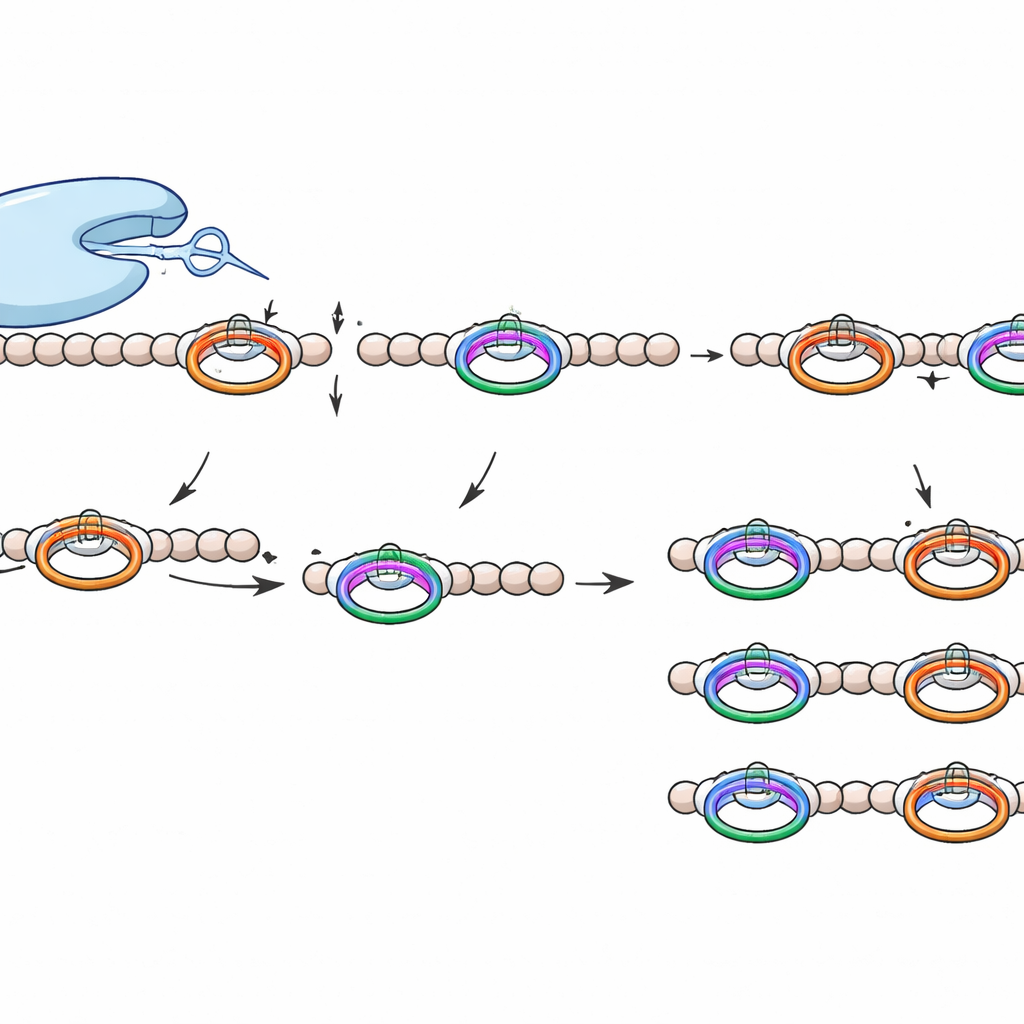
ما الذي يجعل أداة القص هذه مميزة
ينتمي WprP2 إلى عائلة أوسع من بروتيازات S9 التي تضم بالفعل إنزيمات ذات صلة طبية، لكنه يبرز بعدة نواحٍ. يقطع على الجانب N‑الطرفي من بقاعدة برولين بدلاً من بعدها، يعمل على نمط متكرر لتوليد شظايا متساوية القياس عبر السلسلة السلفية كاملة، ويظهر تسامحًا واسعًا تجاه الأحماض الأمينية الواقعة بين موقعي التعرف. هذا المزيج من الدقة والمرونة لم يُلاحظ سابقًا في بروتيازات مرتبطة بـRiPP.
كيف يمكن استخدام هذا الاكتشاف
من خلال كشف بروتياز يتعرف على إشارات تسلسلية بسيطة ويؤدي قصوصًا متكررة وموحدة، تضيف هذه الدراسة أداة قوية جديدة إلى مجموعة الأدوات المتنامية لهندسة الببتيدات. عمليًا، يمكن الاستفادة من WprP2 لإطلاق أو إعادة تشكيل ببتيدات مصمّمة، بما في ذلك تلك التي تحتوي على وصلات عرضية معقدة تقاوم الإنزيمات القياسية مثل التربسين. للمختصين غير المتخصصين، الخلاصة الرئيسية هي أن العلماء اكتشفوا نوعًا جديدًا من المقصات الجزيئية يقطع السلاسل الببتيدية الطويلة إلى قطع دقيقة ومتصاعدة الحجم متساوية، فاتحًا الباب أمام إنتاج أكثر تحكمًا لمضادات حيوية محتملة وجزيئات بيولوجية فعّالة أخرى.
الاستشهاد: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
الكلمات المفتاحية: ببتيدات RiPP, بروتياز سيرين, WprP2, منتجات طبيعية حلقيّة (cyclophane), هندسة الببتيدات