Clear Sky Science · ar
جسيمات نانوية بوليمرية ذات نواة ذهبية مغطاة بسوائل أيونية للالتحام الانتقائي بالخلايا المتعادلة نحو علاج الانتباذ البطاني الرحمي
إعادة التفكير في تخفيف مرض خفي وشائع
الانتباذ البطاني الرحمي حالة مؤلمة ينمو فيها نسيج يشبه بطانة الرحم في أماكن لا ينبغي أن يكون فيها، مما يسبب غالبًا تقلصات شديدة وألمًا مزمنًا ومشكلات في الخصوبة. تعتمد العلاجات الحالية بشكل كبير على الهرمونات أو الجراحة، والتي قد تصاحبها آثار جانبية وإجراءات متكررة ولا تضمن تخفيفًا دائمًا. تستكشف هذه الدراسة فكرة مختلفة تمامًا: جسيمات صغيرة تنشط بالضوء تلتصق بخلايا الجهاز المناعي في الجسم لتصل إلى النسيج المريض وتدمره بلطف، مما قد يوفر خيارًا غير جراحي في المستقبل قادرًا على حفظ الخصوبة وتقليل الآثار الجانبية.
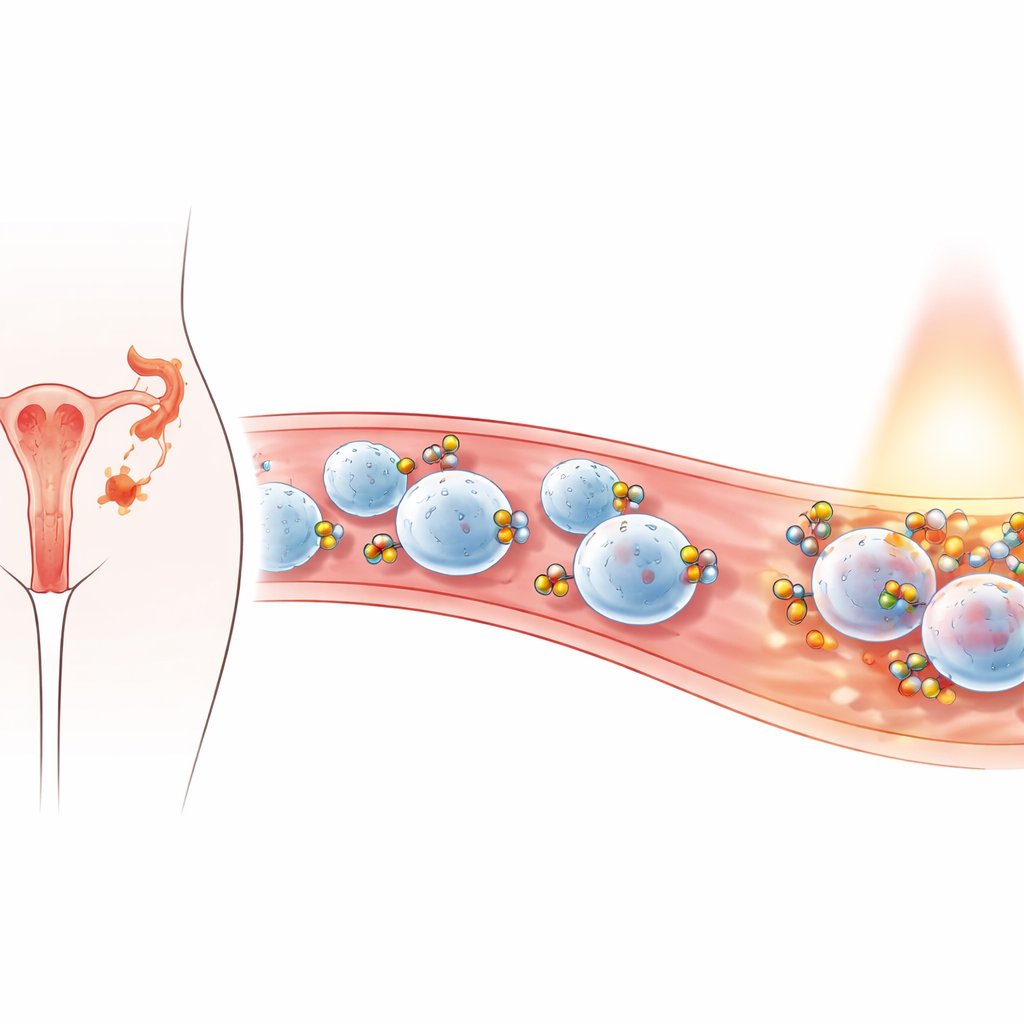
مساعدون صغار يركبون مستجيبي الجسم الأوائل
ركز الباحثون على الخلايا المُتعادلة (النيتروفيلات)، نوع من خلايا الدم البيضاء التي تتجه سريعًا إلى مواقع الالتهاب، بما في ذلك آفات الانتباذ البطاني الرحمي. تكمن استراتيجيتهم في "الالتحام" بهذه الخلايا عن طريق طلاء الجسيمات النانوية بحيث تلتقطها الخلايا المتعادلة طبيعيًا أو تحملها على سطحها. عندما تنتقل هذه الخلايا إلى النسيج الرحمي الملتهب، تجلب معها الجسيمات النانوية، مركزة العلاج في المكان المطلوب مع تجنب الأنسجة السليمة. والأهم أن حركة الخلايا المتعادلة في الأنسجة الحوضية السليمة تكون عادة منخفضة لمعظم أجزاء الدورة الشهرية، مما قد يساعد على تركيز العلاج في مواقع المرض بدلًا من النسيج الطبيعي.
بناء جسيمات ذكية تستجيب للضوء
لتحقيق هذا النظام، بنى الفريق جسيمات بثلاثة مكونات رئيسية. في القلب ذهب، اختير لقدرته على امتصاص الضوء قرب الأشعة تحت الحمراء وتحويله إلى حرارة بطريقة مسيطرة. حول النواة أضافوا غلافًا من بلاستيك حيوي قابل للتحلل يُدعى PLGA، شائع الاستخدام في الغرسات الطبية وتوصيل الدواء. أخيرًا، غطوا هذا الغلاف بـ "سوائل أيونية" خاصة — جزيئات مالحة تشبه الزيوت تبقى سائلة عند درجات حرارة منخفضة نسبيًا. من خلال اختيار السوائل الأيونية بعناية، تمكنوا من ضبط كيفية تفاعل الجسيمات مع خلايا الدم، وبالأخص الخلايا المتعادلة. أكدت المجهرات وقياسات الحجم أن الجسيمات شكلت بنية نواة–غلاف مرتبة، وأظهرت الاختبارات البصرية أن الطلاءات حوّلت امتصاص الضوء للجسيمات بطريقة حسّنت أدائها الحراري.
تسخين الخلايا المريضة دون أدوية قاسية
بعد الوصول إلى تصميم مستقر للجسيمات، اختبر الفريق مدى فاعلية هذه المسخنات النانوية على خلايا بطانة الرحم البشرية في المختبر. عند تسليط الضوء بالقرب من الأشعة تحت الحمراء على المحاليل الحاوية على الجسيمات — مماثلة لما قد يوفره ليزر طبي — ارتفعت درجة الحرارة بضعة درجات فقط إجمالًا، ومع ذلك كان ذلك كافيًا لإتلاف الخلايا المجاورة. والأهم أنه من دون ضوء كانت الجسيمات آمنة إلى حد كبير: بقيت خلايا بطانة الرحم المعرضة لها أكثر من 80% حية عبر مجموعة واسعة من الجرعات. تحت التعرض الضوئي، خضعت الخلايا في الغالب للموت المبرمج (الاستماتة)، وهو شكل مرتب من موت الخلايا، بدلًا من النخر الذي قد يحفز الالتهاب. أظهرت الاختبارات الإضافية أدلة قليلة على تلف الحمض النووي ولا إطلاقًا قابلاً للقياس من جزيئات الإشارة الالتهابية من الخلايا المعالجة.
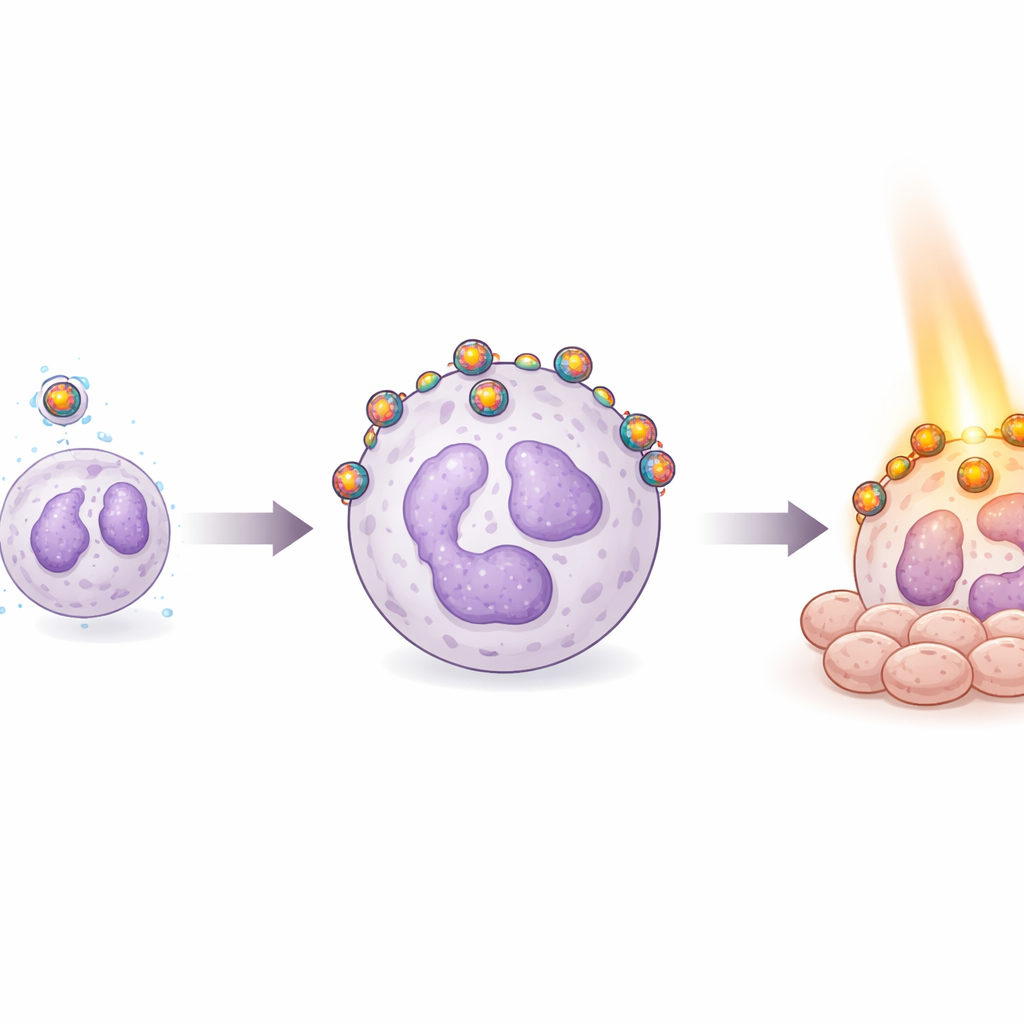
إثبات السلامة في الدم وتتبع رحلة الجسيمات
السلامة في مجرى الدم ضرورية لأي علاج وريدِي. عرض الفريق خلايا الدم الحمراء البشرية للجسيمات ووجدوا عمليًا عدم حدوث انحلال للدم — التحطم المدمّر للخلايا الحمراء الذي قد يسبب مضاعفات خطيرة — مما يوحي بأن الجسيمات لطيفة على الدم. ثم أضافوا صبغة فلورية إلى الجسيمات وخلطوها مع عينات دم بشرية لتتبع الخلايا التي تفضلها الجسيمات. بالمقارنة مع الجسيمات غير المغطاة، أظهرت النسخ المغطاة بالسوائل الأيونية ارتباطًا أقوى بكثير بالخلايا المتعادلة. شجعت بعض الطلاءات الخلايا المتعادلة على ابتلاع الجسيمات، بينما جعلت طلاءات أخرى الجسيمات تلتصق بسطح الخلية كأنها حبات على بالون من الخارج. كلا نمطي الارتباط زادا كمية الذهب المكتشفة في الخلايا المتعادلة، مؤكدة أن الطلاءات توجه الجسيمات النانوية نحو ناقلي الالتهاب الطبيعي في الجسم.
ماذا قد يعني هذا للعلاج في المستقبل
بشكل عام، تقدم الدراسة نوعًا جديدًا من الجسيمات "الذكية" المصممة للالتحام بالخلايا المتعادلة، والدوران بأمان في الدم، وعند التنشيط بضوء ليزري لطيف، تسخين وقتل خلايا بطانة الرحم بشكل أساسي عبر مسارات مبرمجة للانتحار الخلوي. وبينما أُجريت هذه التجارب على خلايا وعينات دم بدلاً من مرضى أحياء، تشير النتائج إلى مستقبل يمكن فيه علاج آفات الانتباذ البطاني الرحمي من داخل الجسم دون جراحة كبرى أو استخدام مكثف للهرمونات. من خلال الجمع بين التوصيل الموجه والتسخين الضوئي الدقيق، قد يوفر هذا النهج يومًا راحة أطول أمداً، آثارًا جانبية أقل، وحفظًا أفضل للخصوبة للأشخاص الذين يعيشون مع الانتباذ البطاني الرحمي.
الاستشهاد: Vashisth, P., Clerc, L.T.D., Hu, D. et al. Ionic liquid-coated gold core polymeric nanoparticles for selective neutrophil hitchhiking towards endometriosis treatment. Commun Chem 9, 119 (2026). https://doi.org/10.1038/s42004-026-01909-8
الكلمات المفتاحية: الانتباذ البطاني الرحمي, جسيمات نانوية, العلاج بالتسخين الضوئي, الخلايا المتعادلة, توصيل الدواء الموجه