Clear Sky Science · ar
متغيرات PI3Kα المسببة للسرطان تكشف عن طيف تَشَكُّل تدريجي مع جيوب خفية خاصة بالطفرة
عندما لا تكفي تغيير واحد في الحمض النووي
غالبًا ما يُوصف السرطان بأنه مرض الطفرات، لكن هذه الدراسة تُظهر أن ليس كل الطفرات تعمل بمفردها. فحص الباحثون إنزيمًا رئيسيًا يتحكم في النمو، PI3Kα، ووجدوا أنه عندما يحدث تغييران محددان في الحمض النووي معًا في نفس نسخة الجين، يمكن أن يدفعا هذا البروتين إلى أشكال أكثر نشاطًا مما يسببه أي تغيير بمفرده. وهذا مهم لأن فرط نشاط PI3Kα لا يدفع السرطانات فحسب، بل يشارك أيضًا في متلازمات فرط النمو الحميدة واضطرابات تطور الدماغ—كما يساعد في تفسير سبب استجابة بعض الأورام بشكل ضعيف للأدوية الحالية.
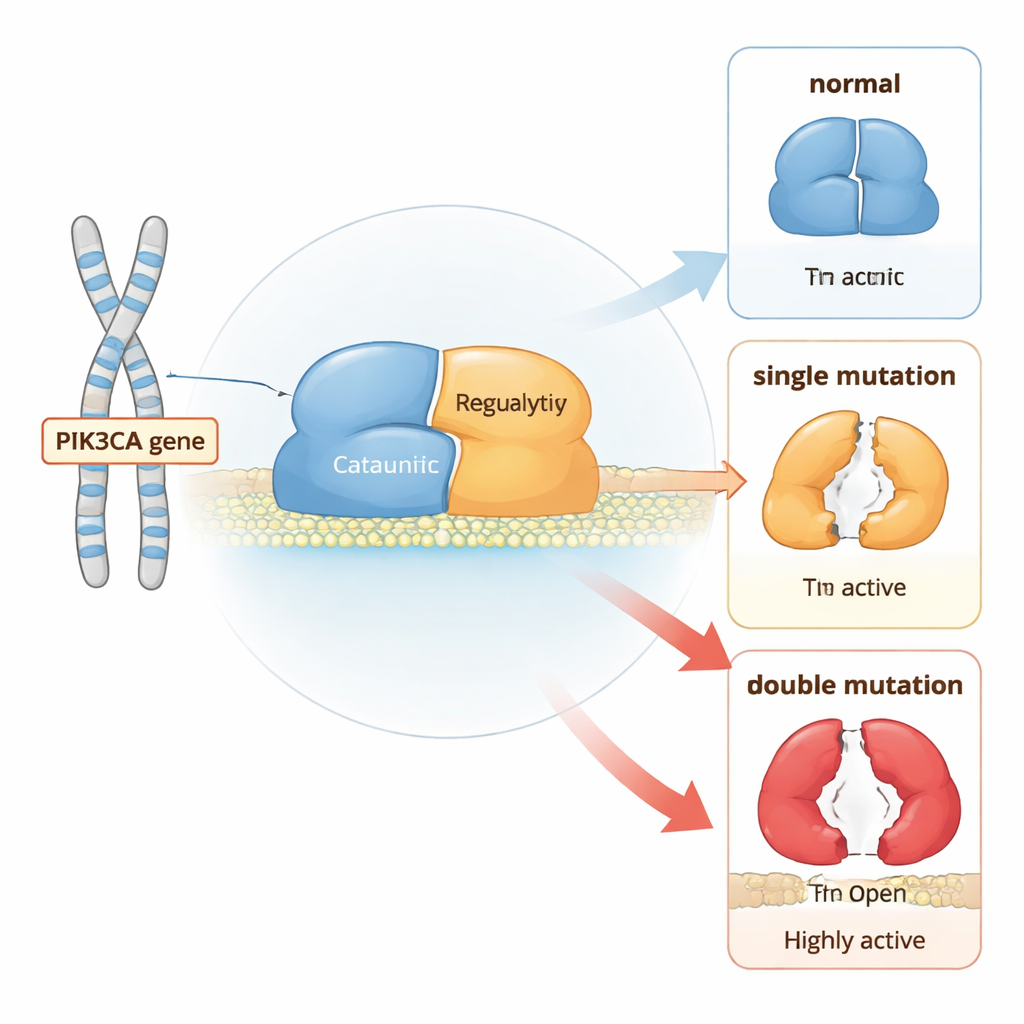
مفتاح جزيئي لنمو الخلايا
PI3Kα بروتين مكوّن من جزأين يجلس قرب غشاء الخلية وينقل إشارات النمو. في الظروف الطبيعية يبقى في الغالب في وضع "إيقاف" حتى تُنَشَّط المستقبلات على سطح الخلية. ثم يتحرك PI3Kα إلى الغشاء ويحوّل ليبيدًا يُسمى PIP2 إلى PIP3، الذي يأمر الخلية بالنمو والانقسام. ولمنع النمو المفرط، تعمل عدة أجزاء من البروتين كفرامل مدمجة: منطقة تُقيد النواة التحفيزية، وأخرى تبقي حلقة التفعيل المرنة قريبة، ووحدة شريكة تساعد في كبح كل المجمع.
كيف تميل الطفرات المفردة والمزدوجة التوازن
باستخدام محاكاة حاسوبية طويلة على مستوى الذرات، قارن المؤلفون PI3Kα الطبيعي بنسخ تحمل إما طفرات سرطانية "نقطة ساخنة" مفردة أو تركيبات من نقطة ساخنة مع طفرة أضعف في نفس الجزيء. وجدوا أن كل طفرة تغير تواتر زيارة البروتين لأشكال أكثر انفتاحًا ونشاطًا، لكن الطفرات المزدوجة تدفع التوازن أبعد بكثير من الطفرات الفردية. وعلى وجه الخصوص، تعمل أزواج معينة من الطفرات معًا على إرخاء الاتصالات التي تبقي قطعة تنظيمية (تُسمى nSH2) ثابتة في مكانها وتحريك قطعة أخرى (iSH2) بعيدًا عن موضعها. هذا التحرك المنسق يفك قفل النواة التحفيزية، مما يجعل من الأسهل أن ينتقل البروتين إلى الغشاء ويبدأ الإشارة.
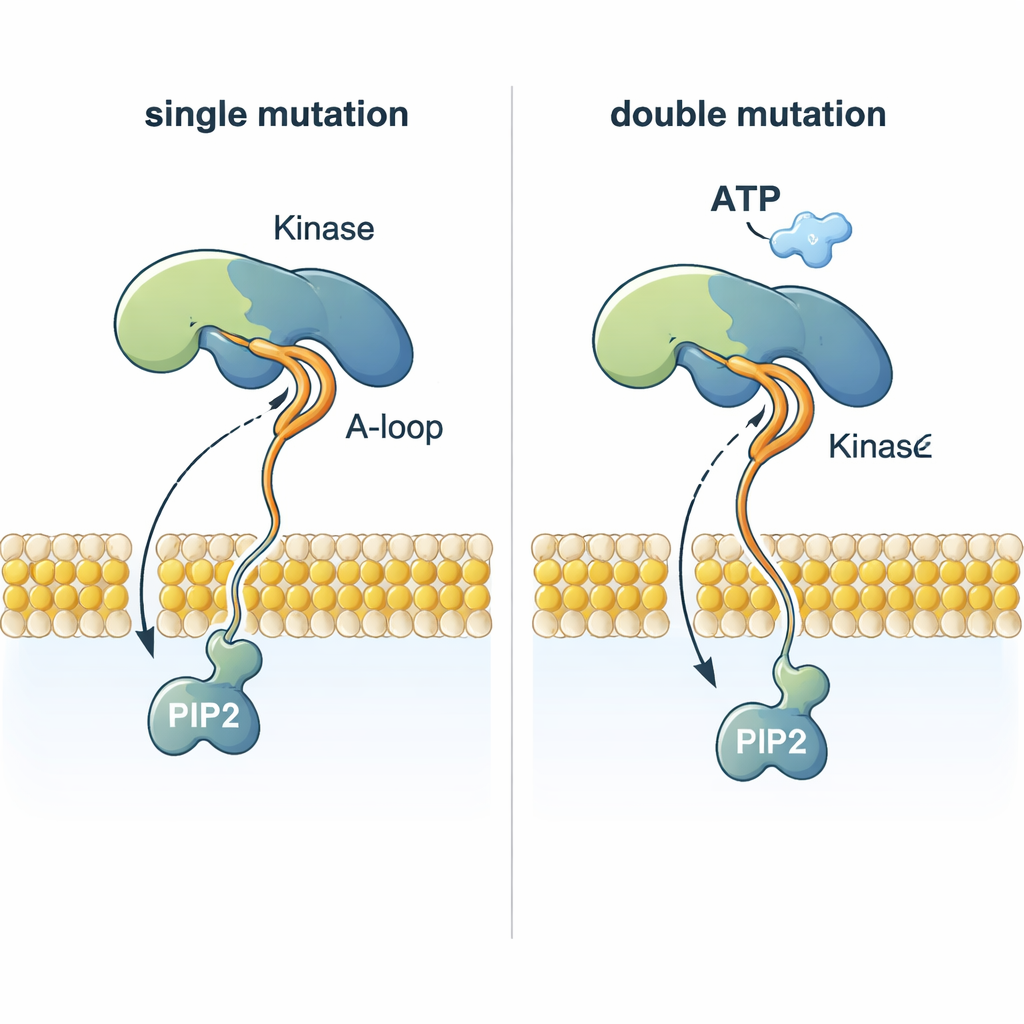
مساعدة الركيزة على الوصول إلى موقع التفاعل
لغز لافت هو كيف يستطيع PI3Kα إضافة مجموعة فوسفات من ATP—الواقعة على بعد يقارب 2 نانومتر فوق الغشاء—إلى PIP2 المدمج في الغشاء. تُظهر المحاكاة أن طفرات معينة تُعيد تشكيل حلقة التفعيل المرنة بحيث يبرز جزء محمل بشحنة موجبة عالية نحو الغشاء. يمكن لهذه الحلقة أن تمسك بالرأس السالب الشحنة لـ PIP2، تخرجه من طبقة الدهون، وتوجهه صعودًا نحو ATP. الطفرات المزدوجة التي تجمع طفرة تربط البروتين بالغشاء مع أخرى تغير هذه الحلقة تنسق PIP2 بكفاءة أعلى بكثير من PI3Kα الطبيعي أو الطفرات المفردة، مما يقدم تفسيرًا بنيويًا لسبب كون الأورام التي تحمل طفرتين في PI3Kα أكثر عدوانية أحيانًا.
مواقع دوائية خفية تكشفها الحركة
بما أن PI3Kα كبير ومرن، فإن دواءً واحدًا يستهدف موقعه النشط غالبًا ما يكافح ليؤثر عبر كل الأشكال الطافرة وقد يسبب آثارًا جانبية مثل تغيّرات شديدة في سكر الدم. من خلال تتبُّع كيف يتنفس البروتين ويتلوى بمرور الزمن، اكتشف الباحثون "جيوبًا خفية"—أخاديد مؤقتة تنفتح فقط في أشكال طافرة معينة وتكون غير مرئية في هياكل البلورة الساكنة. تظهر هذه الجيوب في مواقع خاصة بالطفرات، على سبيل المثال قرب مناطق تتحرك بقوة في طفرات مزدوجة معينة. هذا يوحي بأن مثبطات كلوسطرية مصممة بعناية، والتي تُحْكِم ارتباطها بعيدًا عن الموقع النشط، قد تُفَصَّل لإقفال المتغيرات الطافرة الفردية مرة أخرى في حالات أقل نشاطًا وأكثر أمانًا.
نحو علاجات تركيبيّة أذكى
بشكل عام، يدعم العمل رؤية "الضربة المزدوجة" في علم وراثة السرطان: طفرة قوية في نقطة ساخنة مع شريك أضعف في نفس جزيء PI3Kα يمكن أن تخلق طيفًا تدريجيًا من الأشكال الأكثر نشاطًا، والتي غالبًا ما ترتبط بنتائج سريرية أشد. بالنسبة للعلاج، يجادل المؤلفون بأنه بدل الاعتماد على مثبط وحيد قد يكون أكثر فاعلية الجمع بين أدوية تستهدف جيوبًا مختلفة—واحدة في الموقع النشط وواحدة أو أكثر من المواقع الكلوسطرية التي تظهر فقط في طفرات محددة. مثل هذه الخلطات قد تقلل نشاط PI3Kα بدقة أكبر، وتخفف الآثار السامة، وتطابق العلاج بشكل أفضل مع نمط الطفرات الموجود في ورم المريض.
الاستشهاد: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
الكلمات المفتاحية: PI3K ألفا, طفرات ممرِضة, مثبطات كلوسطرية, ديناميكيات جزيئية, نقل الإشارة