Clear Sky Science · ar
تطوير نموذج نانوي من نقاط كربون مرتبط رباعيًا للعلاج المستهدف للغليوما
أمل جديد لأورام الدماغ العنيدة
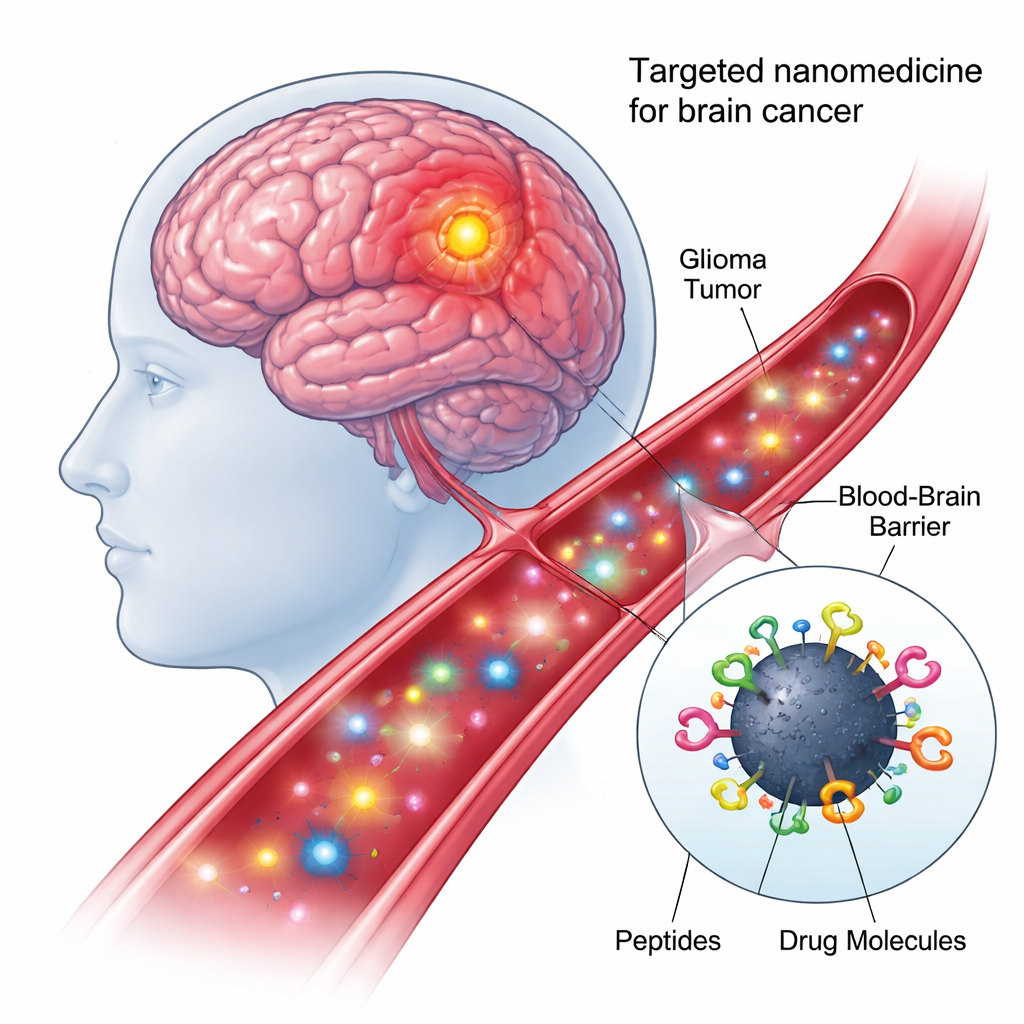
تُعد الأورام الدماغية عالية الدرجة مثل الغلوبلاستوما من أصعب السرطانات علاجًا. العديد من الأدوية الفعالة في أجزاء أخرى من الجسم إما لا تستطيع عبور الحاجز الدموي الدماغي أو تتلف الأنسجة السليمة أثناء تنقلها. تصف هذه الدراسة جسيمًا نانويًا «ذكيًا» صُنِع في المختبر يهدف إلى التسلل بدقة أكبر إلى أورام الدماغ، وحمل خليط دوائي قوي، وإطلاقه مباشرة داخل أنوية خلايا الورم حيث يمكن أن يسبب أكبر قدر من الضرر للخلايا السرطانية مع حفظ الخلايا الطبيعية إلى حدٍّ أكبر.
شاحنة توصيل صغيرة مصنوعة من الكربون
في صلب النهج الجديد تقف نقاط الكربون—جسيمات بحجم نانومتر مصنوعة من الكربون، رخيصة الإنتاج، قابلة للخليط مع الماء، وتتلألأ تحت أنواع معينة من الضوء. وبما أن أسطحها غنية بروابط كيميائية يمكن تفعيلها، فيمكن تزيينها بمكونات حيوية متعددة في آن واحد. في هذا العمل، أنشأ الباحثون نموذجًا نانويًا «مرتبطًا رباعيًا»: ارتبطت كل نقطة كربون كيميائيًا، في تفاعل أحادي الطور، بببتيدين مستهدفتين ومادتين مضادتين للسرطان. يحول هذا التصميم النمطي كل نقطة إلى شاحنة توصيل صغيرة قادرة على التعرف على خلايا الورم، واجتياز الحواجز الخلوية، وحمل الأدوية إلى العنوان الخلوي الصحيح.
العثور على الخلايا الدماغية الصحيحة ودخولها
الببتيد الأول على الجسيم النانوي، المسمى shPep-1، مصمم للتعرف على مستقبل يدعى IL13Rα2. يوجد هذا المستقبل بمستويات مرتفعة على العديد من الأورام الدماغية العدوانية—بما في ذلك غلوبلاستوما الكبار والأطفال وغلومومات الجسر الباطن المنتشرة—بينما يظهر بكمية ضعيفة فقط على الخلايا الدماغية الطبيعية. عبر ارتباطه بـ IL13Rα2، يساعد shPep-1 نقاط الكربون على الوصول إلى خلايا الورم والدخول إليها عن طريق الامتصاص المعتمد على المستقبل. الببتيد الثاني الأطول، lnPep-1، يحتوي على إشارة توطين نووي: تسلسل قصير يساعد الحمولة على عبور الغشاء النووي والوصول إلى مركز تحكم الخلية حيث يُخزن الـDNA. معًا، تمنح هذان الببتيدان الجسيم النانوي تفضيلًا للورم والقدرة على الوصول إلى النواة بعد الدخول.
تسليم هجوم دوائي منسق
تتألف الحمولة العلاجية من جزيئين صغيرين. الأول هو الإبيروبسين، دواء كيماوي معروف يقتل الخلايا السرطانية عبر إدخال نفسه في الـDNA ومنع إنزيمات ضرورية لإصلاح الكسور الثنائية الشريط. الثاني هو ناتج أيضي يُسمى 5-أمينوأيميدازول-4-كربوكسايد (AIC)، يتكوّن من دواء ورم دماغي تيموزولوميد عند الرقم الهيدروجيني الفيزيولوجي. في عمل سابق، أظهرت نفس المجموعة أن الجمع بين الإبيروبسين وAIC على نقطة كربون عزز قتل الخلايا السرطانية مقارنة بكل دواء على حدة. في التصميم الجديد، يُنقل كلاهما معًا على الجسيم النانوي ذي الببتيدين المزدوجين، مستهدفين تأثيرًا تآزريًا مباشرة في نواة خلية الورم.
قوي في خلايا الورم وألطف على الخلايا الطبيعية
لاختبار فعالية النموذج النانوي، تعرض الفريق لعدة سلالات خلايا غليوما عالية الدرجة—غلوبلاستوما البالغين، غلوبلاستوما الأطفال، ونموذج غليوما جذعية جسرية منتشرة—لنقاط الكربون المرتبطة رباعيًا. حتى عند تركيزات منخفضة جدًا (بحدٍّ أدنى 50 نانومولار)، انخفضت قابلية بقاء خلايا الورم إلى نحو نصف الضوابط غير المعالجة، وعند جرعات أعلى قضت جميع الروابط المختبرة على معظم خلايا الورم. والأهم أن النموذج الرباعي تفوق على النسخ الأبسط «ذات الببتيد الواحد»، رغم احتوائه على كمّ أقل من الإبيروبسين إجمالًا. عند اختباره على خلايا عضلية ملساء وعائية غير سرطانية، كان سمّيّته أقل بكثير: إذ كانت هذه الخلايا تحتاج نحو 25–40 ضعف كمية الجسيمات النانوية لرؤية فقد مماثل في البقاء، مما يشير إلى نافذة سلامة مفيدة مدفوعة بالاستهداف الورمي بدل الجرعات القاسية.
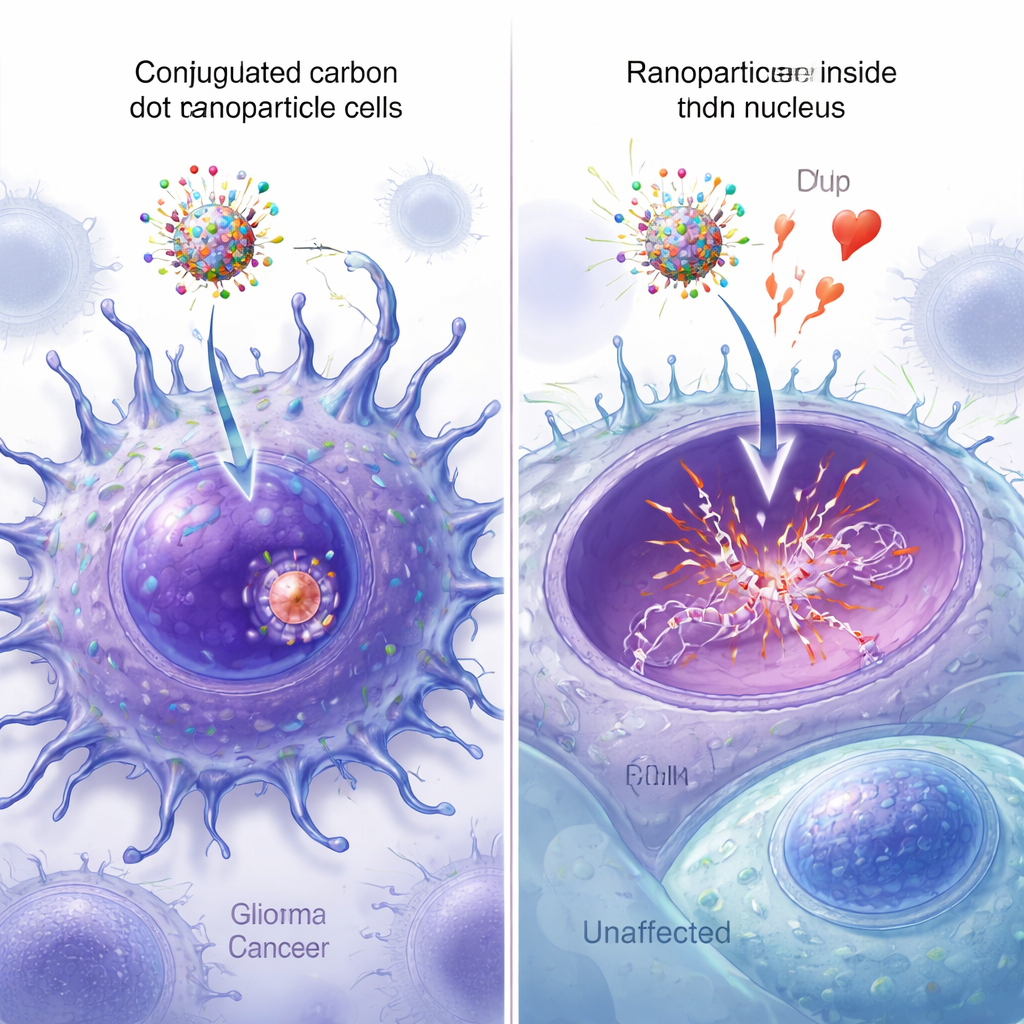
ملاحظة وصول الجسيمات النانوية إلى النواة
سمحت النسخ الفلورية من الجسيمات النانوية للباحثين بمراقبة مدى دخول كل تصميم إلى الخلايا ووصوله إلى النواة. تحت المجهر، أظهرت نقاط الكربون المجهزة بالببتيدين إشارات أضواء أكثر بريقًا منتشرة عبر خلايا السرطان، مع تراكب قوي بين الفلورسنس الأخضر للجسيم والنقش النووي الأزرق. أكدت تحليلات الصور الكمية أن الجسيمات ذات الببتيدين المزدوجين كانت لها أعلى تزامن موضعي نووي، متجاوزةً بشكل كبير جسيمات تحمل ببتيدًا واحدًا أو لا تحمل أيًا. وأكدت قياسات مطيافية الكتلة والمطيافية وقوة الذرة المجهرية أن المكوّنات الأربعة رُبطت بنجاح بنقاط الكربون وزادت حجمها بشكل طفيف، دون تعطيل وظيفة ربط الـDNA الأساسية للإبيروبسين.
ماذا قد يعني هذا لرعاية سرطانات الدماغ المستقبلية
بالنسبة للمرضى، لا تزال هذه النتائج عرضًا مبكرًا في أطباق الخلايا وليست علاجًا جاهزًا بعد. ومع ذلك، فإنها تعرض مفهومًا واعدًا: جسيم نانوي صغير ومستقر وسهل الصنع نسبيًا قائم على الكربون يمكن تخصيصه بسرعة بببتيدات استهداف وتركيبات دوائية. عبر توجيه الأدوية تحديدًا إلى خلايا الورم التي تفرط في إنتاج IL13Rα2 وتركيزها في النواة، قد تتيح مثل هذه الأدوية النانوية يومًا ما جرعات أقل، آثار جانبية أقل، واستراتيجيات علاج أكثر تخصيصًا للأورام الدماغية شديدة الفتك مثل الغلوبلاستوما والغلومومات الجسرية المنتشرة.
الاستشهاد: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
الكلمات المفتاحية: الغلوبلاستوما, الطب النانوي, نقاط الكربون, توصيل الدواء المستهدف, أورام الدماغ