Clear Sky Science · ar
ضبط AlphaFold بدقة باستخدام ملاحظات cryo-EM المحدودة
لماذا من الصعب رؤية أشكال البروتينات
البروتينات آلات جزيئية صغيرة تُحرّك تقريباً كل عملية في أجسامنا، من إنتاج الطاقة إلى نقل الإشارات العصبية. لفهم كيف تعمل—وكيف يمكن للأدوية أن تتحكم فيها—يحتاج العلماء إلى معرفة أشكالها الثلاثية الأبعاد بدقة. ظهرت أداتان قويتان لهذه المهمة: الميكروسكوب الإلكتروني بالتبريد (cryo‑EM)، الذي يلتقط العديد من اللقطات الضبابية للبروتينات المجمدة، وAlphaFold، نظام ذكاء اصطناعي يتنبأ بهياكل البروتين من تسلسلاتها. لكن في العديد من التجارب الواقعية تكون بيانات cryo‑EM ناقصة، وتنبؤات AlphaFold لا تتطابق دائماً مع الواقع. تقدم هذه الورقة طريقةٍ جديدة اسمها CoCoFold تُعلّم AlphaFold أن يستمع مباشرة إلى بيانات cryo‑EM الصعبة ويحسّن تنبؤاته وفقاً لذلك.
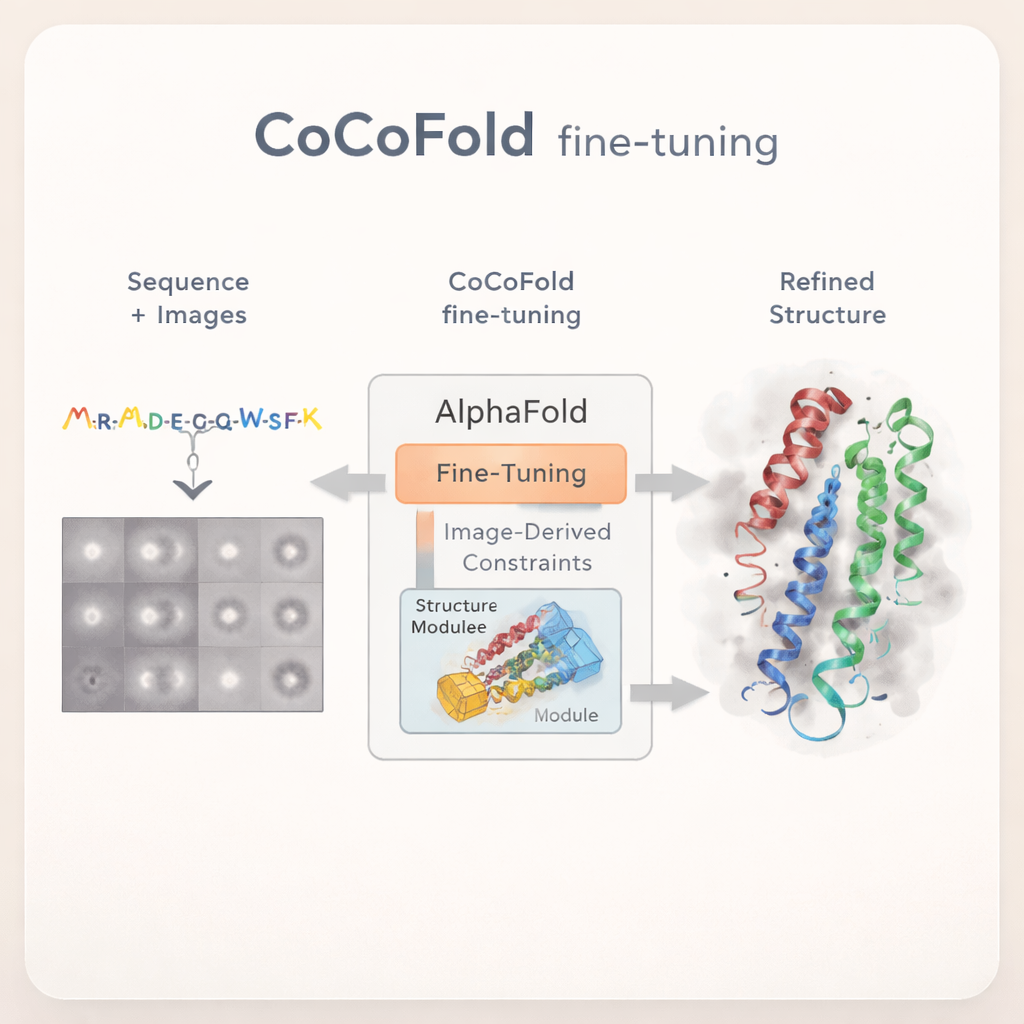
عندما ترى الكاميرا القليل جداً
تعمل cryo‑EM بتجميد البروتينات بسرعة وتصوير أعداد هائلة من الجزيئات الفردية من زوايا متعددة، ثم جمع تلك الصور في خريطة ثلاثية الأبعاد. في الممارسة العملية، ومع ذلك، غالباً لا يحصل الباحثون على عدد كافٍ من الصور الجيدة. أحياناً يظهر البروتين لفترة وجيزة فقط في حالة طاقة عالية، فيُلتقط عدد قليل جداً من الجسيمات. وفي حالات أخرى، تفضّل البروتينات أوضاعاً معينة على سطح الجليد، فيختفي الكثير من زوايا المشاهدة. كلا المشكلتين تُؤديان إلى خرائط ضبابية وغير مكتملة يصعب تحويلها إلى نماذج ذرية موثوقة. يمكن للبرمجيات الحالية أن تضبط الهياكل المتوقعة بواسطة AlphaFold داخل مثل هذه الخرائط، لكن نجاحها يعتمد بشدة على توفر بيانات حادة وعالية الدقة في البداية.
تدريس AlphaFold للتعلّم من الصور الأولية
يتبع CoCoFold نهجاً مختلفاً: بدلاً من الاعتماد على خريطة cryo‑EM ثلاثية الأبعاد مُعاد بناؤها بالكامل، يستخدم مباشرة صور الجسيمات ثنائية الأبعاد الأولية لضبط AlphaFold بدقة. تبدأ الطريقة من تنبؤ AlphaFold‑Multimer وتحافظ على تجميد معظم الشبكة الأصلية، محافظاً على معرفتها الواسعة بطي البروتينات. يُسمح فقط لجزء بناء الهيكل النهائي بأن يتغير. يُضاف "مُكيّف" خفيف الوزن لتغذية معلومات مستمدة من صور cryo‑EM إلى وحدة البناء هذه، مما يدفع النموذج بلطف نحو أشكال متوافقة مع البيانات التجريبية مع تجنّب انحرافات كبيرة عن فيزياء البروتين المعروفة.
تحويل الصور إلى ملاحظات بنيوية
لربط ذرات البروتين الفردية بالصور الميكروسكوبية المليئة بالضوضاء، يبني CoCoFold صورة ناعمة ومرنة للبنية المتوقعة باستخدام كتل ثلاثية الأبعاد متداخلة، تُعرف بخليط غاوسي. من هذا التمثيل يُحاكي كيف سيبدو البروتين في الميكروسكوب لنفس اتجاهات العرض وظروف التصوير الموجودة في التجربة الحقيقية. ثم تُقارن هذه اللقطات المحاكاة بالجسيمات الفعلية من cryo‑EM، حلقة بحلقة في نطاق الترددات، لمعرفة مدى تطابقها. أي عدم تطابق يتحول إلى إشارة تغذية راجعة تتدفق عبر الشبكة، معدّلة قليلاً كلاً من نموذج البروتين وتمثيل الكثافة. بعد التدريب، يتم تنظيف النموذج الذري أكثر بخطوة تنعيم تعتمد على مبادئ فيزيائية لإزالة التضارب الهندسي المحلي.
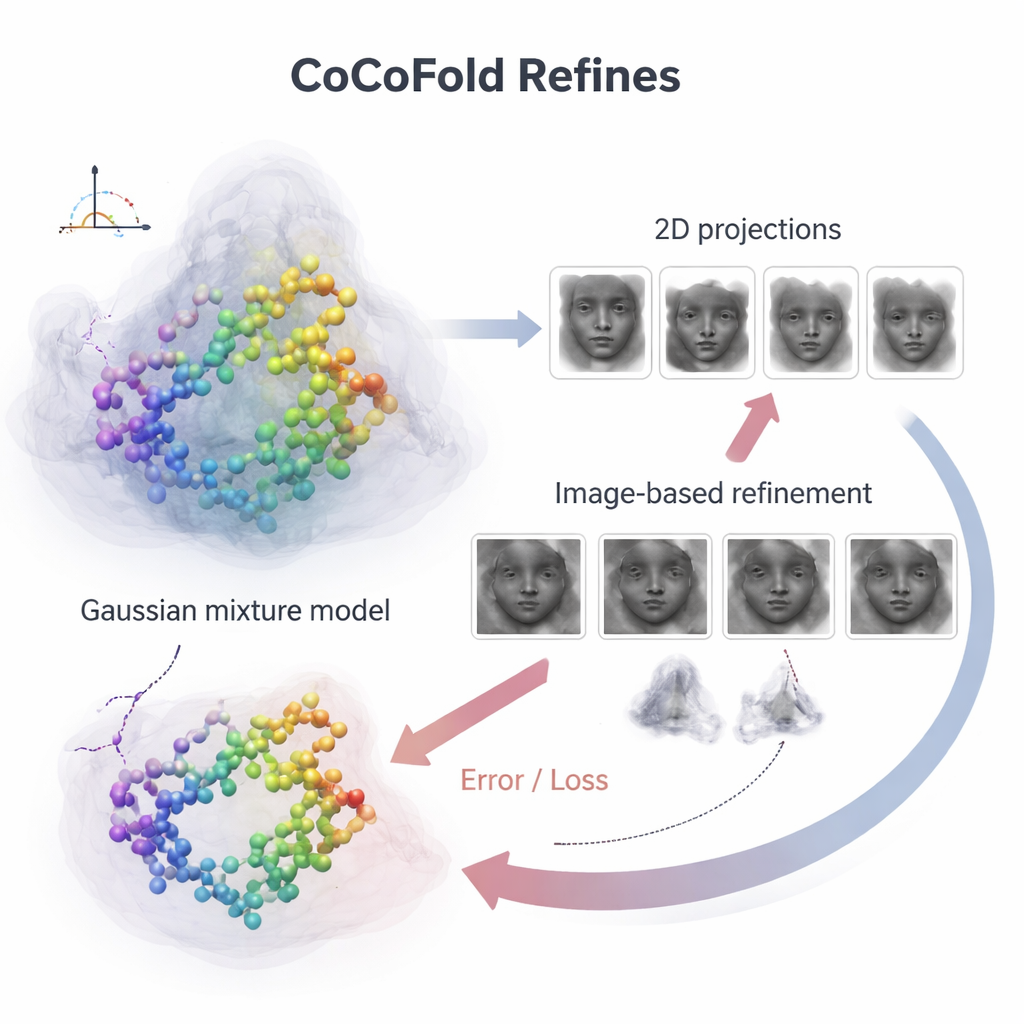
الحفاظ على الدقة عندما تكون البيانات قليلة أو متحيزة
اختبر الباحثون CoCoFold على عدة مجموعات بيانات تجريبية ومحاكاة صُممت لمحاكاة المشكلتين الرئيسيتين في cryo‑EM: قلة الجسيمات ووجود فراغات كبيرة في زوايا المشاهدة. تحت هذه الظروف الصعبة، كانت الأدوات القياسية—بما في ذلك طرق تعلم عميق أخرى تعتمد على الخرائط المُعاد بناؤها—تميل إلى فقدان مناطق من البروتين، أو وضع الحلزونات في أماكن خاطئة، أو فقدان التفاصيل الدقيقة مع تزايد ضبابية الخرائط. بالمقارنة، أنتج CoCoFold نماذج تطابقت بصورة أقرب وأكثر تكاملاً مع الهياكل المرجعية المعروفة. بقيت أخطاؤه صغيرة حتى عندما انخفض عدد الجسيمات بشكل كبير أو عندما اختفت مخاريط واسعة من اتجاهات العرض، مما يوحي بأن التعلم المباشر من الصور الأولية يحافظ على معلومات حاسمة تتجاهلها الأساليب المعتمدة على الخرائط.
ماذا يعني هذا لمستقبل علم الأحياء البنيوي
للغير متخصصين، الرسالة الأساسية هي أن CoCoFold يعمل كمترجم بين توقعات الذكاء الاصطناعي القوية والبيانات التجريبية غير الكاملة. بدلاً من الوثوق بـ AlphaFold أو cryo‑EM كلٍ على حدة، يسمح للطرفين بإفادة بعضهما البعض، خصوصاً في الحالات الصعبة حيث توفر التجارب رؤية جزئية فقط. في الحالات المباشرة التي تتوفر فيها بيانات وفيرة وعالية الجودة، لا تزال الأدوات القائمة المعتمدة على الخرائط تعمل بشكل ممتاز. لكن عندما تكون الجسيمات نادرة أو تكون الأوضاع مفقودة—وهي حالات شائعة عند تتبّع حالات البروتين العابرة أو الهشة—يوفّر CoCoFold طريقة لاستعادة نماذج ذرية موثوقة من معلومات كانت ستُهدر لولا ذلك.
الاستشهاد: Liao, J., Zheng, D., Zhang, H. et al. Fine-tuning AlphaFold with limited cryo-EM observations. Commun Chem 9, 95 (2026). https://doi.org/10.1038/s42004-026-01899-7
الكلمات المفتاحية: cryo-EM, AlphaFold, بنية البروتين, التعلّم العميق, علم الأحياء البنيوي