Clear Sky Science · ar
أول بنية بلورية لتركيب يتكوّن عند تفاعل مركب فاناديوم مع ترانسفيرين مصل الإنسان
لماذا يهم بروتين الدم ودواء معدني
تحتوي العديد من الأدوية التجريبية على ذرات معادن يمكن أن تساعد في علاج أمراض تتراوح من السكري إلى السرطان. لكن بمجرد دخول هذه الأدوية المعدنية إلى مجرى الدم، يتعين عليها أن تستقل بروتينات النقل الطبيعية في الجسم. تدرس هذه الدراسة كيفية تفاعل أحد هذه البروتينات، ترانسفيرين مصل الإنسان—الناقِل الرئيسي للحديد في دمنا—مع مركب فاناديوم واعد، مما يضيء كيف تُنقل الأدوية المعدنية عبر الجسم وكيف يمكن تعديلها لتصبح أكثر أماناً وفعالية.
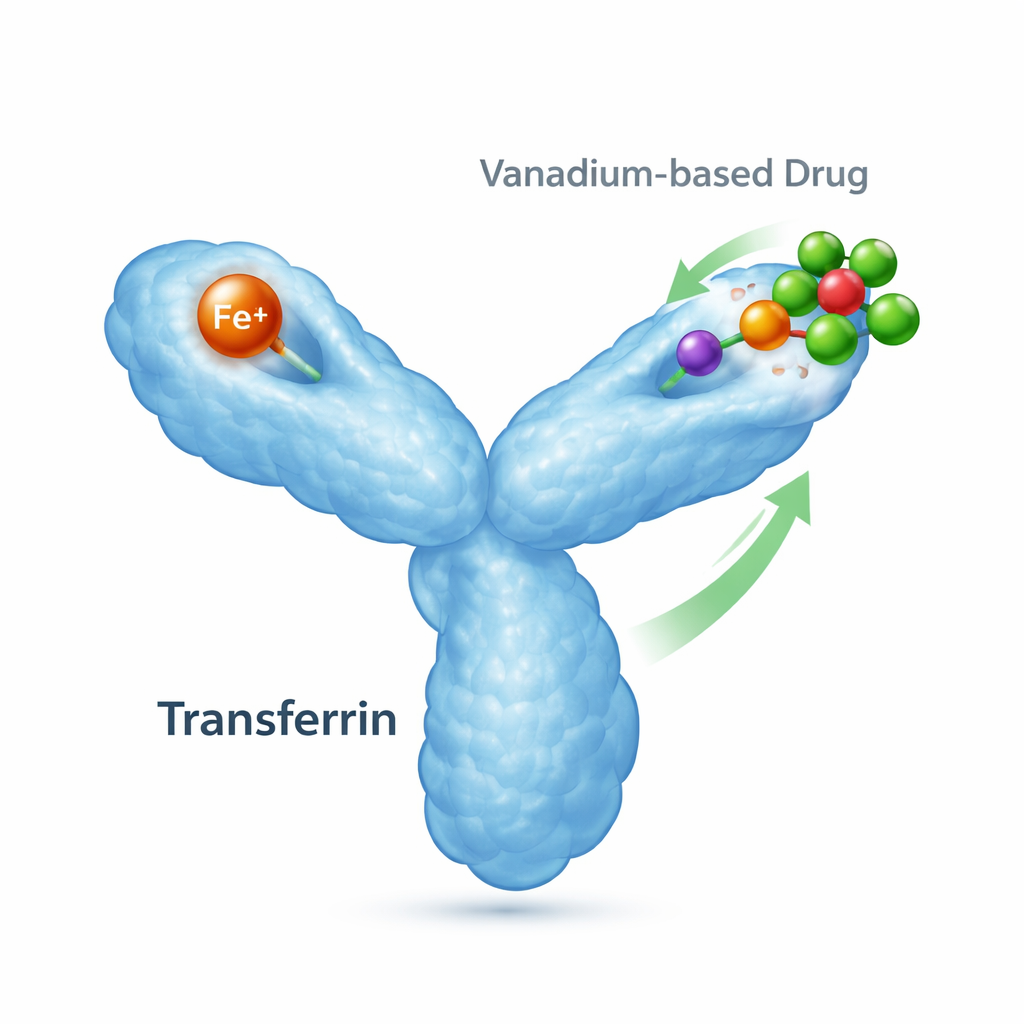
ساعي الحديد في الجسم ووظائفه الأخرى
الترانسفيرين هو بروتين بوزن نحو 80 كيلودالتون ومهمته اليومية التقاط الحديد وتسليمه إلى الخلايا التي تحتاجه. له فصّان («فصان»)، كل منهما قادر على ربط أيون حديد واحد، ويتغير شكله اعتماداً على وجود الحديد أم لا. عندما يرتبط الحديد، ينغلق الفص؛ وبدون الحديد، يبقى مفتوحاً. تتعرف مستقبلات متخصصة على أسطح الخلايا على هذه الأشكال المحمَّلة بالحديد وتُدخلها إلى داخل الخلية، مما يجعل الترانسفيرين مركزياً لتوازن الحديد وصحة الخلايا. ومع ذلك، يمكن للترانسفيرين أيضاً أن يرتبط بمعادن أخرى، بما في ذلك معادن من علاجات طبية، مما يعني أنه قد يؤثر على وجهة ومفعول الأدوية المعدنية.
لمحة شكلية عن الفاناديوم على الترانسفيرين
ركّز الباحثون على مرشح دوائي من الفاناديوم دُرِس جيداً يُدعى بيس(أستيل أسيتوناتو)أوكسو فاناديوم(IV)، ويُختصر عادة [VIVO(acac)₂]. أظهرت أعمال سابقة أن هذا المركب، أو أنواع مشتقة منه في الماء، يمكن أن تلتصق بالترانسفيرين، لكن لم يرَ أحد الشكل الدقيق لذلك. باستخدام البلّورة بالأشعة السينية، حصل الفريق على هياكل عالية الدقة للترانسفيرين الذي يحمل الحديد فقط في فصّه الطرفي C (الشكل «FeC»)، قبل وبعد التعرض لدواء الفاناديوم. في البلّورات المعالجة بالفاناديوم، لم يروا الدواء الأصلي بل عنقود فاناديوم–أكسجين متحوّل مرتبط بالفص النَّفسي N الخالٍ من الحديد. منحهم ذلك أول صورة بنيوية مباشرة لشظية فاناديوم مرتبطة بترانسفيرين الإنسان.
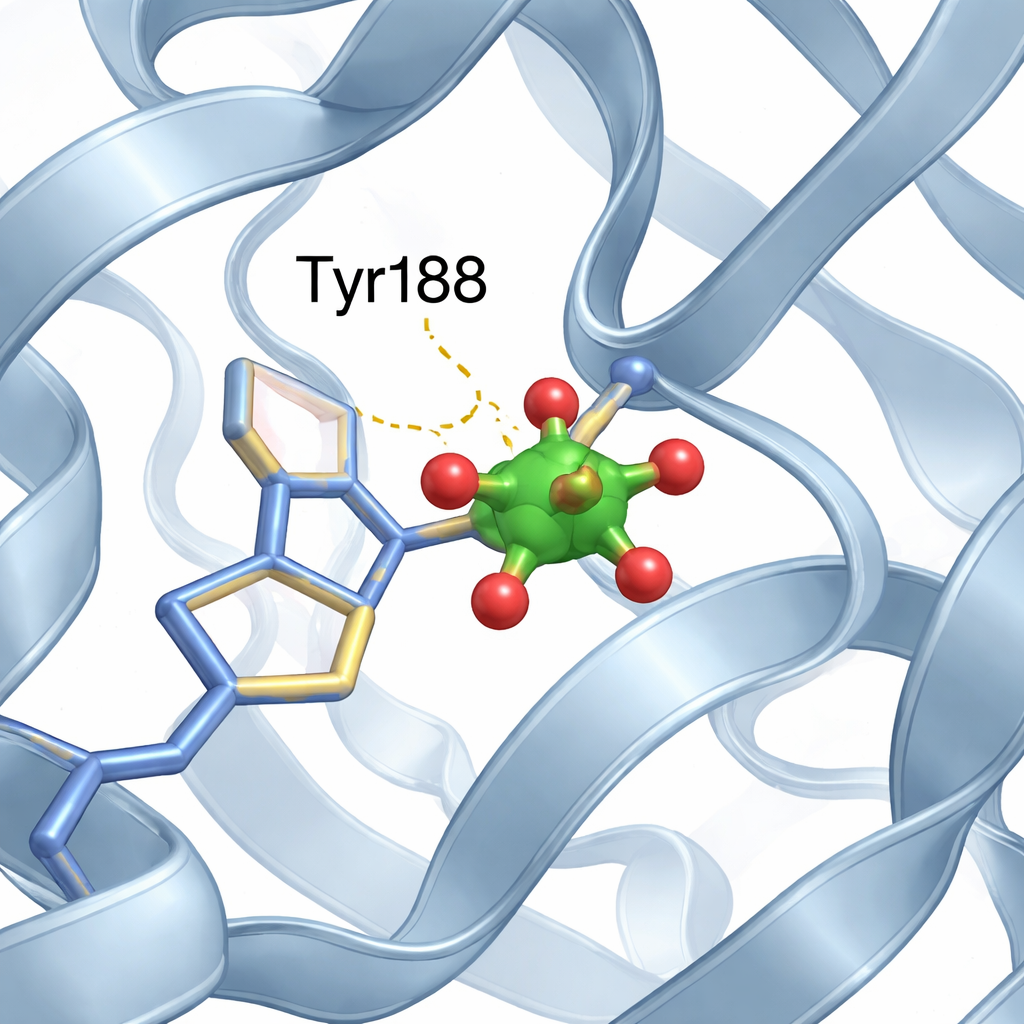
عنقود فاناديوم صغير يجد مكانه
داخل موقع الحديد في الفص N، عرّف الفريق عنقوداً صغيراً مكوّناً من ذرتين فاناديوم وذرات أكسجين، يُوصف على أفضل نحو كوحدة «ديفانادات» معدّلة. يحتل أحد مواقع الأكسجين في العنقود الأكسجين القادم من حمض أميني محدد، تيروزين 188 (Tyr188)، مكوِّناً رابطة مباشرة بين البروتين وعنقود المعدن. تثبّت تفاعلات لطيفة إضافية، مثل روابط الهيدروجين من أجزاء قريبة من البروتين، العنقود في مكانه. والأهم من ذلك أنه على الرغم من وجود هذا الضيف المعدني الجديد في جيب ربط الحديد، يحافظ البروتين عموماً على ترتيب فصي N المفتوح وC المغلق، متماثلاً تقريباً مع البنية الخالية من الفاناديوم.
كيف يعيد الترانسفيرين تشكيل كيمياء الفاناديوم
في المحلول وبقيم الحموضة والتركيز المستخدمة للتبلور، يكون النوع المكوّن من ذرتين فاناديوم الذي شوهد في البلّورة عادةً لاعباً ثانوياً؛ فالعناقيد الأكبر من الفاناديوم–الأكسجين تميل إلى أن تكون مهيمنة. تشير قياسات مطيافية وحسابات تصنيف الأنواع النظرية إلى أن الدواء الأصلي للفاناديوم يتأكسد تدريجياً ويتحلل في الماء، مكوناً أيونات فانادات بسيطة تتجمع بعد ذلك إلى مجموعة متنوعة من العناقيد. تشير البنية البلّورية إلى أن الترانسفيرين يثبت انتقائياً هذا الشظية الصغيرة الشبيهة بالديفانادات على حساب العناقيد الأكبر، إذ «يختار» شكلاً كيميائياً واحداً من خليط محلول مزدحم من خلال توفير موقع ربط محكم عند Tyr188 وشبكة داعمة من روابط الهيدروجين.
الحفاظ على مصافحة المستقبل الخلوية
لأن الترانسفيرين يجب أن يرتبط بمستقبل على أسطح الخلايا لتوصيل الحديد، تساءل الباحثون عما إذا كان ارتباط هذا العنقود الفاناديومي سيعطل تلك «المصافحة» الحيوية. باستخدام هجرة جِل غير باعثة للطيّ (non‑denaturing gel electrophoresis) وتقنية حساسة تُسمى التداخل الحيوي بطبقة ثنائية (biolayer interferometry)، قاسوا مدى ارتباط الترانسفيرين المعالج بالفاناديوم بمستقبل الترانسفيرين مقارنةً بالشكل المعالج بالحديد فقط. كلاهما تصرّفا تقريباً بنفس الطريقة، مع ارتباط قوي جداً في نطاق النانومولار المنخفض. يؤكد هذا أن العنقود الفاناديومي، بينما يقع في فص N، لا يغيّر بشكل كبير شكل الترانسفيرين في منطقة تفاعل المستقبل، وبالتالي لا ينبغي أن يمنع التعرف على البروتين من قبل الخلايا.
ما الذي يعنيه ذلك للأدوية المعدنية المنشأ
لغير المتخصصين، الخلاصة أن هذه الدراسة توفر لقطة جزيئية لكيفية ارتباط مشتق من دواء فاناديوم بناقل الحديد الرئيسي في الجسم دون تعطيل وظيفته الطبيعية. يمكن للترانسفيرين أن يلتقط عنقود فاناديوم–أكسجين صغير محدد داخل موقع الحديد، ومع ذلك يظل الشكل العام للبروتين وقدرته على الارتباط بالمستقبل تقريباً دون تغيير. يساعد ذلك في تفسير كيف قد تدور أدوية الفاناديوم وهي مرتبطة بالترانسفيرين، ويبرز أن بروتينات مختلفة قد تفضّل أحجام عناقيد فاناديوم مختلفة. مثل هذه الرؤى أساسية لتصميم علاجات معدنية أذكى يمكن التنبؤ بسلوكها في مجرى الدم—الأشكال التي تتخذها، إلى أين تذهب، ومدة بقائها—وللسيطرة عليها.
الاستشهاد: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
الكلمات المفتاحية: أدوية الفاناديوم, ترانسفيرين مصل الإنسان, علاجات معدنية المنشأ, ارتباط البروتين–المعدن, علم الأحياء البنيوي