Clear Sky Science · ar
البروتين المفرز CLCF1 يحسّن أمراض الكبد الراكدة عن طريق تثبيط تخليق أحماض الصفراء الكبدية وتعزيز إخراجها
لماذا تهم هذه الدراسة لصحة الكبد
أمراض الكبد الراكدة هي حالات يتوقف فيها تدفق الصفراء، السائل الهضمي الذي يصنعه الكبد، عن السير بشكل سليم فيتراكَم بدلاً من ذلك ويُسمم الكبد تدريجياً من الداخل. الأدوية الحالية تفيد شريحة صغيرة فقط من المرضى، والعديد منهم ينتهي بهم المطاف بحاجة إلى زراعة كبد. تكشف هذه الدراسة عن بروتين يُنتَج طبيعياً يدعى CLCF1 يبدو أن الجسم يشغّله كآلية دفاع عند حدوث الركود الصفراوي. فهم كيف يعمل هذا البروتين قد يوجّه نحو علاجات جديدة تحمي الكبد عن طريق تقليل إنتاج مكونات الصفراء الضارة ومساعدة الجسم على التخلص منها بكفاءة أكبر.
مساعد مخفي في الكبد المريض
بدأ الباحثون بفحص أنسجة الكبد من مرضى التهاب الأقنية الصفراوية المصلب الأولي والتهاب الأقنية الصفراوية الصفراوي الأولي، وهما شكلان رئيسيان من أمراض الكبد الراكدة طويلة الأمد. قارنوا بين أشخاص في مرحلة مبكرة من المرض وآخرين في مراحل أكثر تقدماً من الركود الصفراوي، وحللوا أيضاً مجموعات بيانات جينية منشورة. عبر هذه المصادر البشرية المستقلة برز بروتين مفرز واحد: كان CLCF1 باستمرار من بين الجينات التي تُظهِر زيادة قوية في الكبد الراكد. ارتبطت مستويات أعلى من CLCF1 بعلامات دموية أسوأ لشدة المرض، ما يوحي بأن الكبد يزيد إنتاج هذا البروتين مع تفاقم الإجهاد وتراكم الصفراء. في المرضى المبكرين الذين عولجوا بالدواء القياسي حمض الأورسوديوكسيكوليك، أولئك الذين استجابوا جيداً كانوا يميلون إلى امتلاك مستويات أعلى من CLCF1 في أكبادهم، مما يشير إلى أن هذا البروتين قد يدل على كبد أكثر قابلية للتكيف وحساسية للعلاج.
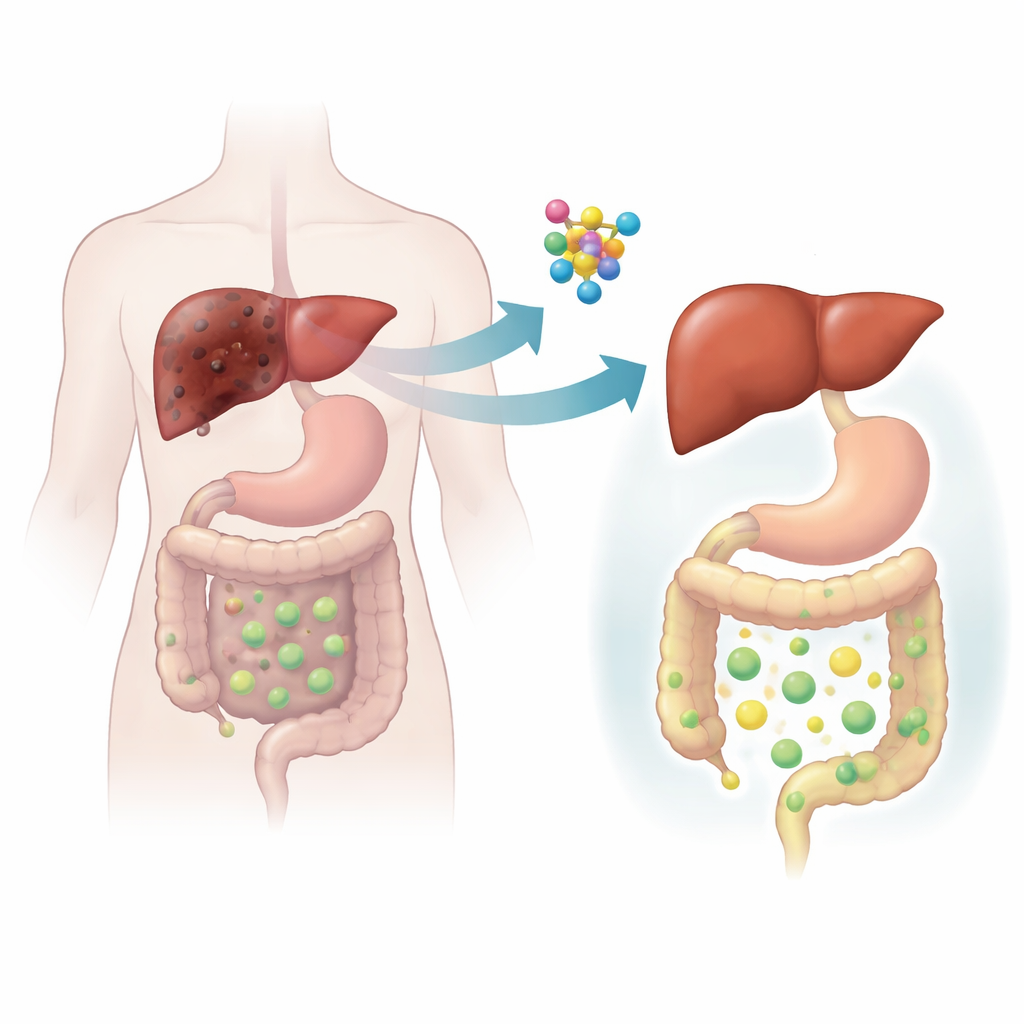
اختبار CLCF1 في نماذج حيوانية
للتجاوز عن الارتباطات البشرية إلى آليات سببية، لجأت الفريق إلى الفئران واستخدموا أساليب جينية وغذائية لمحاكاة مرض الكبد الراكد. في نموذجين فئريين مختلفين، زاد الركود الصفراوي بشدة من إنتاج الكبد لـ Clcf1، ما يعكس النتائج البشرية. عندما حذفت المجموعة مستقبل CLCF1 تحديداً من خلايا الكبد، ساءت الإصابة الركودية بشكل كبير: تكاثر الأقنية الصفراوية، وموت أنسجة الكبد، وازدياد الالتهاب، وتراكم النسيج الندبي، وتراكم أحماض صفراوية سامة. التجربة العكسية قدّمت صورة أكثر تفاؤلاً. عندما استخدم الفريق فيروساً غير ضار لرفع مستويات Clcf1 في الكبد فقط، تحسنت حالة الفئران. بدت أكبادهم أكثر صحة، تحسنت اختبارات الدم، قلّ التندب، وانخفضت كمية أحماض الصفراء المحتجزة في الكبد بصورة ملحوظة.
إغلاق الصنبور وفتح المصرف
كيف يقلل CLCF1 من حمولة أحماض الصفراء بهذه الفاعلية؟ وجد الباحثون فعلين مكمّلين. أولاً، هدأ CLCF1 مباشرة آلية الكبد لصنع الصفراء. في نماذج فئران متعددة وفي خلايا كبدية مزروعة، أطفأ CLCF1 الإضافي باستمرار إنزيمات رئيسية تحول الكوليسترول إلى أحماض صفراوية، ما يعادل خفض صنبور إنتاج الصفراء الجديد. حدث ذلك دون تنشيط مفتاح الكبد المعتاد للتحكم بالصفراء، وهو مستقبل نووي يسمى FXR، ما يعني أن CLCF1 يستخدم مساراً بديلاً داخل خلايا الكبد لإبطاء تخليق الصفراء. ثانياً، أثّر CLCF1 على كيفية معالجة الصفراء لاحقاً في الجسم. أعاد تشكيل مجتمع البكتيريا المعوية باتجاه أنواع قادرة بشكل خاص على معالجة أحماض الصفراء وزاد كمية أحماض الصفراء التي تخرج من الجسم مع البراز، فعمل كمصرف أقوى.
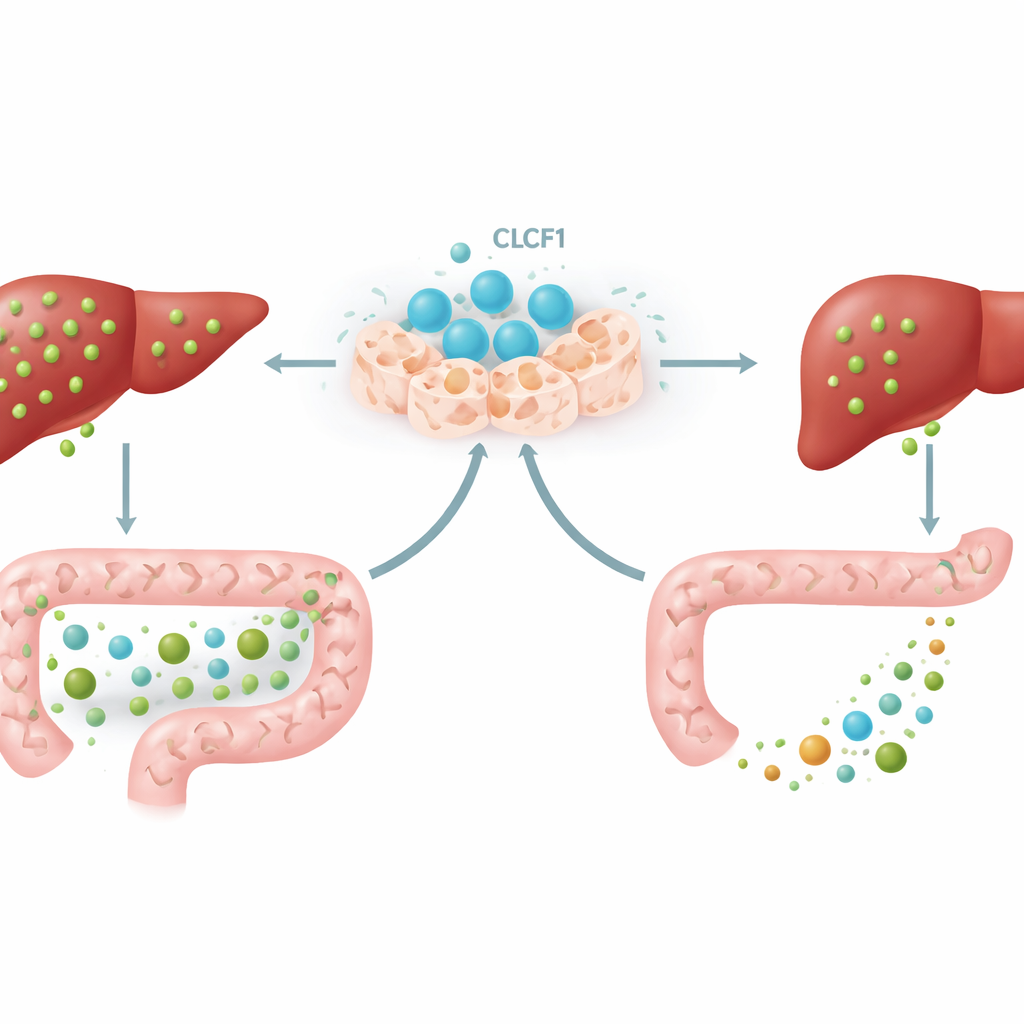
حوار الأمعاء–الكبد
جزء أساسي من اللغز تضمن حلقة إشارة بين الأمعاء والكبد. بعض أحماض الصفراء في الأمعاء تنشط مستشعراً يدعى FXR في خلايا الأمعاء، والتي تطلق بعد ذلك هرمون رسولي يعرف باسم FGF15 في الفئران. يسافر هذا الهرمون عبر الدم إلى الكبد ويخبره بتقليل إنتاج أحماض الصفراء. مع زيادة CLCF1، تراكمت أنواع محددة من أحماض الصفراء في أمعاء الفئران—خاصة الأشكال المعروفة بكونها منشطات قوية لـ FXR. نتيجة لذلك، انشطرت FXR المعوية، وارتفعت مستويات FGF15 في كل من الأمعاء والكبد، وكبح الكبد إنتاج أحماض الصفراء أكثر. عندما منع العلماء FXR المعوي بواسطة دواء محدود التأثير على الأمعاء، ضعف الكثير من التأثير الوقائي لـ CLCF1، مما يوضح أن هذا الحوار بين الأمعاء والكبد جزء أساسي من عمل البروتين.
ما الذي قد يعنيه ذلك للعلاجات المستقبلية
معاً، تصوّر هذه النتائج CLCF1 كصمام أمان مدمج لمرض الكبد الراكد. يخفّض البروتين مستويات أحماض الصفراء من الطرفين: يبطئ تكوينها داخل الكبد ويشجع على إزالتها عبر الأمعاء، بمساعدة ميكروبات معوية مفيدة وإشارة هرمونية راجعة. على عكس الأدوية الحالية التي تنشط FXR في جميع أنحاء الجسم وقد تسبب آثاراً جانبية مثل الحكة واضطراب دهون الدم، يبدو أن CLCF1 يوجّه التحكم في الصفراء بشكل أهدأ وأكثر انتقائية، خصوصاً عبر الأمعاء. رغم أن هذه النتائج لا تزال في نماذج فئران وعينات مخبرية، فإنها تشير إلى أن تعزيز CLCF1 أو محاكاة مساراته قد يؤسس لأساس علاجي جديد—وأن قياس هذا البروتين، أو أحماض الصفراء التي يزيدها في الأمعاء، قد يساعد في تحديد المرضى الذين سيستفيدون أكثر.
الاستشهاد: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
الكلمات المفتاحية: مرض الكبد الراكد, أحماض الصفراء, محور الأمعاء–الكبد, CLCF1, ميكروبيوتا الأمعاء