Clear Sky Science · ar
تحسين دقة CRISPR في أجنة الفئران عبر استهداف مهيمن على طريق الانضمام المتوسط التشابه
لماذا يهم صنع فئران معدلة وراثياً بدقة أعلى
جعلت أدوات تحرير الجينات مثل CRISPR من السهل بشكل ملحوظ إنشاء فئران تحاكي أمراض الإنسان، لكن هناك مشكلة خفية: التغيرات الجينية في الجيل المؤسس تكون غالباً فوضوية ومتنوعة. هذا يجعل التجارب أبطأ، وأقل موثوقية، ويستلزم استخدام حيوانات أكثر. تقدّم هذه الدراسة طريقة لتوجيه قطوع CRISPR في أجنة الفئران نحو نتائج متوقعة بدرجة عالية، بحيث تولد غالبية الفئران المؤسسة بنفس الطفرة المحددة والواضحة — مما يجلب بيولوجيا أنظف وأخلاقيات أفضل لأبحاث تحرير الجينات.
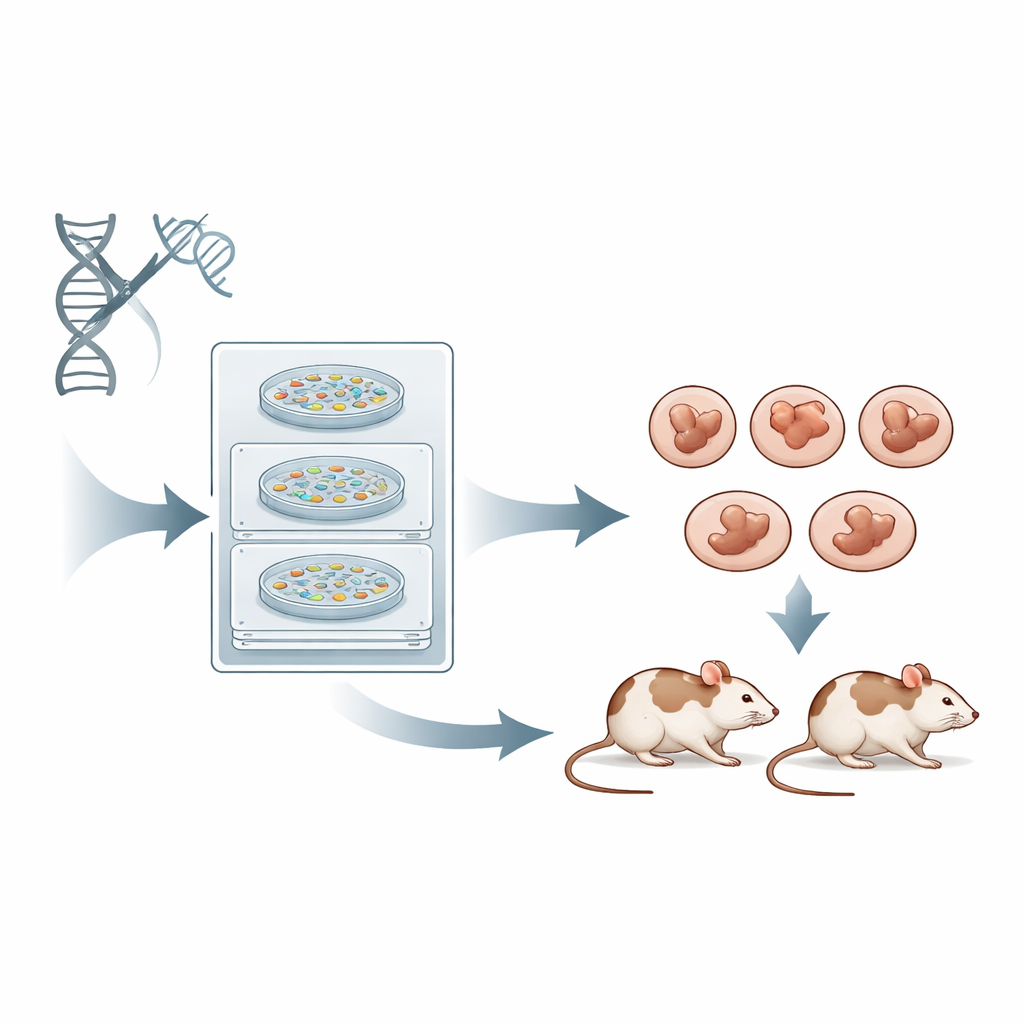
تحدي إصلاحات الحمض النووي الفوضوية
عندما يقطع CRISPR الحمض النووي، يجب على الخلية سد الكسر باستخدام آليات الإصلاح الخاصة بها. المسار الأكثر شيوعاً، المسمى الربط اللا متجانس للنهايات، سريع لكنه غير دقيق، وينتج خليطاً من الإضافات والحذوفات الصغيرة عند موقع القطع. مسار آخر، الانضمام المتوسط التشابه، يميل إلى حذف مقاطع من الحمض النووي بصورة نمطية باستخدام سلاسل قصيرة متطابقة كأدلّة. كلاهما أكثر فعالية بكثير من المسار الدقيق البطيء المعتمد على التماثل. في تجارب CRISPR التقليدية، يركز العلماء بشكل أساسي على مدى كفاءة الحمض النووي الدليلي في القطع وكمية المواقع غير المستهدفة، ويهملون إلى حد كبير أي مسار إصلاحي سيسود أو ما الطفرة الدقيقة التي ستنجم. النتيجة أن العديد من الفئران المؤسسة تحمل خليطاً من طفرات مختلفة في خلايا مختلفة، مما يجبر الباحثين على التهجين إلى الجيل التالي قبل أن يتمكنوا من العمل بجينوتيب نقي وموحد.
طريقة أذكى لاختيار أدلة CRISPR
سعى المؤلفون إلى قلب هذا السيناريو عبر تصميم أدلة ليست للقوة والسلامة فحسب، بل أيضاً للتنبؤية. بدأوا بأداة تعلم آلي اسمها inDelphi، مدرّبة على مجموعات بيانات ضخمة لطفرات ناتجة عن CRISPR في خلايا مزروعة. لا تكتفي inDelphi بالقول كم مرة سيُحرَّر الموقع؛ بل تتنبأ بقائمة كاملة من الإضافات والحذوفات المحتملة وبمدى تكرار كل واحدة، مع اهتمام خاص بالأحداث المدفوعة بالتشابه المتوسط. فحص الفريق جين التيروزيناز (Tyr) لدى الفئران، حيث يؤدي فقدان الوظيفة إلى الباليدية، واختروا أحماضاً ريبية دليلة متوقعة أن تفضّل حذوفات مهيمنة ومتكررة مدفوعة بالتشابه المتوسط مع إبقاء مخاطر المواقع غير المستهدفة منخفضة. ثم عدّلوا أجنة الفئران وقيّموا الطفرات الناتجة بتسلسل عميق. عموماً، ظهرت النمط الجيني المفضّل لـ inDelphi لكل دليل بتواتر مماثل في الأجنة كما تنبأت، وأنتجت الأدلة ذات ميزات التشابه المتوسط الأقوى بالفعل أنماط طفرات أكثر تجانساً.
استخدام الخلايا الجذعية كمسرح تجريبي
مع ذلك، لم تكن التنبؤات وحدها كافية. عندما قارن الفريق توقعات inDelphi مع أنماط التحرير الفعلية، وجدوا توافقاً متواضعاً فقط. لسد هذه الفجوة، أدخلوا خطوة عملية وسيطة: اختبار كل دليل في خلايا جذعية جنينية للفأر تشترك في العديد من الخصائص مع الأجنة المبكرة جداً. بعد إدخال مكوّنات CRISPR إلى هذه الخلايا، فرزوا الخلايا المعدلة وسلسلوا مواقع الاستهداف. طابقت أنماط الطفرات في الخلايا الجذعية تلك الموجودة في الأجنة بدرجة أكبر بكثير من نموذج الحاسوب. الأدلة التي أنتجت حذفاً واحداً مهيمنًا في الخلايا الجذعية عادةً ما فعلت الشيء نفسه في الكيسة الأريمية والأجنة في مراحل لاحقة. من خلال الجمع بين تصنيف inDelphi وهذه "البروفة" في الخلايا الجذعية، تمكن الباحثون من اختيار الأدلة التي تدفع إصلاحاً متوسط التشابه وتقلل من تنوع الأليلات الطافرة بشكل موثوق.
من لون العين إلى الأطراف المفقودة
اختبر المؤلفون خط أنابيبهم في حيوانات حية. بالنسبة لجين Tyr، اختاروا ثلاثة أدلة تمثل دقة متوقعة عالية ومتوسطة ومنخفضة ونقلوا الأجنة المعدلة إلى أمهات حاضنة. في اليوم 11.5 من التطور، فحصوا تصبغ العين وسلسلوا كل جنين على حدة. أنتج الدليل الذي يفضل التشابه المتوسط بشدة أجنة كانت في الغالب شاحبة وحملت حذفًا صغيرًا مهيمنًا، وغالباً في نسختي الجين، مع تغاير ضئيل جداً. أدى دليل أقل تحسينًا إلى مزيج من فقدان الصبغة وتصبغ جزئي مرتبط بمجموعة أكثر تعقيدًا من الطفرات. ثم طبّقوا نفس النهج على جين Fgf10، حيث يؤدي فقدان الوظيفة إلى أجنة بلا أطراف. باختيار دليل تنبؤ به—وتحقق منه في الخلايا الجذعية—لإعطاء حذف من أربع قواعد مع احتمال كبير لتعطيل الجين، ولّدوا أجنة في اليوم 15.5 كانت بلا أطراف بشكل موحد وحملت مجموعة مُثبّتة بقوة من الحذوفات المتوقعة. عبر كلا الجينين، سيطرت نفس الأنواع القليلة من الطفرات على توقعات inDelphi، والخلايا الجذعية، والأجنة المبكرة، والأجنة في المراحل اللاحقة.
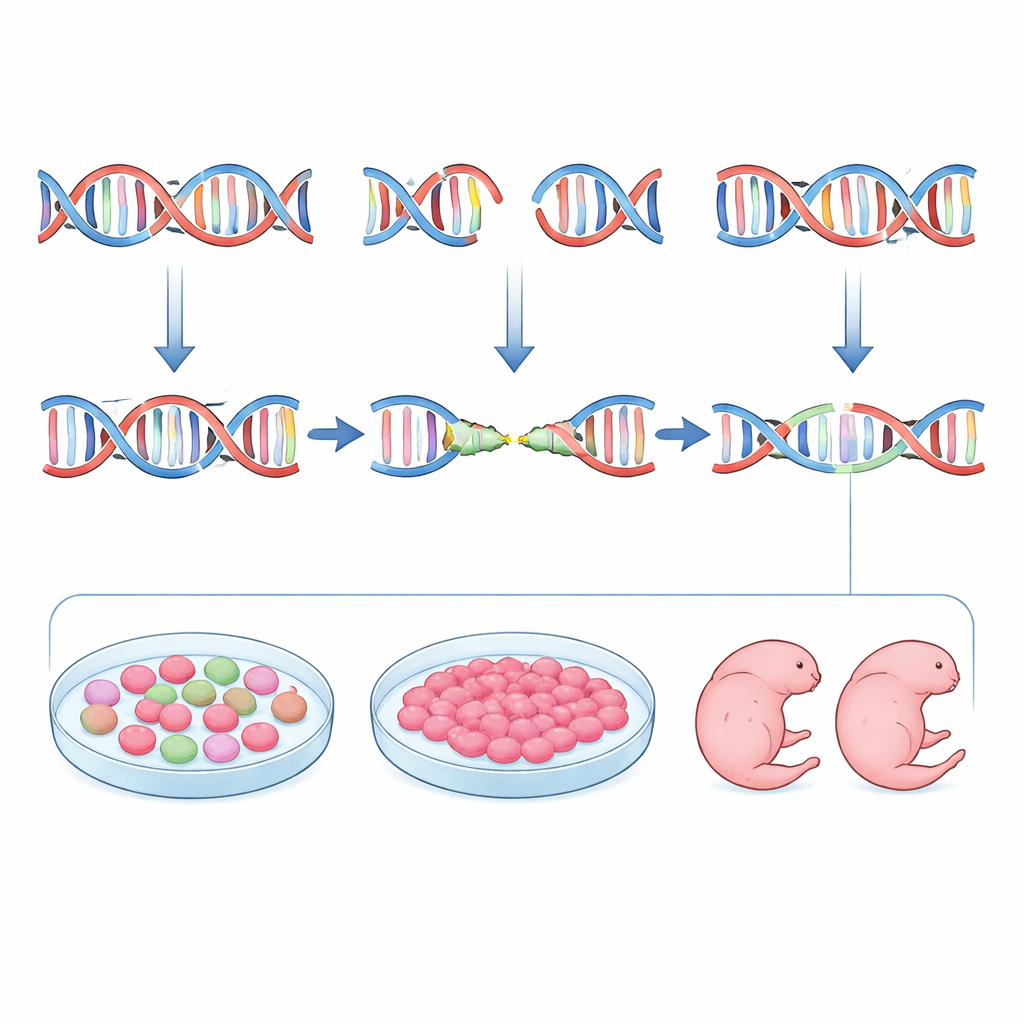
جينات أنظف بعدد أقل من الحيوانات
من الناحية العملية، تقدم الدراسة نموذجًا جديدًا لتصميم تجارب CRISPR في الفئران. بدلاً من الانتقال مباشرة من دليل مُصمم بالحاسوب إلى تعديل الأجنة، يوصي المؤلفون بخط متكامل: استخدام inDelphi وأدوات تقييم المواقع غير المستهدفة لاختيار الأدلة التي من المرجح أن تفضّل الحذوفات المتوسطة التشابه وإزاحات الإطار، اختبار تلك الأدلة في الخلايا الجذعية الجنينية لتأكيد كل من الكفاءة وانتظام الطفرات، ثم المضي قُدماً بالأفضل أداءً فقط إلى تجارب الأجنة. تُثمر هذه الاستراتيجية فئرانًا مؤسسة تشترك خلاياها بغالبية ساحقة في نفس الطفرة الموصوفة جيدًا، مما يجعلها مفيدة فورياً لنمذجة أمراض الإنسان—خصوصًا تلك الناجمة عن تغييرات نمطية من نوع الحذف—مع تقليل عدد الحيوانات التي يجب تربيتها وفحصها. النتيجة هي جينات أوضح وأكثر قابلية للتكرار ومسار أكثر أخلاقية إلى نماذج أمراض قوية.
الاستشهاد: Lkhagvadorj, K., Okamura, E., Taki, T. et al. Optimizing CRISPR precision in mouse embryos via microhomology-mediated end joining-dominant targeting. Commun Biol 9, 371 (2026). https://doi.org/10.1038/s42003-026-09771-z
الكلمات المفتاحية: CRISPR, نماذج الفئران, تحرير الجينوم, إصلاح الحمض النووي, نمذجة الأمراض