Clear Sky Science · ar
الجلكزة كمنظم ديناميكي لمسارات الإشارات المناعية الفطرية RLR و cGAS-STING
كيف تساعد وسوم السكر الخلايا على استشعار الفيروسات
تظل خلايانا في حالة يقظة دائمة ضد الفيروسات الغازية، ويعتمد الكثير من هذا الدفاع على وسوم سكّرية صغيرة مرتبطة بالبروتينات. تستعرض هذه المراجعة كيف تعمل هذه الوسوم السكرية، المعروفة بالجلكزة، كأجهزة ضبط شدة (مخفتات) بدلاً من أن تكون مفاتيح تشغيل/إيقاف بسيطة لمسارات مضادة للفيروسات. قد يفتح فهم هذا الضبط المعتمد على السكر طرقاً جديدة لتعزيز اللقاحات، وعلاج العدوى الفيروسية، وحتى توظيف الجهاز المناعي ضد السرطان.
المنبه المبكر للخلايا
عند دخول الفيروسات إلى الخلية، تترك وراءها شرائط من الحمض النووي الريبي أو الحمض النووي كدلائل. تقوم أنظمة "الإنذار" المتخصصة بدوريات داخل الخلية بحثاً عن هذه الحطام الجيني. يكشف نظام واحد، يُسمى مسار مستقبلات RIG-I الشبيهة (RLR)، الحمض النووي الريبي الفيروسي. ونظام آخر، معروف باسم مسار cGAS–STING، يستشعر الحمض النووي الذي يظهر في مكان غير مناسب داخل الخلية. عند تنشيطها، تشغّل كلا المسارين شلالات كيميائية تنتهي بإطلاق الإنترفيرونات من النوع الأول وجزيئات التهابية—إشارات قوية تحذر الخلايا المجاورة وتجند الدفاعات المناعية. وبما أن زيادة أو نقصان هذا الاستجابة يمكن أن يكون مضرًا، يجب على الخلية ضبط هذه المنبهات بعناية، وتعد الجلكزة إحدى الطرق الرئيسة للقيام بذلك. 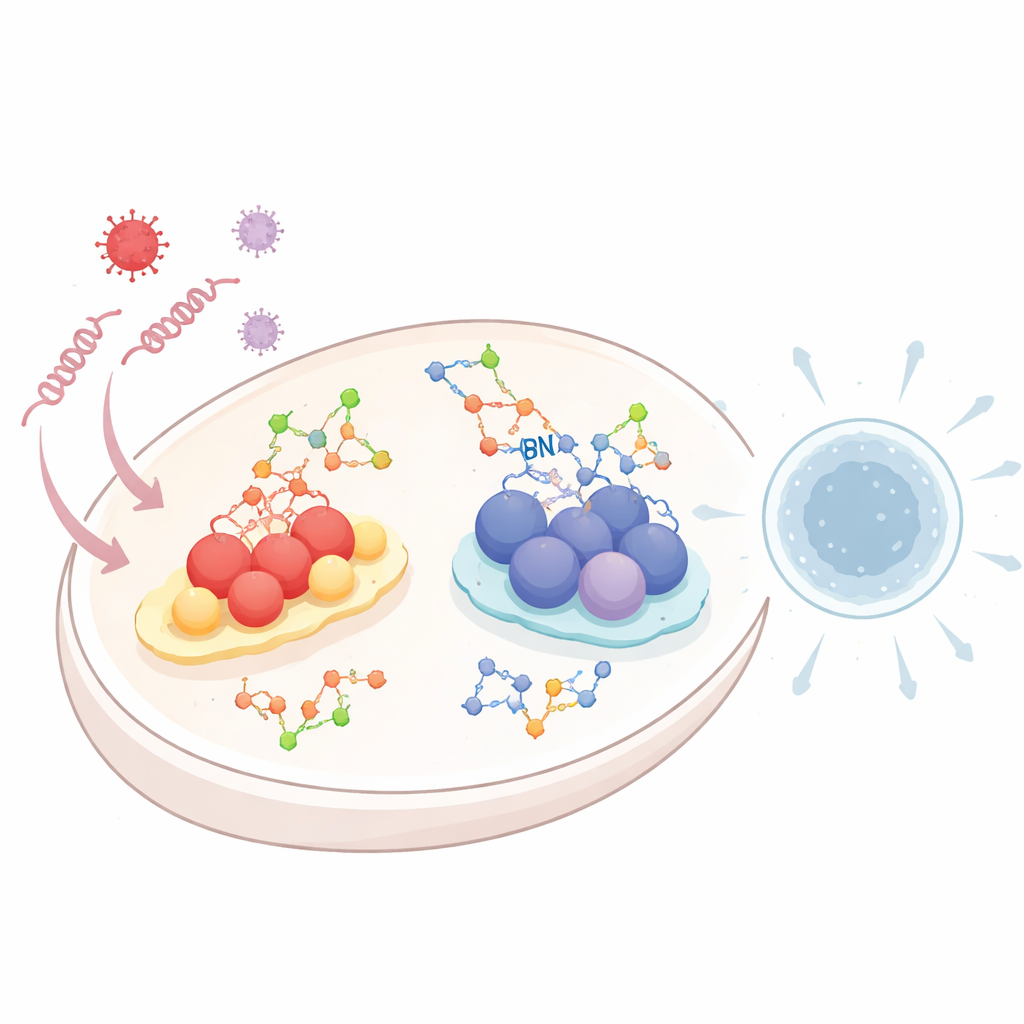
أغطية السكر كضوابط دقيقة
تضيف الجلكزة وحدات سكرية صغيرة إلى البروتينات في مواقع خلوية مختلفة. في شبكة الشحن الداخلية للخلية، الشبكة الإندوبلازمية وجولجي، تساعد سلاسل السكّر المرتبطة بطريقة N الكبيرة البروتينات على الطي الصحيح، والحفاظ على استقرارها، والانتقال إلى الغشاء المناسب. بالمقابل، شكل أنحف يدعى O-GlcNAcylation يضع سكرًا واحدًا على البروتينات في السيتوبلازم والنواة. هذا الوسم البسيط شديد الديناميكية، إذ يتبدل بسرعة عبر إنزيمين يضيفانه أو يزيلانه استجابةً لمستويات المغذيات والضغط الخلوي. تصف المراجعة كيف أن هذه الأنواع المختلفة من السكّر لا تعمل ببساطة على تشغيل أو إيقاف حسّاسات المناعة؛ بل تضبط مدى سهولة تجمع الحساسات، ومدة بقائها، وقوة إشارتها. بهذه الطريقة، تربط الجلكزة حالة الأيض الخلوي مباشرةً بجهوزيته لمكافحة العدوى.
ضبط مسار مستقبِلات الـRNA
ضمن نظام استشعار RNA (RLR)، يوجد بروتين ناقل مركزي يُدعى MAVS موضوعًا على الميتوكوندريا ويعمل كمحور رئيسي. تبيّن المراجعة أن O-GlcNAcylation على MAVS يمكن أن يسرّع أو يبطئ الإشارة المضادة للفيروسات، اعتمادًا على موضع وضع السّكر. تسهّل وسوم سكرية عند مواقع معينة زينة بروتينية لاحقة، مثل نوع محدد من سلاسل اليوبكوتين، تساعد MAVS على تكوين تجمعات إشارية كبيرة ودفع إنتاج إنترفيرون قوي ضد فيروسات RNA. مواقع سكرية أخرى تبقي MAVS موزعًا وبحالة ساكنة وغير نشطة في الظروف العادية، مانعةً الالتهابات غير الضرورية. يمكن للعدوى الفيروسية وتغيرات مسار التمثيل الغذائي المنتج للسكر في الخلية أن تحوّل الميزان بين هذه الوسوم المنشِّطة والمثبطة. كما أن تعديلات مرتبطة على عامل آخر، IRF5، قد تدفع الجهاز المناعي نحو "عواصف السيتوكين" الضارة، مما يبرز أن المزيد من السكر ليس دائماً أفضل. وبالموازاة، قد يستغلّ الفيروس سلاسل N المرتبطة ببروتينات سطح الخلية مثل مستقبل عامل النمو EGFR لوضع علامات على حسّاسات أعلى مثل RIG-I للضمور، مما يضعف الدفاعات المضادة للفيروسات.
ضبط مسار مستقبِلات الـDNA
يتأثر مسار استشعار الحمض النووي cGAS–STING أيضاً بشكل كبير بالجلكزة. يحتاج STING، وهو بروتين غشائي في الشبكة الإندوبلازمية، إلى سلاسل سكرية مرتبطة بطريقة N للطي الصحيح، والبقاء مستقراً، والتجمع في عناقيد إشارية عند تنشيطه بواسطة رسوليات مشتقة من الحمض النووي. بدون هذه السكريات، يفشل STING في تشكيل البنى الأعلى المرتبة والمرور عبر مقصورات الخلية اللازمة لإطلاق إنترفيرون قوي. في الوقت نفسه، تعزز O-GlcNAcylation لـSTING عند موقع معين مجموعة مختلفة من الوسوم الكيميائية التي تشجّع تجمعه وحركته، مما يضخم الإشارات المضادة للفيروسات ضد فيروسات DNA. تساعد سلاسل سكرية أخرى تسمى جليكوسامينوغليكانات مكلَّفة بالسلفات، المبنية في جولجي، أيضاً عبر تسهيل بوليمرة STING إلى هياكل طويلة تجذب الإنزيمات اللاحقة. يرد الفيروسون بالمواجهة عبر تعديل جليكوبروتيناتهم أو تحفيز مسارات تآكل تستهدف STING، غالبًا في نفس المساحات الخلوية حيث تضاف هذه الزينات السكرية أو تتم معالجتها. 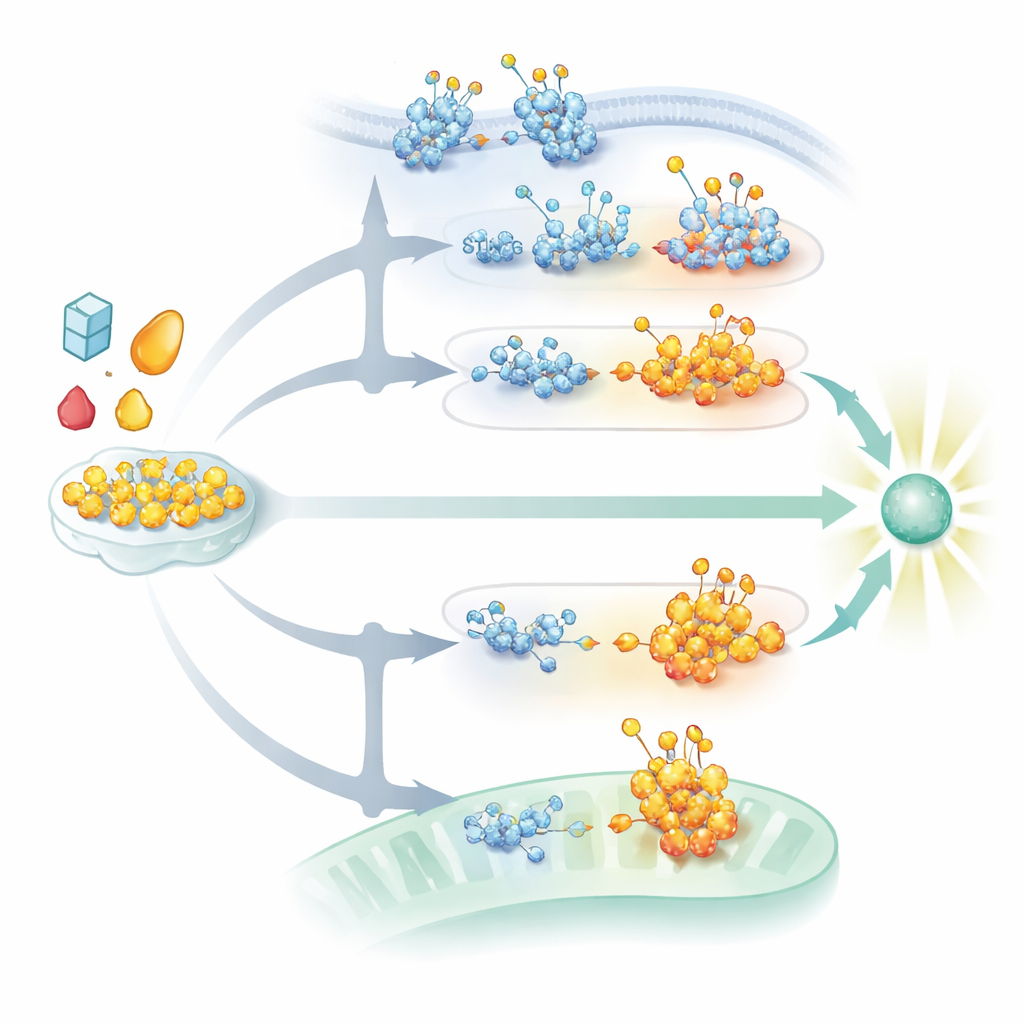
الأيض والمرض والعلاجات المستقبلية
بما أن المانح السكري الرئيسي لـO-GlcNAcylation يُصنَع عبر مسار أيضي يعرف بمسار تخليق الهكسوزأمين، فإن التحولات في استخدام المغذيات تشكل مباشرةً الإشارات المضادة للفيروسات. يستغل العديد من الفيروسات هذا المسار لصالحها، بينما يمكن أن يقوّي أو يضعف تعزيز أو حجب تدفق الهكسوزأمين الاستجابات المضادة للفيروسات في نماذج حيوانية. تربط المراجعة هذه الآليات بالأمراض البشرية: غالبًا ما تعيد الأورام برمجة الجلكزة لتقليل إشارات الإنترفيرون والهروب من الهجوم المناعي، بينما يمكن أن تميل الضغوط الأيضية المزمنة أو العيوب الوراثية في معالجة السكر تجاه مناعة ذاتية ضارة. يجادل المؤلفون بأن الإنزيمات التي تتحكم بالجلكزة—خصوصًا تلك التي تضيف أو تزيل O-GlcNAc أو تبني الهياكل الرئيسية المرتبطة بطريقة N—تمثل أهدافًا دوائية واعدة لكنها تحدٍّية. من المرجح أن تحتاج العلاجات المستقبلية إلى العمل بموقعية وحسّ سياقي، لدفع "كود الجليكان" نحو حماية أفضل ضد العدوى والسرطان والاضطرابات الالتهابية دون إثارة أشكال جديدة من الاختلال المناعي.
الصورة الأوسع للصحة اليومية
بشكل يومي، تكشف هذه المقالة أن منبهات الجسم الأمامية المضادة للفيروسات لا تعمل بمعزل—بل هي مرتبطة بشبكة استخدام الطاقة وكيمياء السكر داخل الخلية. تقرر وسوم السكر الصغيرة على عدد محدود من البروتينات الحرجة ما إذا كان جينوم فيروسي طائش سيشعل تحذيراً محسوباً، أو دفاعاً كاملاً، أو رد فعل مفرطاً وخطيراً. من خلال فك شيفرة هذا النظام الضابِط القائم على السكر وتعلّم كيفية تعديله في نهاية المطاف، يأمل الباحثون في تصميم علاجات تجعل اللقاحات أكثر فعالية، تساعد على التخلص من العدوى المستعصية، تكشف الأورام أمام الجهاز المناعي، وتهدئ الالتهاب الجامح في أمراض المناعة الذاتية.
الاستشهاد: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
الكلمات المفتاحية: المناعة الفطرية, الجلكزة, مسار RLR, cGAS-STING, O-GlcNAcylation