Clear Sky Science · ar
يشير نمذجة مدفوعة بمعدل النمو إلى أن التكيّف الظاهري يقود مقاومة الدواء في الميلانوما الحاملة لطفرة BRAFV600E
خلايا السرطان التي تتعلّم العيش مع الأدوية
غيّرت الأدوية الموجهة مجرى العلاج لكثير من المصابين بالميلانوما، وهو سرطان جلدي خطير. ومع ذلك، تتوقف هذه الأدوية تقريبًا دائمًا عن العمل: الأورام التي كانت تتقلص تبدأ بالنمو مجددًا. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قويًا: بدل الاعتماد فقط على الطفرات الجينية، هل يمكن لخلايا الميلانوما أن "تتعلّم" البقاء أثناء العلاج بتغيير سلوكها—وهل قد يفسّر هذا التعلم سبب تفوّق بعض طرق إعطاء الأدوية على غيرها؟
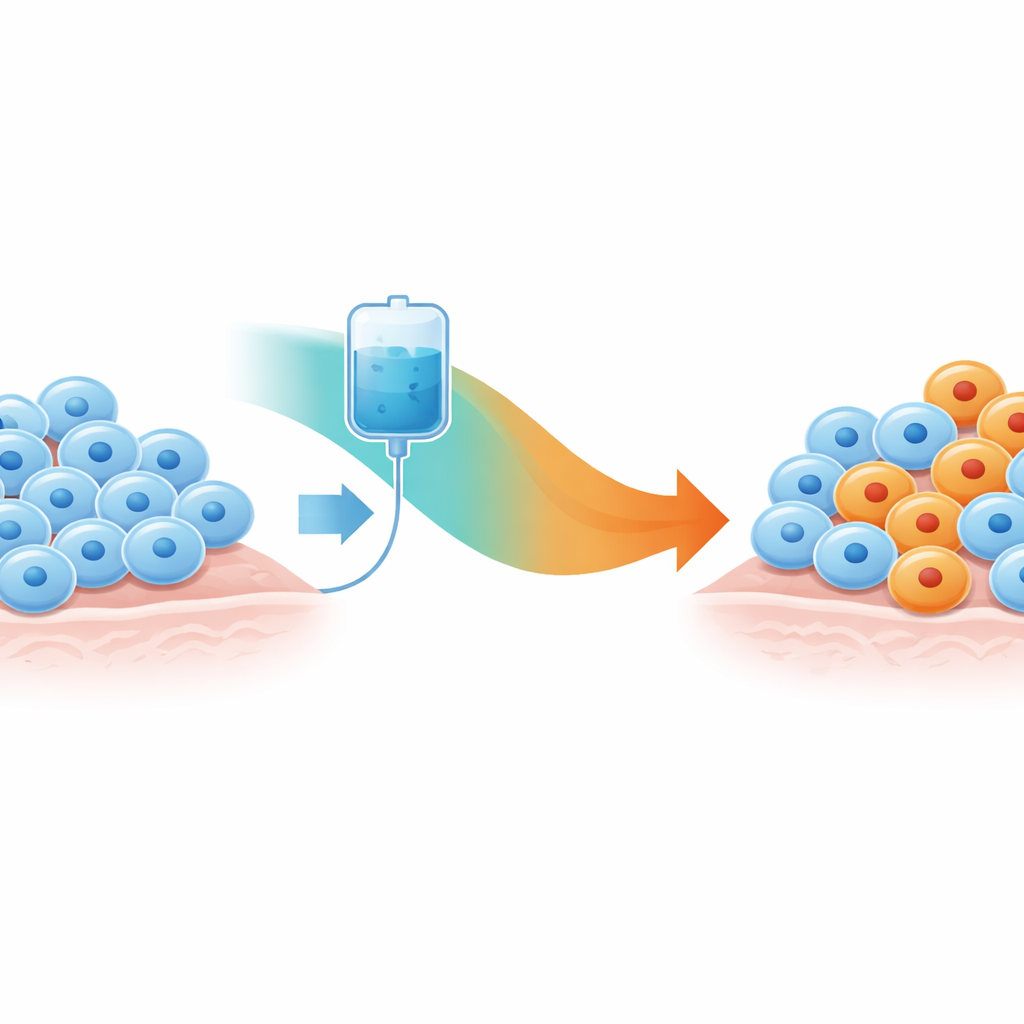
من خلايا حسّاسة إلى ناجية
ركّز الباحثون على خلايا ميلانوما تحمل تغيرًا شائعًا في جين يُدعى BRAF، ما يجعلها حسّاسة بشكل خاص لنوع من الأدوية يُعرف بمثبطات BRAF. في تجارب مخبرية من أعمال سابقة، تعرّضت هذه الخلايا لمادّة انكورافينيب بجرعات وأطوال مدة مختلفة. من خلال قياس سرعة نمو الخلايا أو موتها تحت كل حالة بعناية، قسم المؤلفون الخلايا إلى فئتين عامّتين: خلايا لم تتعرض للدواء من قبل، وخلايا تكيفت مع الدواء بعد أن عاشت في وجوده لأسبوع على الأقل. الخلايا التي لم تتعرّض للدواء نمت جيدًا دون معالجة لكنها تباطأت بشدة أو قُتلت بوساطة الدواء. بالمقابل، الخلايا المتكيّفة نمت أفضل في حضور الدواء لكنها فقدت هذه الميزة عند إزالة الدواء—ما يلمّح إلى أن بقائها مرتبط بتغيير مرن وقابل للانعكاس في الحالة بدلاً من ضرر جيني دائم.
خريطة السلوكيات الخفية للخلايا
لفهم هذه التغيّرات بنحوٍ أدق، بنى الفريق نموذجًا رياضيًا تُمنح فيه كل خلية سرطانية "حالة ظاهريّة"—موقعًا تجريديًا على مقياس من الحساسية الشديدة تجاه الدواء إلى المقاومة الشديدة له. بدل افتراض وجود نوعين فقط من الخلايا، سمحوا بوجود حالات متوسطة عديدة، تعكس تحوّلات تدريجية في مؤشرات بيولوجية للمقاومة. لكل مزيج من الحالة وجرعة الدواء، قدّروا معدل نمو صافٍ، يمكن أن يكون موجبًا (انقسام خلايا أكثر من الوفيات) أو سالبًا (وفيات أكثر من الانقسامات). رتّبوا كل هذه المعدلات في شبكة أو "مصفوفة لياقة" تعمل كمنظومة تضاريس: بعض الحالات عند بعض الجرعات أماكن مناسبة لازدهار الخلايا، وأخرى قاتلة. يمكن للخلايا في النموذج أن تتحرّك خطوة بخطوة عبر هذه التضاريس حين يُشغّل العلاج أو يُوقَف.
هل تنجرف الخلايا أم تتسلّق نحو الميزة؟
المجهول الرئيسي كان كيفية تحرّك الخلايا عبر هذه التضاريس. اختبر المؤلفون أربع استراتيجيات محتملة. في إحدى الاستراتيجيات، لا تغيّر الخلايا حالتها أبدًا، فعندئذٍ يجب أن تكون الخلايا المقاومة موجودة منذ البداية. في أخرى، تتجوّل الخلايا عشوائيًا بين الحالات المجاورة، كمسيرة سكير، بغض النظر عمّا إذا كان وضعها يتحسّن أم لا. في الاستراتيجيتين المتبقيتين، تميل الخلايا إلى التحرك نحو حالات يكون فيها معدل نموها أعلى—إما بحركة متخبّطة مع بعض الأخطاء، أو بقوة دافعة دائمًا تتسلّق نحو بقاء أفضل. عند تشغيل الفريق لمحاكيات حاسوبية ومقارنتها مع بيانات مخبرية حقيقية، ولا سيما تجارب أعطيت فيها الدواء إما باستمرار أو بنمط تشغيل/إيقاف (أسبوع تشغيل، أسبوع إيقاف)، لم تستطع سوى الاستراتيجيات التي تتسلّق فيها الخلايا نحو لياقة أعلى أن تعيد إنتاج ما لوحظ: العلاج المتقطع بجرعة عالية قلّص أعداد الخلايا أفضل من العلاج المستمر مع نفس إجمالي الزمن وكمية دواء كلية أعلى.
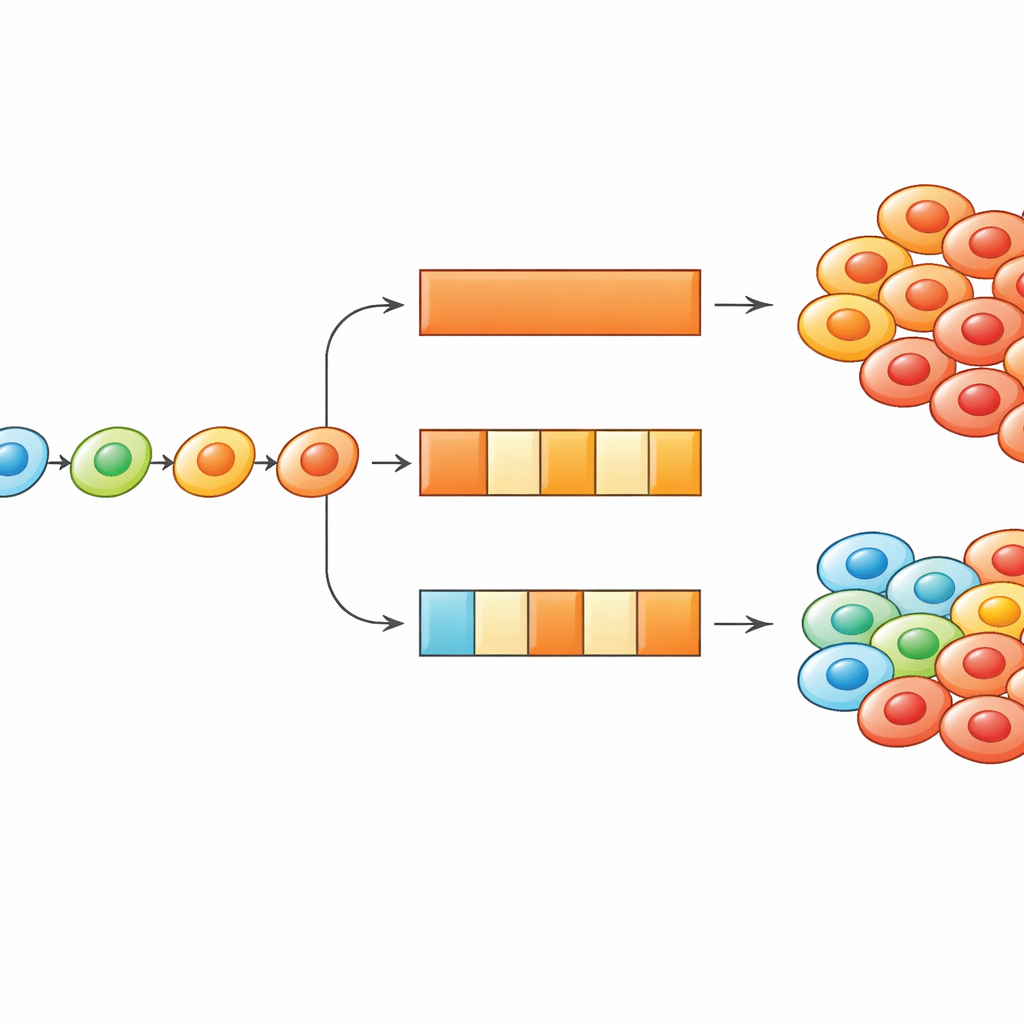
استخدام الجرعات بالتشغيل/الإيقاف لتحويل التكيّف ضد السرطان
تعمّق الباحثون، مستخدمين كلًا من المحاكاة ومعادلات أبسط لاستكشاف مدى تكرار سماح الخلايا بتغيير حالتها وطول فترات تشغيل وإيقاف الدواء. وجدوا أنه عندما يتكيّف الخلايا بطريقة موجهة، يمكن ضبط جداول العلاج إما لإبطاء هذا التكيّف أو لاستغلاله. تقصير وتيرة تحديث الخلايا لحالتها—من حيث المفهوم، إبطاء الآليات البيولوجية التي تمكّن التغيير الظاهري—يميل إلى جعل العلاجات المتقطعة أكثر فعالية، لأن الخلايا لا تستطيع بسرعة الصعود نحو حالات مقاومة عالية. على النقيض، إذا بدأت الخلايا في حالة مقاومة قوية، يمكن لعطلات الدواء أن تمنحها وقتًا للانزلاق مرة أخرى نحو حالات أكثر حساسية، بحيث يؤدي إعادة إدخال الدواء إلى موجة من موت الخلايا. تُظهر الدراسة كيف يشكّل توقيت الجرعات وسرعة تكيّف الخلايا معًا أي جدول يكون الأفضل.
ماذا يعني هذا لرعاية السرطان المستقبلية
لغير المتخصص، الرسالة المركزية هي أن خلايا السرطان ليست أعداء ثابتين؛ بل هي متغيرة الشكل. في نظام الميلانوما هذا، يبدو أن الخلايا تتحرّك بنشاط نحو سلوكات تساعدها على النمو تحت أي ظروف تواجهها. يقترح نموذج المؤلفين أن هذا التكيّف الموجَّه بمفرده—دون استدعاء أجيال دائمة مختلفة—يستطيع تفسير سبب تفوّق جداول الدواء بالتشغيل/الإيقاف أحيانًا على الجرعات الثابتة، حتى عندما تستخدم كمية أقل من الدواء إجمالًا. ومع أن هذه النتائج مستمدة من خلايا مزروعة في المختبر وتحتاج إلى مزيد من العمل قبل أن تُوجَّه رعاية المرضى، فإن النهج يوفر إطارًا عمليًا: بقياس سرعة وفي أي اتجاه تتكيّف خلايا السرطان، قد يتمكّن الأطباء في نهاية المطاف من تصميم جداول علاجية لا تهاجم الأورام فحسب، بل توجّه "تعلم" الخلايا الظاهري إلى مسارات مسدودة بدلًا من طرق هروب.
الاستشهاد: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
الكلمات المفتاحية: الميلانوما, مقاومة الدواء, مرونة الخلايا, العلاج المتقطع, النمذجة الرياضية