Clear Sky Science · ar
الأساس البنيوي لتفعيل ريدوكتاز أول أكسيد النيتريك المعتمد على الكينول لدى Neisseria meningitidis عن طريق التزاوج الثنائي
كيف تُخدع البكتيريا دفاعنا المناعي
عندما تغزو البكتيريا الضارة الجسم، تطلق خلايا جهاز المناعة لدينا جزيئات سامة مثل أول أكسيد النيتريك لقتلها. غير أن بعض الممرضات طورت حيلًا جزيئية لتحييد هذا الهجوم والبقاء على قيد الحياة. تكشف هذه الدراسة، بتفاصيل ذرية، كيف يعيد إنزيم بكتيري رئيسي تشكيل نفسه ليكوّن أزواجًا ويصبح أكثر فعالية كثيرًا في إزالة سمية أول أكسيد النيتريك، ولماذا قد يفتح فهم هذا السلوك المتغير الأشكال سبلًا جديدة لتصميم مضادات حيوية.
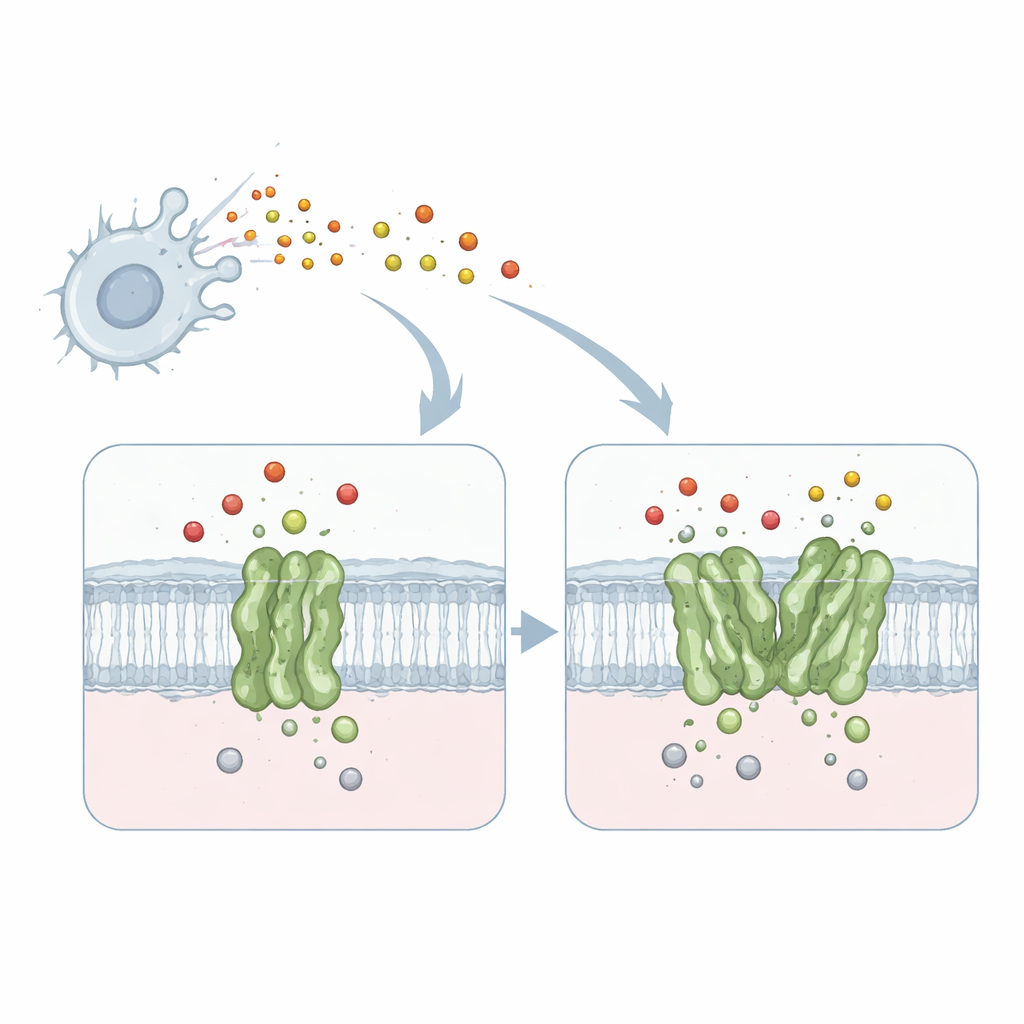
آلة صغيرة تعطل غازًا سامًا
تركز الدراسة على بروتين غشائي يُسمى ريدوكتاز أول أكسيد النيتريك المعتمد على الكينول، أو qNOR، من البكتيريا المسببة للالتهاب السحائي Neisseria meningitidis. يقع qNOR في غشاء الخلية البكتيرية ويحوّل أول أكسيد النيتريك—وهو غاز سام تنتجه منظومة المناعة لدينا—إلى منتجات أقل ضررًا. تسمح هذه إزالة السمية للميكروب بمواصلة التنفس والنمو حتى داخل بيئات معادية مثل الخلايا البلعمية البشرية. وبما أن التنفس وإزالة أول أكسيد النيتريك ضروريان لبقاء الممرض، فإن qNOR يُعد هدفًا جذابًا لأدوية مضادة للميكروبات جديدة.
واحد جيد ولكن اثنان أفضل
أظهرت دراسات بيوكيميائية سابقة أن qNOR يمكن أن يوجد إما كوحدة مفردة (مونومر) أو كزوج (دايمر)، وأن الدايمر يعمل بمعدل أسرع بمقدار مرتين إلى أربع مرات في تحييد أول أكسيد النيتريك. حتى الآن، لم يكن واضحًا لماذا يؤدي مجرد اقتران نسختين من نفس الإنزيم إلى تأثير كبير على الأداء. للإجابة عن ذلك، استخدم الباحثون مجهر إلكتروني بالتبريد أحادي الجسيمات عالي الدقة لالتقاط هياكل ثلاثية الأبعاد مفصلة لكل من qNOR المونومري والدايمري من نفس السلالة البكتيرية. حصلوا على مشاهد بدقة قريبة من الذرية—1.89 أنغستروم للدايمر و2.25 أنغستروم للمونومر—حادة بما يكفي لتحديد سلاسل جانبية لأحماض أمينية منفردة، أيونات معدنية، والعديد من جزيئات الماء.
حلزون مرن يتحول إلى دعامة مثبتة
من المدهش أن قلب الإنزيم الحفاز—المركز المعدني حيث يتحول أول أكسيد النيتريك—بدى شبه مطابق في الشكل في كلا الصيغتين. وبدلاً من ذلك، ظهرت الفروقات الرئيسية على مسافة ما، في حلزون عبر الغشاء يُدعى TM10 وفي كيفية تلامسه مع حلزون آخر (TM2) عندما يتزاوج جزيئا qNOR. في المونومر، يكون TM10 مثبتًا بشكل فضفاض ويمكنه التأرجح والانحناء إلى حد كبير، كما كشفت تحليلات حسابية لبيانات المجهر الإلكتروني بالتبريد. في الدايمر، يقفل TM10 لكل شريك مقابل نظيره لتشكيل حزمة مكونة من أربعة حلزونات، مما يقيد حركته بشكل كبير. يؤدي هذا التثبيت إلى إعادة وضع طفيفة لحمض أميني حاسم، حمض الغلوتامات المسمى Glu563، ليقربه من غلوتامات أخرى (Glu494) بالقرب من الموقع الفعال ويُشكّل مسارًا أكثر تركيزًا للدونات البروتون اللازمة للتفاعل.
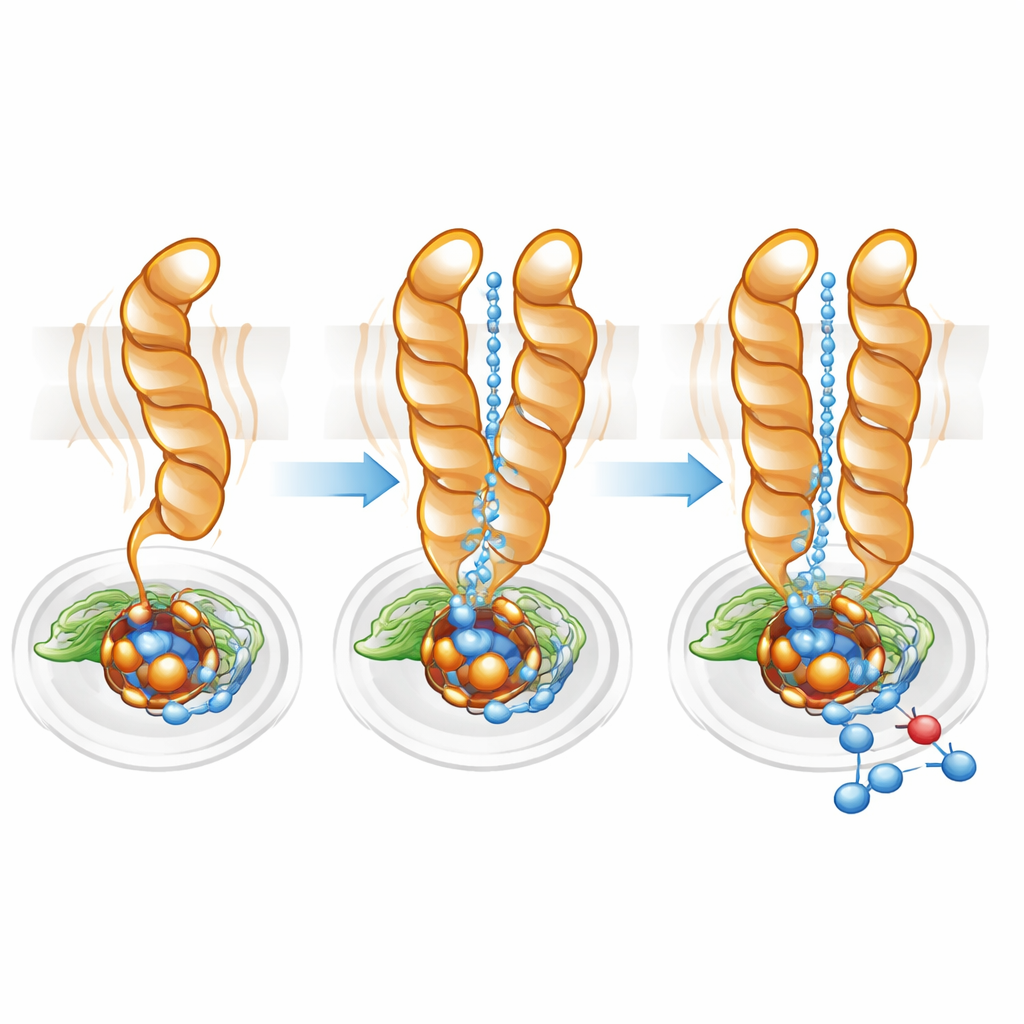
ضبط دقيق لطريق البروتون
يجب توصيل البروتونات—أيونات الهيدروجين موجبة الشحنة—بفعالية من داخل الخلية إلى الموقع الفعال المدفون حتى يتقدم اختزال أول أكسيد النيتريك. باستخدام برنامج لرسم مسارات النقل، وجد الفريق تجويفًا محبًا للماء يربط السيتوبلازم بالموقع الفعال في كل من المونومر والدايمر. ومع ذلك، في المونومر كان هذا القناة أوسع وأكثر تشتتًا، متسقًا مع الحركة الأكبر لـ TM10. في الدايمر، ساعدت وضعية TM10 المقفلة والاتجاه الملائم لـ Glu563 في تحديد مسار أكثر مباشرة وتنظيمًا. أدت طفرات تحول Glu563 إلى أحماض أمينية لا تستطيع تكوين نفس التفاعلات إلى خفض نشاط الإنزيم إلى أقل من 10% من المستوى الطبيعي كما زعزعت استقرار الدايمر، بينما قلّلت الطفرات في مواقع ذات صلة كمية الحديد غير الهيمي الضروري في الموقع الفعال. توضح هذه النتائج مجتمعة أن تكوين الدايمر والموضع الدقيق لـ Glu563 وGlu494 مرتبطان ارتباطًا وثيقًا بكل من السلامة البنائية والكفاءة الحفازة.
تحويل الاستنتاجات البنيوية إلى علاجات جديدة
تكشف النتائج خطًا واضحًا من اقتران البروتينات على سطح الغشاء إلى تعديلات دقيقة عميقًا داخل الموقع الفعال التي تتحكم في مدى فعالية qNOR في إزالة أول أكسيد النيتريك. ببساطة، عندما تتشابك نسختان من الإنزيم، تقومان بتقويم وتقييد مقطع مرن يساعد على توجيه البروتونات إلى مركز التفاعل، مما يعزز ناتجية الإنزيم. وبالنسبة لتطوير الأدوية، يشير ذلك إلى استراتيجية غير تقليدية: بدلاً من حجب الموقع الفعال مباشرة، يمكن تصميم جزيئات تفصل الدايمر أو تعطل تفاعل Glu563–Glu494، مما يجبر الإنزيم على الدخول في حالة المونومر البطيئة. ونظرًا لأن qNOR والإنزيمات ذات الصلة حاسمة لبقاء عدة ممرضات خطرة مقاومة للأدوية، فقد تسهم مثل هذه المناهج الموجهة ببنية البروتين في الجيل القادم من مضادات الميكروبات المستهدفة.
الاستشهاد: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
الكلمات المفتاحية: إزالة سمية أول أكسيد النيتريك, تنفس البكتيريا, إنزيمات غشائية, مجهر إلكتروني بالتبريد, أهداف أدوية مضادة للميكروبات