Clear Sky Science · ar
منشطات NRF2 ومثبط التصدير النووي سيلينيكسور تحدان من الفيروسات التاجية عبر استهداف شبكة تشمل ACE2 وTMPRSS2 وXPO1 بآلية مستقلة عن NRF2
أدوية تساعد الخلايا على قول “لا” للفيروسات التاجية
تتجه معظم العلاجات الحالية للفيروسات التاجية إلى استهداف الفيروس نفسه. لكن الفيروسات ماهرة في التغير، ويمكن للمتغيرات الجديدة أن تقلل بسرعة من فعالية هذه الأدوية. تبحث هذه الدراسة في استراتيجية مختلفة: جعل خلايانا أقل ترحيبًا بالفيروسات التاجية الخطرة مثل SARS-CoV-2 وأنواع المواسم الأخف. من خلال تعديل كيفية تعامل الخلايا مع بضعة بروتينات حارسة أساسية، يوضح الباحثون أن جزيئات صغيرة موجودة يمكن أن تقلل العدوى بشكل كبير في نماذج مخبرية، وتفعل ذلك بطريقة لا تعتمد على المسار المضاد للفيروسات الذي كانت معروفة به عادة.
زاوية جديدة في الدفاع ضد الفيروسات التاجية
ركز الفريق على مركبات معروفة بتنشيط برنامج حماية خلوي يتحكم به بروتين يسمى NRF2. هذه المركبات—4-أوكتيل إيتاكونيت (4OI)، باردوكسولون (BARD)، وسولفورافان (SFN)—اختبرت جنبًا إلى جنب مع سيلينيكسور (SEL)، دواء يعيق بروتين نقل يُسمى XPO1، الذي يساعد على إخراج بروتينات من نواة الخلية. في نماذج من خلايا الرئة والكلى، خفضت الأدوية الأربعة مستويات SARS-CoV-2 دون أن تضر الخلايا. كما عملت ضد عدة متغيرات مثيرة للقلق. بشكل مفاجئ، عندما أُزيل NRF2 وراثيًا، تكرر الفيروسات بشكل أفضل، ما يثبت أن NRF2 حمائي بطبيعته—لكن الأدوية استمرت في العمل جيدًا، مما يدل على أن فعاليتها المضادة للفيروسات تأتي عبر مسار مختلف. 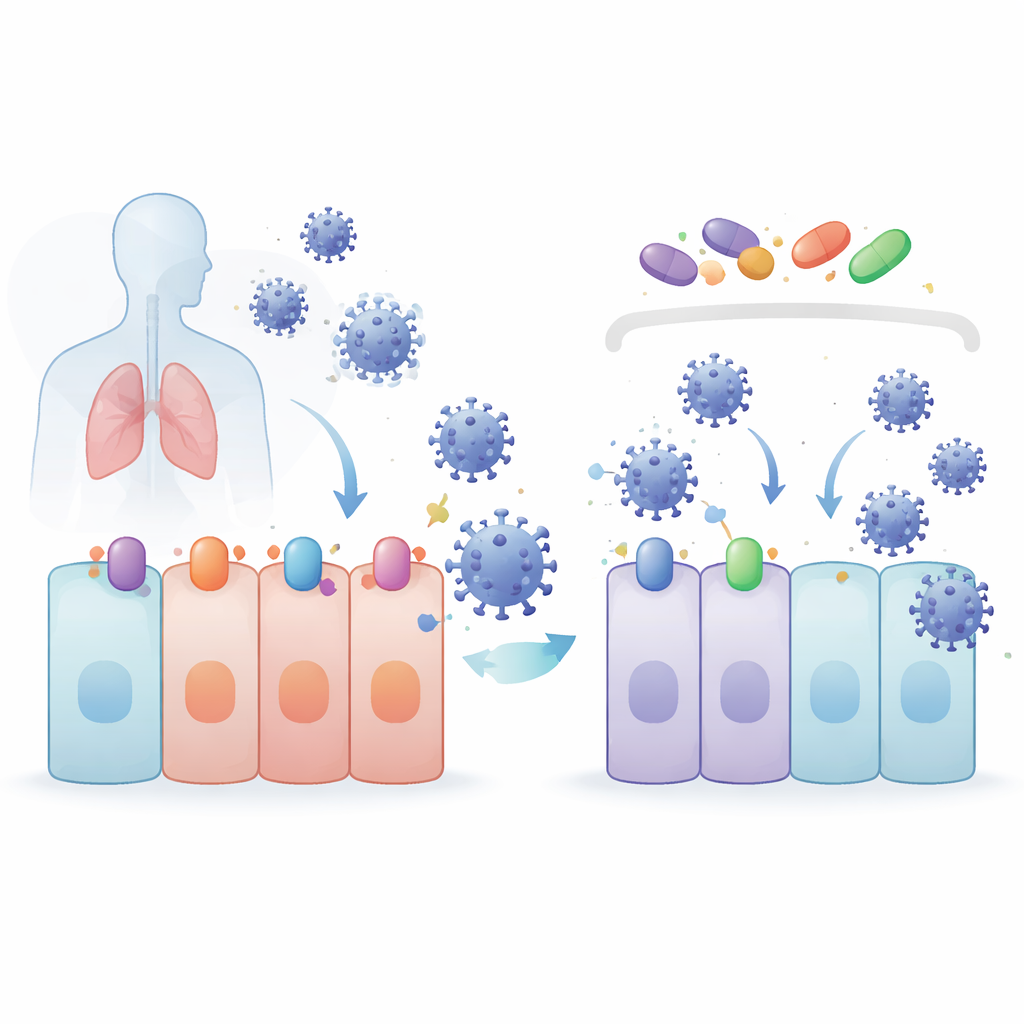
إغلاق الباب الأمامي للفيروس
تبدأ الفيروسات التاجية العدوى بالالتصاق ببروتينات مستقبلية على سطح الخلية. بالنسبة لـ SARS-CoV-2 وأقاربه، الباب الرئيسي هو ACE2، بمساعدة إنزيم قاطع يسمى TMPRSS2. ويبدو أن بروتين التصدير XPO1 يساهم أيضًا في العدوى. وجد الباحثون أن 4OI وBARD وSFN وSEL خفضت جميعها كميات ACE2 وTMPRSS2 وXPO1 في خلايا رئة بشرية. كان 4OI وSEL قويين بشكل خاص عند وجودهما قبل العدوى، وعرقلا دخول جزيئات شبيهة بالفيروس مغلفة ببروتينات سبايك للفيروس التاجي. بعبارة أخرى، هذه الأدوية لا تبطئ الفيروس فقط بعد دخوله—بل تساعد على إزالة الأقفال والمقابض التي يحتاجها الفيروس لفتح الباب في المقام الأول.
كيف تفكك الخلايا مساعدين فيروسيين رئيسيين
بالغوص أعمق، أظهر الفريق أن 4OI يُسرع تكسير بروتين ACE2. في الظروف العادية، يبقى ACE2 لساعات عديدة؛ مع 4OI، اختفى من سطح الخلية في جزء بسيط من ذلك الوقت. تطلّب هذا التدمير اثنين من وسمات الخلايا، NEDD4L وMDM2، اللتين تلصقان علامات «تخلص مني» جزيئية بالبروتينات. إعاقة هاتين الوسمتين أضعفت قدرة 4OI على إزالة ACE2. والمفاجئ أن آلية تكسير البروتين المعتادة، البروتيازوم، لم تكن المسار الرئيسي. بدلًا من ذلك، تم توجيه ACE2 إلى نظام إعادة التدوير والنفايات داخل الخلية، الليسوسوم. كما خفّضت الأدوية نشاط الجينات لـ ACE2 وXPO1، جزئيًا عن طريق تقليل تنشيط STAT3، وهو بروتين يعزز عادة قراءة جين ACE2. 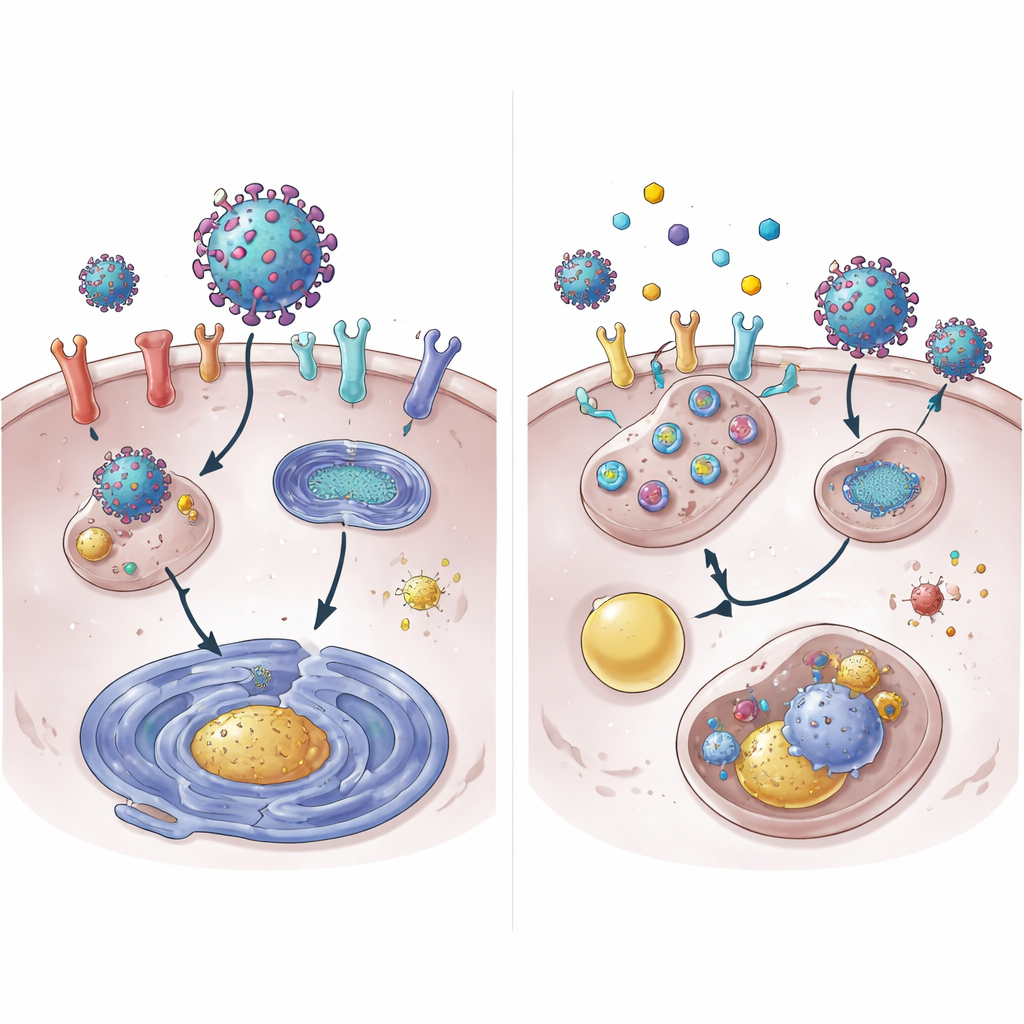
الفيروسات التاجية الموسمية وصلة XPO1
ثم توجه العلماء إلى hCoV-229E، فيروس تاجي موسمي يسبب عادة نزلات برد خفيفة لكنه قد يكون خطيرًا لدى ذوي المناعة الضعيفة. باستخدام فيروسات مهندسة تتوهج عند التكاثر، أظهروا أن المركبات الأربعة قمعت 229E بشدة في خلايا الرئة والأوعية الدموية، حتى عند غياب NRF2. على عكس SARS-CoV-2، يستخدم هذا الفيروس مستقبلًا مختلفًا، ANPEP، الذي لم تغيره الأدوية. بدلاً من ذلك، ارتبط تأثيرها ارتباطًا وثيقًا بمدى خفضها لـ XPO1. إنقاص مستوى XPO1 نفسه خفض تكرار 229E بشدة، وتأثير سيلينيكسور تكاد تزول في هذه الخلايا الفقيرة بـ XPO1. هذا الترتيب—اعتماد SEL الأكبر على XPO1 وBARD الأقل—يشير إلى أن لكل مركب توليفة مختلفة قليلًا من الأهداف، مع كون XPO1 محورًا مركزيًا للعديد من تأثيراتهم المضادة للفيروسات.
ماذا قد يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن من الممكن محاربة الفيروسات التاجية ليس فقط بمهاجمة الفيروس، بل بإعادة توصيل خلايانا بلطف حتى تصبح أصعب على العدوى. في خلايا بشرية مزروعة في المختبر، أزالت المركبات المدروسة مواقع الربط ومسارات المساعدة الأساسية التي يعتمد عليها SARS-CoV-2 وفيروس نزلة البرد الشائع، وفعلت ذلك إلى حد كبير بدون مسار NRF2 الذي أثار الاهتمام في البداية. وبينما لا تزال هذه النتائج قبل سريرية ولا تتحول مباشرة إلى أدوية بعد، فإنها تبرز مسارًا واعدًا: أدوية تخفض دخول الفيروس في آن واحد، وتخفف الالتهاب الضار، وتحمي الأنسجة عبر استهداف شبكة مشتركة من بروتينات المضيف مثل ACE2 وTMPRSS2 وXPO1.
الاستشهاد: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
الكلمات المفتاحية: مضادات الفيروسات الموجهة للمضيف, دخول الفيروس التاجي, ACE2 و TMPRSS2, منشطات NRF2, تثبيط XPO1