Clear Sky Science · ar
استراتيجية ثنائية الخطوات تعتمد على الأكتين تمكّن Campylobacter jejuni من تعزيز تجمّع الميتوكوندريا وتوازن الحديد، للبقاء داخل الخلايا والاستمرار
لماذا تهمّ هذه المعركة الصغيرة داخل الخلايا
التسمم الغذائي الناتج عن الدجاج غير المطهو جيداً يُعزى غالباً إلى بكتيريا تُدعى Campylobacter jejuni. يتعافى معظم الناس، لكن هذا الميكروب بارع بشكل مدهش في البقاء في بيئات متعددة، ما يساعده على الانتشار من المزرعة إلى المائدة. تبحث هذه الدراسة فيما يحدث عندما تختبئ البكتيريا داخل أميبا حرة العيش—وهي ميكروب مائي شائع—وتكشف عن حيلة بقاء متقنة تدور حول إعادة تشكيل الهيكل الداخلي للخلية، تجميع «محطات الطاقة» المولدة للطاقة المسماة الميتوكوندريا، والتحكم في الحديد والكيمياء المؤذية للأكسجين. قد يشير فهم هذه المرحلة الخفية من دورة حياة البكتيريا إلى طرق جديدة للحد من التلوث قبل أن تصل البكتيريا إلى البشر.
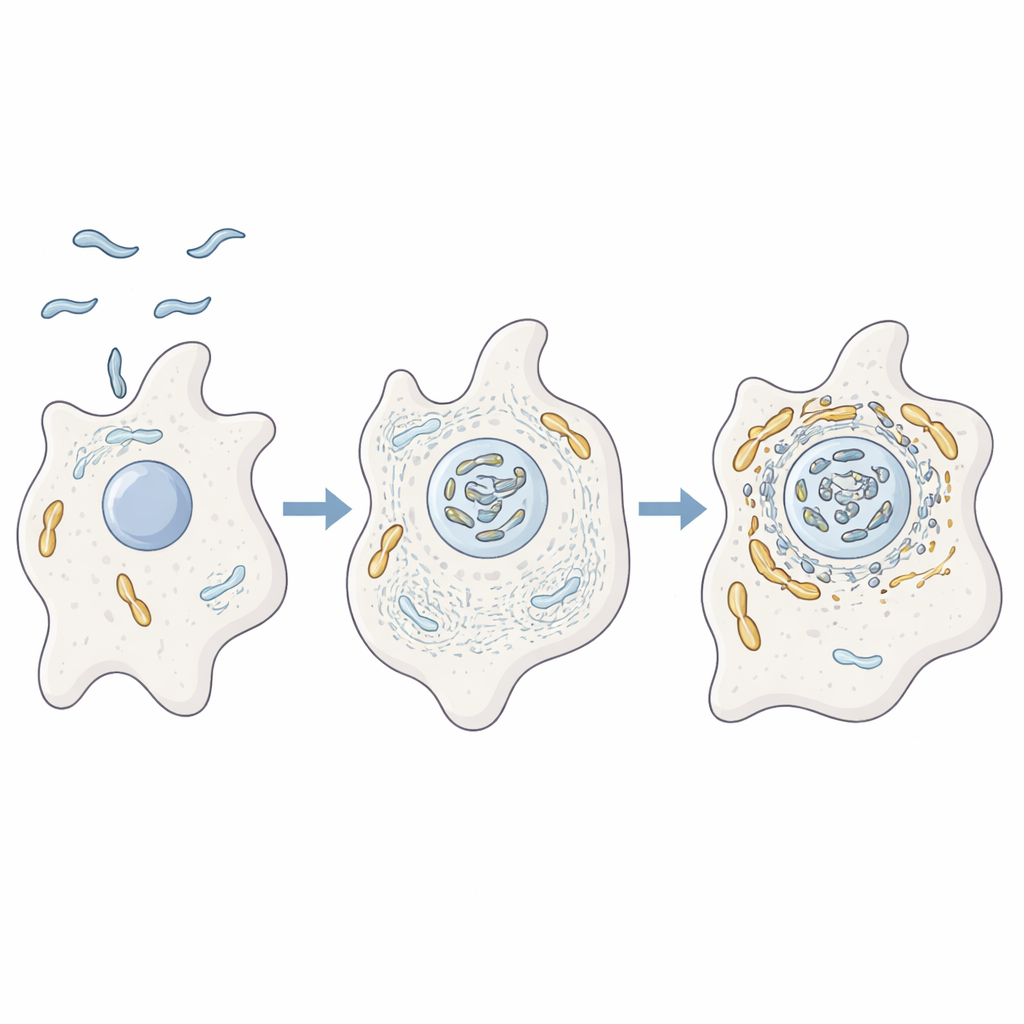
ميكروب يتدرّب داخل الأميبات
درس الباحثون سلوك C. jejuni داخل الأميبا Acanthamoeba castellanii، وهي كائن أحادي الخلية يعيش في التربة والمياه. تعمل هذه الأميبات كمواقع تدريب للعديد من البكتيريا الممرضة، حيث توفر حماية من الظروف القاسية والمطهرات. باستخدام تحليلات بروتينية متقدمة، والمجهر، وطفرات جينية، أظهر الباحثون أنه عندما تصيب C. jejuni الأميبات فإنها تنتهي مرتبطة ارتباطاً وثيقاً بميتوكوندريا العائل. في الوقت نفسه، كان السقالة الداخلية للأميبا المكوّنة من الأكتين، إلى جانب بروتينات تنظم شكلها وحركتها، مركزة بقوة بالقرب من هذه الميتوكوندريا، ما يوحي بأن البكتيريا تعيد ترتيب العمارة الداخلية لخلية العائل بنشاط.
ثني هيكل الخلية لنقل محطات الطاقة
لاختبار ما إذا كان الأكتين يقود فعلاً هذا التفاعل، قام الفريق بعرقلة تكوين خيوط الأكتين أو تفرعها إلى شبكات. تحت هذه الظروف، لم تعد الميتوكوندريا تتجمع بالقرب من البكتيريا وبقيت بدلاً من ذلك على شكل نقاط متناثرة، كما انخفضت بقاء البكتيريا. ثم ركزوا على بروتينين مساعدين بكتيريين، CiaD وCiaI، اللذين يُحقَنَان في خلايا العائل عبر السوط البكتيري، ذي الشكل الشوكي. تبين أن CiaD يعزز نمو الأكتين ويُشجّع بروزات شوكية على سطح الأميبا، مما يساعد الخلية على التقاط البكتيريا. وبعد أن تدخل البكتيريا، رُصِدت الميتوكوندريا متجمعة حول الحجرة الحاوية للبكتيريا بطريقة تعتمد على الأكتين، واضعة البكتيريا في منطقة مميزة غنية بآلات طاقة العائل.
مفتاح جزيئي يعيد تشكيل الميتوكوندريا
بينما يعد CiaD مفتاحاً للدخول، يتحكم CiaI فيما يحدث بعد ذلك. عندما حذف الباحثون جين CiaI، لم تعد C. jejuni تحفّز تجمّعاً قوياً للميتوكوندريا وبقيت تعيش بشكل ضعيف داخل الأميبات. إضافة CiaI منقى وملتصق بخرزات صغيرة، دون أي بكتيريا حية، كانت كافية للتسبب في اندماج الميتوكوندريا وتجمعها محلياً وإزالة الأكتين محلياً. أظهرت اختبارات كيميائية حيوية أن CiaI يرتبط بجزيئات ناقلة للطاقة بطريقة تعاونية، متصرفاً كمفتاح جزيئي قد يشغل أو يوقف نشاطه اعتماداً على الظروف داخل العائل. يقترح المؤلفون أنه بعد أن يؤدي نمو الأكتين المدفوع بـCiaD إلى تقريب الميتوكوندريا، يدفع CiaI تحلل الأكتين محلياً ويعيد تشكيل شبكة الميتوكوندريا إلى تجمعات كثيفة تحيط بالحجرة المحتوية على البكتيريا.
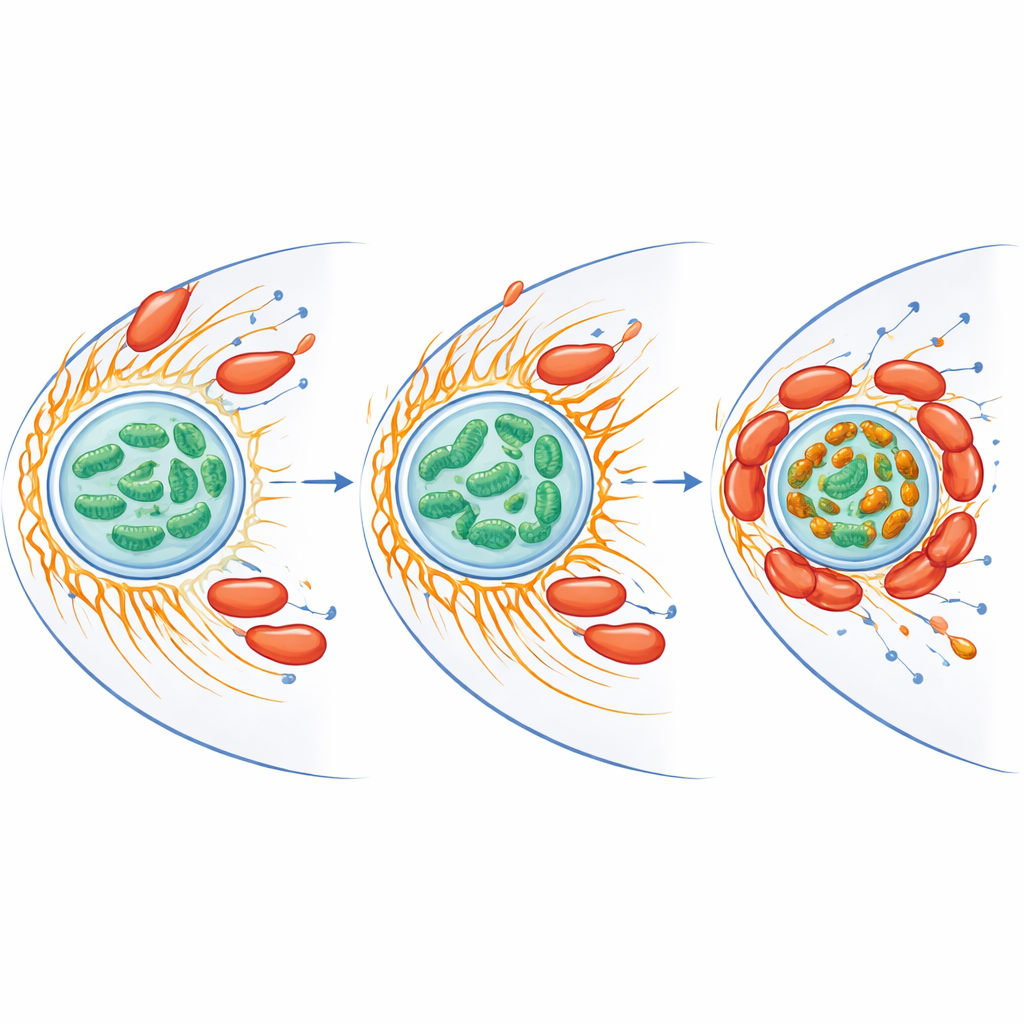
إعادة توصيل الحديد والإجهاد داخل خلية العائل
لا تقتصر وظيفة الميتوكوندريا على توليد الطاقة—فهي أيضاً تتعامل مع الحديد وتنتج أنواع أكسجين تفاعلية، أشكال كيميائية عدوانية من الأكسجين يمكن أن تقتل الميكروبات. وجد الباحثون أن العدوى قللت من إجمالي الحديد الحر داخل الميتوكوندريا، ولكنها في الوقت نفسه خلقت تجمعات لامعة غنية بالحديد حيث تجمعت الميتوكوندريا حول البكتيريا. ارتفعت بروتينات مشاركة في تداول الحديد وفي الدفاع ضد الإجهاد التأكسدي في كل من العائل والبكتيريا. عندما أزالت المجموعة الحديد الحر باستخدام مركب مخلّب، انخفض اندفاع أنواع الأكسجين التفاعلية لدى الأميبا وارتفع بقاء C. jejuni بشكل كبير. كما أظهرت الميتوكوندريا في الخلايا المصابة فرقاً أعلى في الجهد الغشائي، وهو علامة على نشاط متزايد، ما يقترح أن البكتيريا تدفع محطات طاقة العائل إلى حالة تفضل استمرارها مع الحد من الكيمياء المؤذية للأكسجين.
ما معنى هذا لسلامة الغذاء والعدوى
تدعم النتائج مجتمعة استراتيجية من خطوتين: أولاً، يحفز CiaD نمو الأكتين لمساعدة البكتيريا على دخول الأميبات وسحب الميتوكوندريا نحو موقع الدخول؛ ثانياً، يقوم CiaI بتفكيك الأكتين محلياً ويعيد تشكيل الميتوكوندريا إلى تجمعات غنية بالحديد ملفوفة حول الحجرة الحاوية للبكتيريا، مع تثبيط دفاعات العائل التأكسدية. يساعد هذا التحكم الدقيق في شكل الخلية واستخدام الطاقة وتوازن المعادن C. jejuni على البقاء داخل الأميبات ومن المحتمل أن يسهِم في قدرته على الاستمرارية في البيئة ثم إصابة البشر لاحقاً. من خلال الكشف عن اللاعبين الرئيسيين في هذه المنازلة المجهرية، تشير الدراسة إلى أهداف جديدة—مثل بروتينات Cia، وصلات الأكتين-الميتوكوندريا، أو مسارات تداول الحديد—يمكن تعطيلها لتقليل التلوث والمرض.
الاستشهاد: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
الكلمات المفتاحية: كامبيلوباكتر, أميبا, الميتوكوندريا, هيكل الأكتين الخلوي, توازن الحديد