Clear Sky Science · ar
إساءة استخدام المخدرات الإدمانية والاكتئاب — تركيز على علم فوق الجينات
لماذا يهم هذا البحث في الحياة اليومية
غالباً ما يُعالج تعاطي المخدرات الإدمانية والاكتئاب كمشكلتين منفصلتين، مع ذلك فهما كثيراً ما يظهران معاً عند نفس الشخص. توضح هذه المراجعة كيف أن الاستخدام طويل الأمد لمخدرات مثل الميثامفيتامين، والكوكايين، والمخدرات الأفيونية، والقنب يمكن أن يترك "ندوبًا جزيئية" دائمة في الدماغ تزيد من خطر الاكتئاب. ومن خلال كشف هذه التغيرات الخفية، يشير المقال إلى اختبارات مستقبلية قد تحذر من هم الأكثر عرضة — وعلاجات أكثر دقة قد تعكس الضرر بدلاً من مجرد إخفاء الأعراض.
كيف يتشابك الإدمان والحالة المزاجية المنخفضة
يبدأ المؤلفون بتوضيح الصلة السريرية الوثيقة بين تعاطي المخدرات والاكتئاب. الأشخاص الذين يستخدمون المواد الإدمانية بشكل متكرر هم أكثر عرضة للإبلاغ عن حزن مستمر، فقدان المتعة، اضطرابات النوم، وأفكار انتحارية. المناطق الدماغية التي تتحكم بالمكافأة، والدافع، والذاكرة، واتخاذ القرار — مثل المنطقة البرية الهابطة (ventral tegmental area)، والنواة المتكئة (nucleus accumbens)، والقشرة الجبهية الأمامية، والحصين — هي محورية في كلتا الحالتين. يتسبب التعرض المزمن للمخدرات في اضطراب كيمياء الدماغ مثل الدوبامين والسيروتونين، وهرمونات التوتر التي يتحكم بها محور ما تحت المهاد — الغدة النخامية — الكظرية، وإشارات الجهاز المناعي، وإمداد الطاقة للخلايا العصبية. معاً تجعل هذه التغيرات الدماغ أقل قدرة على التكيف مع التوتر وأكثر ميلاً للحالات الاكتئابية، حتى بعد فترة طويلة من آخر جرعة.
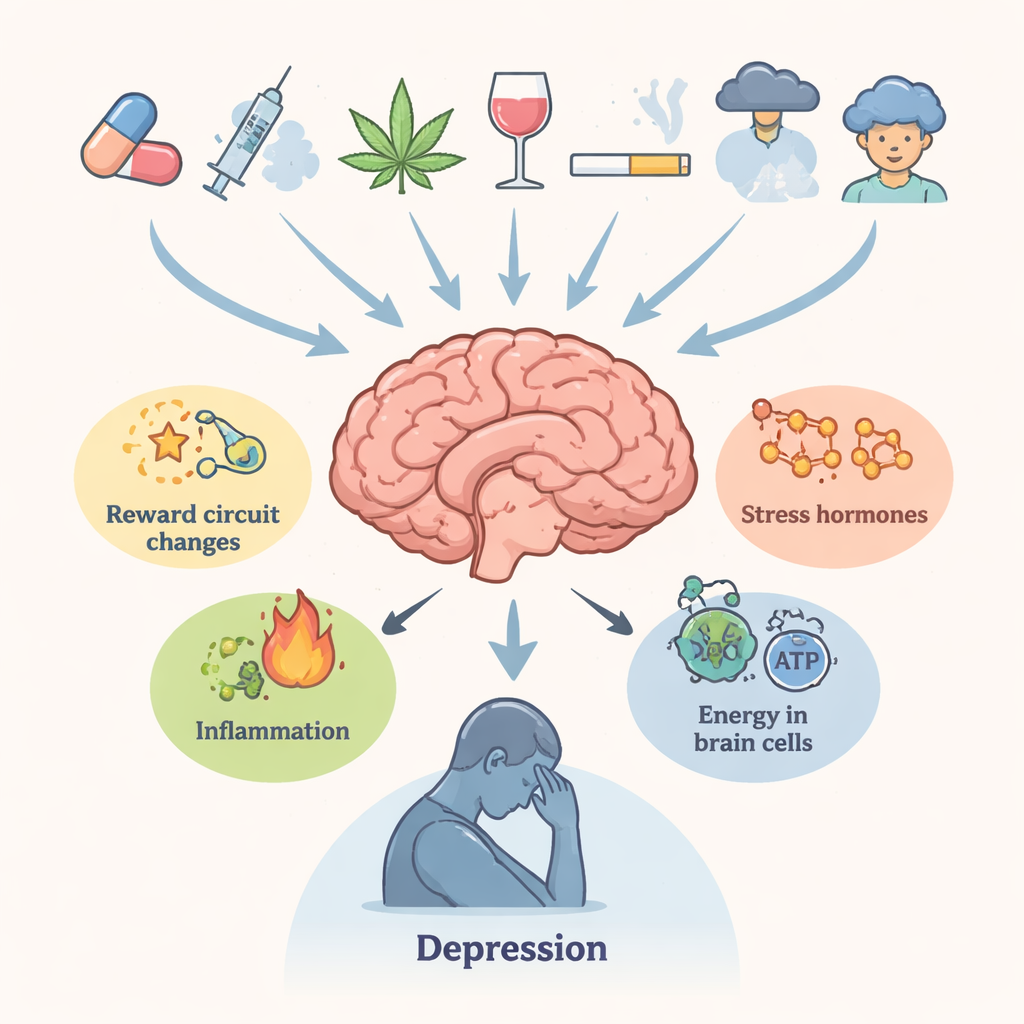
مخدرات تعيد تشكيل كيمياء الدماغ
تستعرض المراجعة عدة فئات رئيسية من المخدرات. المنبهات من نوع الأمفيتامين وأقاربها، بما في ذلك المركبات الاصطناعية المعروفة باسم "أملاح الحمام"، تُحدث اندفاعات قوية من الدوبامين وناقلات عصبية أخرى والتي، بمرور الوقت، تُتلف النهايات العصبية، وتعطل توازن الغلوتامات، وتجهد الشبكة البلازمية الداخلية (الشبكة داخل الخلوية)، وتدفع الخلايا نحو هضم ذاتي مضر (الالتهام الذاتي). يرتبط تعاطي القنب في مرحلة المراهقة بالاكتئاب لاحقًا وخطر الانتحار، على الأرجح عبر تغييرات طويلة الأمد في مستقبلات الكانابينويد، وتركيب المادة البيضاء، وحساسية دوائر الدوبامين. يمكن للمخدرات الأفيونية، رغم تخفيفها للألم، أن تحفز الالتهاب، وفشل الميتوكوندريا، وانخفاض إشارات دعم النمو مثل عامل التغذية العصبية المشتق من الدماغ (BDNF). ينشط الكوكايين مراراً نظام التوتر ويغير منظِّمات رئيسية مثل FKBP5، مما يساهم في القلق والمزاج المنخفض أثناء الانسحاب. في كل حالة، تميل الاضطرابات البيولوجية إلى الاستمرار، مما يفسر لماذا قد تستمر الأعراض العاطفية بعد زوال حالة السمّية الواضحة.
علم فوق الجينات: ذاكرة التعرض
لفهم سبب بقاء تأثيرات المخدرات، يركز المؤلفون على علم فوق الجينات — العلامات الكيميائية والمفاتيح الجزيئية التي تضبط نشاط الجينات دون تغيير أحرف الحمض النووي. تُعدّل المخدرات الإدمانية مثيلة الحمض النووي (علامة على قواعد السيتوزين)، وتغير مجموعات كيميائية على بروتينات الهيستون التي تغلف الحمض النووي، وتغيّر الأحماض النووية غير المشفرة التي تضبط دقة أي البروتينات تُنتج. على سبيل المثال، يحوّل الميثامفيتامين والكوكايين أنماط المثيلة في مناطق الدماغ المرتبطة بالمكافأة، مغيرين مستويات الإنزيمات التي تضيف أو تزيل هذه العلامات. تعيد الأفيونات والمنشطات تشكيل أسيتلة وميثلة الهيستونات على جينات تتحكم بمستقبلات الغلوتامات، وإشارات التوتر، وبنية المشابك. ترتفع أو تنخفض عشرات الميكروRNA، والأحماض النووية الطويلة غير المشفرة، والأحماض النووية الدائرية مع التعرض للمخدرات، مؤثرة جماعياً في الالتهاب، ونمو الخلايا العصبية، وقوة المشابك. تعمل هذه التغيرات فوق الجينية كـ"ذاكرة" جزيئية لتاريخ التعرض للمخدرات.
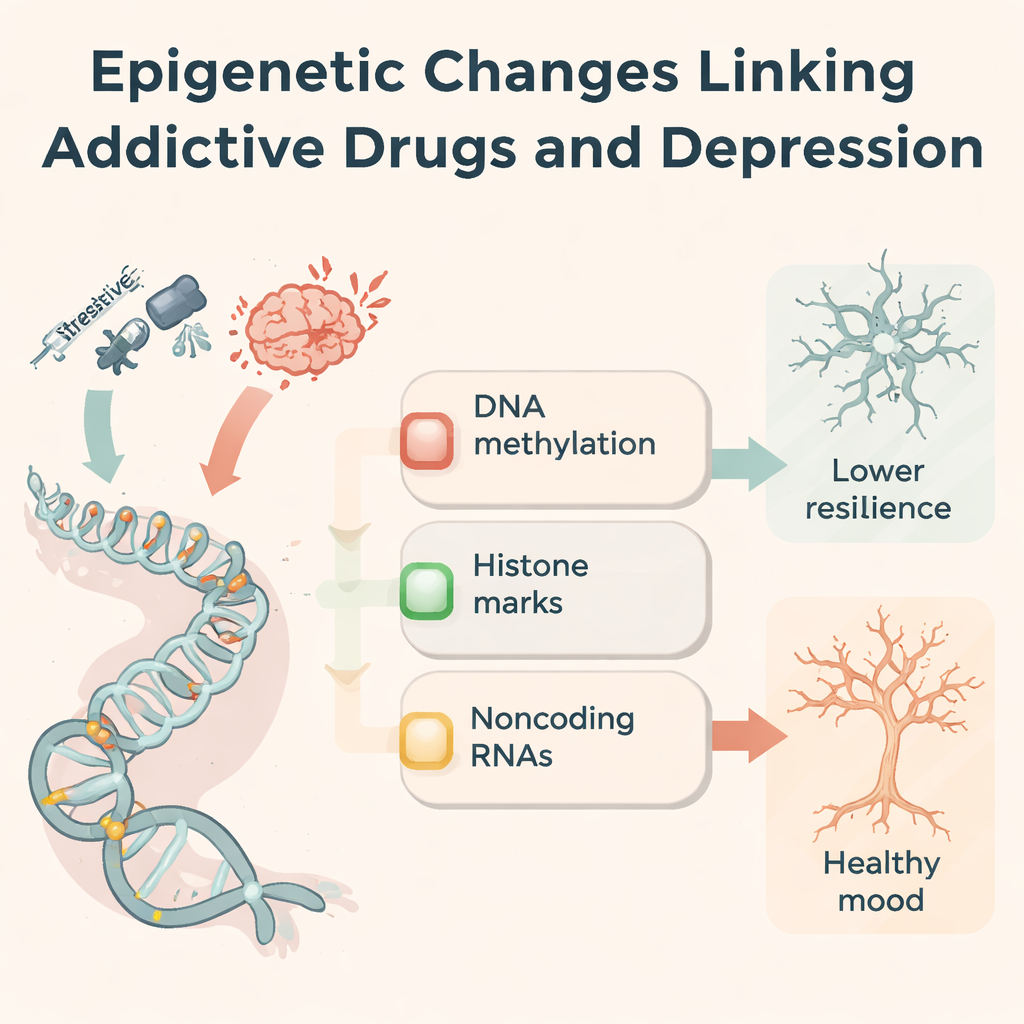
مسارات جزيئية مشتركة في الاكتئاب والإدمان
تظهر نفس آليات فوق الجينات أيضاً في البشر والحيوانات المصابين بالاكتئاب الذين لم يتعاطوا مخدرات قط. يمكن للتجارب المجهدة أن تغير مثيلة مستقبلات هرمونات التوتر (مثل NR3C1 وFKBP5)، وتقلل عوامل النمو المفيدة مثل BDNF، وتعيد توصيل مسارات المناعة والغلوتامات. العديد من الأحماض النووية غير المشفرة التي تغيرها المخدرات تُشوه أيضاً في الاكتئاب، مؤثرة على كيفية ولادة الخلايا العصبية الجديدة، وكيفية استجابة الخلايا الدبقية الصغيرة للالتهاب، ومدى قوة توصيل المشابك. يقترح المؤلفون إطاراً ثلاثي الأجزاء: تنظيم استجابة التوتر، وإعادة تشكيل دوائر المكافأة، واللدونة المشبكية. عبر هذه المحاور، يتقاطع الإدمان والاكتئاب مراراً على مجموعة صغيرة من الجينات والعلامات، ما يشير إلى سبب بيولوجي لحدوث الاضطرابين معاً في كثير من الأحيان.
ماذا يعني هذا للوقاية والعلاج المستقبلي
في الخاتمة، يجادل الاستعراض بأن التغيرات فوق الجينية يمكن أن تصبح مؤشرات مبكرة للتحذير وأهدافاً للعلاجات القادمة. لقد أظهرت أدوية واسعة التأثير تمسح العلامات فوق الجينية بعض التأثيرات الشبيهة بمضادات الاكتئاب في الحيوانات، لكنها خامّة جداً لاستخدام روتيني لدى البشر. قد تضبط أدوات جديدة — مثل محررات فوق الجينوم المستندة إلى CRISPR وعلاجات تعدل ميكروRNA أو الأحماض النووية الطويلة المحددة — يوماً ما الجينات الإشكالية في خلايا دماغية بعينها مع الحفاظ على الخلايا الأخرى. ويحذر المؤلفون أن معظم البيانات الحالية جاءت من القوارض وأنسجة دماغية مجمعة، وأن البيولوجيا البشرية أكثر تعقيداً. ومع ذلك، من خلال كشف كيف يكتب الإدمان والاكتئاب في نفس "دفتر الملاحظات" الجزيئي، يقدم هذا العمل مساراً واعداً نحو علاجات أكثر تخصيصاً وديمومة.
الاستشهاد: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
الكلمات المفتاحية: الإدمان والاكتئاب, علم فوق الجينات, تعاطي المخدرات, مثيلة الحمض النووي, الحمض النووي غير المشفر RNA