Clear Sky Science · ar
إثبات المبدأ لعلاج جيني لجين NF1 في نماذج فأرية مزروعة لأورام الورم العصبي الضفيري
لماذا يهم هذا البحث
غالبًا ما يطوّر الأشخاص المصابون بالاضطراب الوراثي اعتلال العصب الليفي من النوع 1 (NF1) أورامًا عصبية كبيرة ومشوهة تُسمى الأورام العصبية الضفيرية. يمكن أن تسبب هذه الأورام ألمًا ومشاكل في الحركة ومخاوف تجميلية كبيرة، ومع ذلك فإن خيارات العلاج الحالية محدودة وغالبًا ما تكون الجراحة مستحيلة. بما أن NF1 ناتج عن تغيّر في جين واحد، فقد راجت لدى كثير من الباحثين فكرة أن العلاج الجيني—إصلاح أو استبدال الجين المعيب—قد يقلّص هذه الأورام أو يقضي عليها يومًا ما. يقدم هذا الورق اختبارًا مبكرًا لكنه قويًا لتلك الفكرة في الفئران، مطروحًا سؤالًا بسيطًا ذو تبعات كبيرة: إذا أعدت تشغيل جين NF1 المفقود في الأورام القائمة، هل تختفي هذه الأورام؟
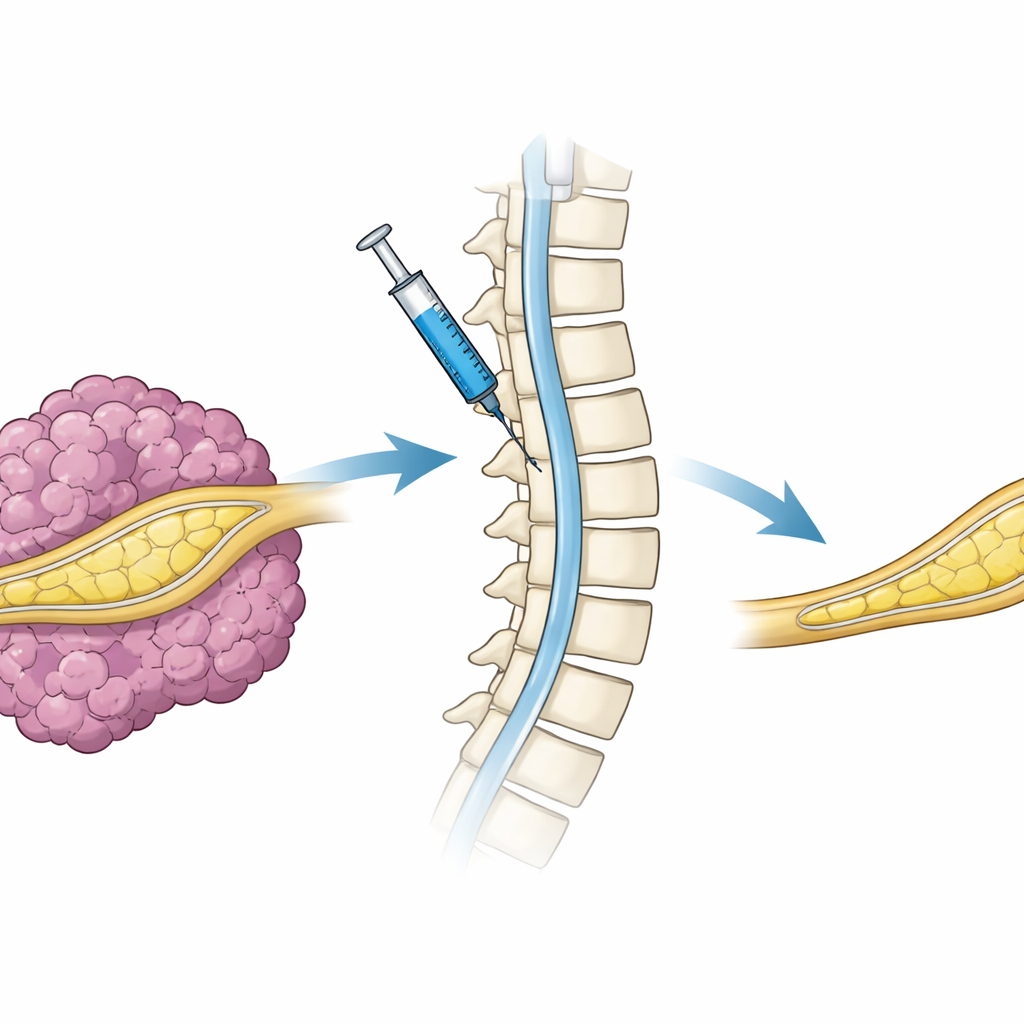
بناء نموذج ورمي واقعي في الفئران
كان على الباحثين أولاً إنشاء نظام مخبري يحاكي الأورام العصبية الضفيرية البشرية عن كثب. استخدموا خلايا شوان بشرية—الخلايا الداعمة التي تلتف عادة حول الأعصاب—أُخذت من مريض فقدت خلاياه النسختين العاملتين من جين NF1. وُضعت هذه الخلايا بجوار أعصاب الورك المصابة في فئران ناقصة المناعة. على مدى أسابيع، طورت الأعصاب نسيجًا سميكًا عالي الكثافة مع بنية غير منظمة وأشرطة كولاجين كثيفة—وهي سمات مميزة للأورام العصبية الضفيرية. لم تؤدِّ العمليات الضابطة التي لم تتضمن هذه الخلايا الناقصة NF1، أو استخدام خلايا بها نسخة واحدة معيبة من NF1، إلى تكوّن أورام بشكل موثوق. أظهر ذلك أن الخلايا البشرية التي فقدت NF1 تمامًا كانت المحرّك لنمو الورم وأنشأت نموذجًا قويًا وسريعًا للمرض.
إعادة تشغيل NF1 في خلايا الورم
مع هذا النموذج، مهندَس الفريق خلايا شوان المكوِّنة للأورام لتحمل نسخة قابلة للتشغيل من جين NF1 مأخوذة من الفئران. كانت آلية التشغيل تستجيب للمضاد الحيوي المعروف دوكسيسيكلين: عندما شربت الفئران ماءً يحتوي على دوكسيسيكلين، انطفأت/اشتغلت إضافة جين NF1 في الخلايا المزروعة (عند إعطاء الدواء شغِلت الجين). سُمح للفئران أولًا بتطوير الأورام، ثم شُغّل الجين فقط بعد ذلك. وكانت النتائج لافتة. في الحيوانات التي ظل فيها NF1 متوقفًا، احتوت غالبية أعصاب الورك على أورام عصبية. بالمقابل، عند إعادة تنشيط NF1، بدا معظم الأعصاب طبيعيًا تحت المجهر، وانخفضت مؤشرات الكيمياء الحيوية للإشارات المرتبطة بنمو مفرط بشكل كبير. باختصار، دفع إعادة تشغيل NF1 نسيج الورم نحو حالة عصبية صحية.
عكس فقدان NF1 بطريقة ثانية
لإظهار أن هذا التأثير لم يقتصر على حيلة هندسية واحدة، أنشأ العلماء نموذجًا ثانويًا مكملًا. في هذه المرة بدأوا بخلايا شوان بشرية كانت تملك نسخة واحدة تالفة من NF1—مماثل لما يرثه الأشخاص المصابون بـNF1 في خلاياهم جميعًا. أضافوا مفتاحًا جينيًا يمكنه خفض النشاط المتبقي لـNF1 مؤقتًا عند وجود دوكسيسيكلين. عندما شربت الفئران دوكسيسيكلين، انخفضت مستويات NF1 أكثر وتكوّنت الأورام بسهولة. والأهم من ذلك أنه عندما أُزيل الدوكسيسيكلين بعد نمو الأورام، عادت مستويات NF1 للارتفاع وعادت العديد من الأعصاب إلى بنية أقرب إلى الطبيعية. مرة أخرى، انخفضت مؤشرات الإشارات المرتبطة بالنمو في الأعصاب التي عادت إلى وضع طبيعي. معًا، تشير هاتان الاستراتيجيتان المتعاكستان—إما تشغيل NF1 أو إيقاف قمعه—إلى نتيجة واحدة: إن استعادة NF1 في خلايا الورم يمكن أن يبدل المرض القائم.
اختبار نهج توصيل أكثر واقعية
بعيدًا عن المفاتيح الجينية المدمجة في الخلايا في المختبر، سيتطلب العلاج الحقيقي توصيل جين NF1 العامل إلى الجهاز العصبي للمريض الحي. للاستكشاف في هذا الاتجاه، عبأ الباحثون الجين الكامل NF1 في ناقل لنتيفيروسي وحقنوه في الفراغ السائلي حول الحبل الشوكي للفئران الحاملة للأورام، وهو مسار يُعرف بالتوصيل داخل الجافية (intrathecal). ثم تلقت الحيوانات دوكسيسيكلين لكي ينشط الجين الموصل. مقارنةً بالفئران التي أعطيت فيروسًا تحكمياً، طوّرت الفئران المعالجة بالفيروس الحامل لـNF1 عددًا أقل بكثير من الأورام، وبدا نسيج أعصابها أكثر طبيعية. وعلى الرغم من أن هذه تجربة قصيرة بجرعة واحدة، فقد برهنت أن توصيل جين NF1 عبر سائل النخاع الشوكي يمكنه الوصول إلى الأعصاب المحيطية وتقليل عبء الورم بشكل ملموس.
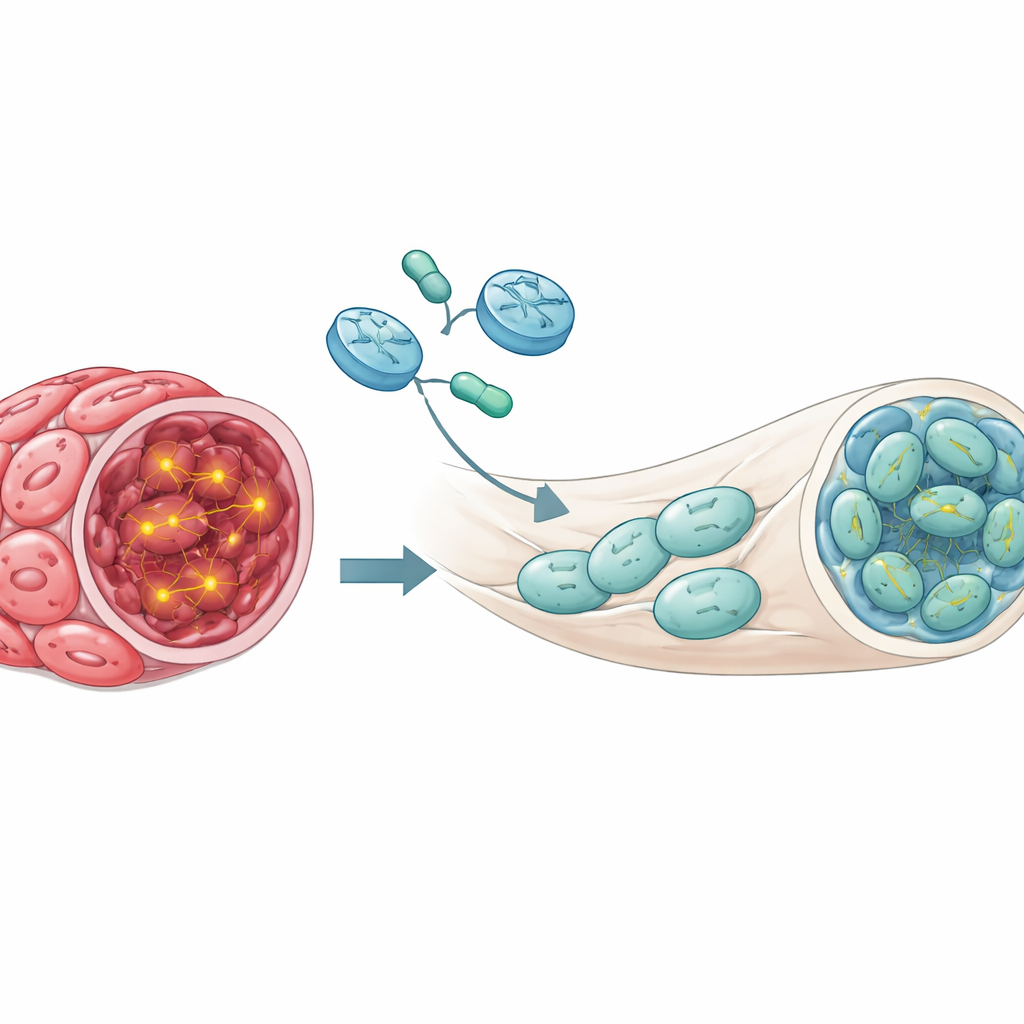
ماذا يعني هذا العمل للأشخاص المصابين بـNF1
لا يقدم هذا البحث حتى الآن علاجًا جاهزًا للمرضى، لكنه يجيب على سؤال حاسم: في نماذج فأرية مصممة بعناية تُشبه أورام الورم العصبي الضفيري البشرية، يمكن لاستعادة NF1 في خلايا الورم أن تقلّص أو تطبّع الأورام القائمة. يوفر العمل إثبات مبدئيًا أن العلاج الجيني لـNF1 استراتيجية معقولة وليست مجرد أمل نظري. تبقى تحديات كثيرة—إيجاد ناقلات آمنة وفعالة، تحديد مقدار نشاط NF1 الكافي، واختبار التأثيرات طويلة المدى في نماذج أكثر طبيعية. ومع ذلك، تضع هذه النتائج أساسًا علميًا لعلاجات مستقبلية معتمدة على الجين قد توفّر يومًا ما راحة دائمة من الأورام العصبية الضفيرية لدى الأشخاص المصابين بـNF1.
الاستشهاد: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
الكلمات المفتاحية: اعتلال العصب الليفي من النوع 1, العلاج الجيني, الورم العصبي الضفيري, خلايا شوان, توصيل لنتيفيروسي