Clear Sky Science · ar
فشل الطاقة الميتوكوندرية يكمن وراء الاعتلال العصبي الحسي المرتبط بـ FLVCR1
عندما تنفد طاقة أعصاب الألم
يولد بعض الأشخاص مع قدرة شبه منعدمة على الشعور بالألم. قد يبدو ذلك في الوهلة الأولى نعمة، لكنه سرعان ما يتحول إلى نقمة: فبدون الألم كإشارة تحذير، يتعرضون لحروق وكسور وعدوى وحتى فقدان البصر. تستقصي هذه الدراسة شكلاً نادراً من اضطرابات فقدان الألم وتكشف عن سبب مفاجئ: مصانع طاقة صغيرة داخل خلايا الأعصاب تعجز عن إنتاج الطاقة كما ينبغي.
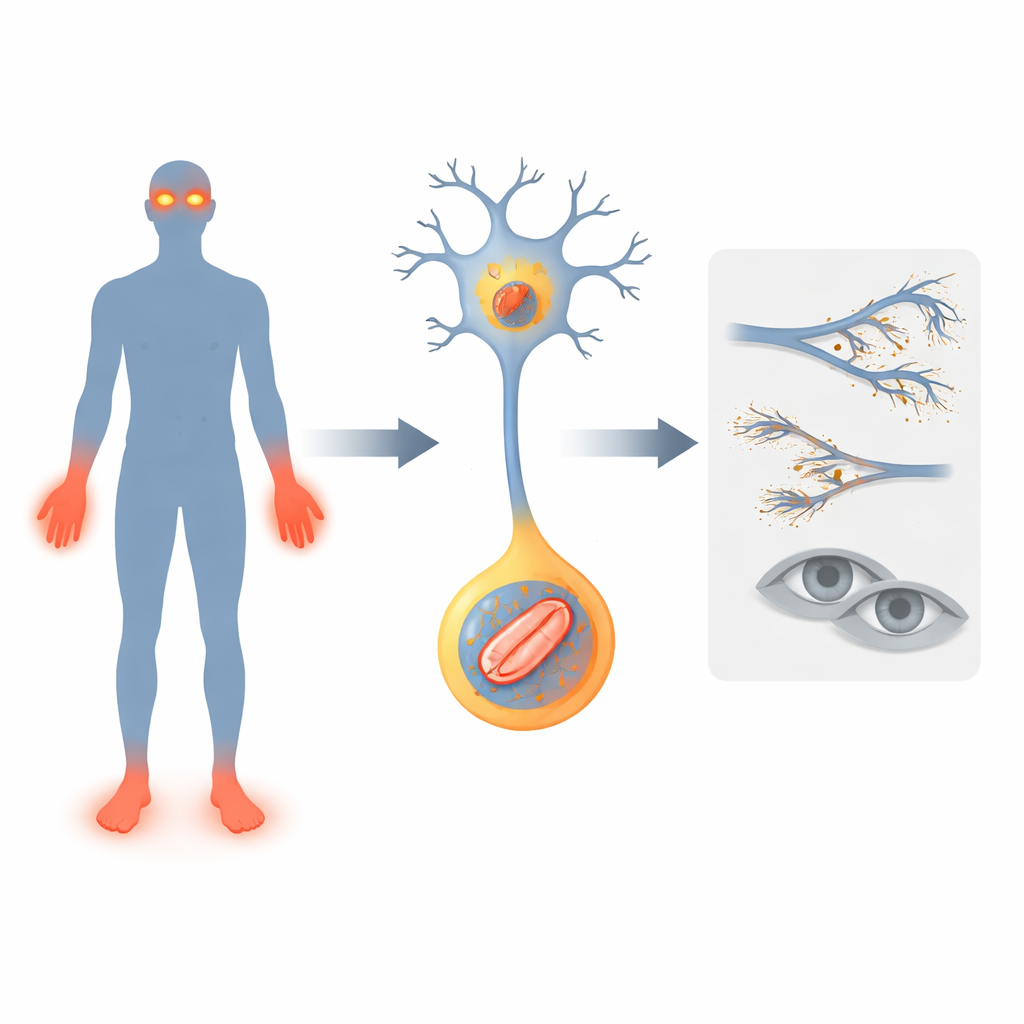
جينة تُسكت أجراس الإنذار
ركز الباحثون على جين يدعى FLVCR1، المرتبط بالفعل بحالات نادرة تفقد فيها الناس إحساس الألم، ويطورون مشية غير ثابتة وفي بعض الأحيان فقدان رؤية تقدمي. يصفون حالتين جديدتين تحملان طفرات في FLVCR1. أظهر كلا الطفلين مشاكل مبكرة: تأخر في محطات الحركة، سقوط متكرر، عدوى عميقة وتشويه الأصابع وأطراف الأصابع لأن الإصابات ظلت دون ملاحظة. كما أصيب أحدهما بمرض تنكسي في العين يُدعى التهاب الشبكية الصباغي، مما أدى إلى العمى الليلي. توسع هذه الحالات الصورة السريرية لخلل FLVCR1 وتدعم الفكرة القائلة إن هذا الجين حيوي لبقاء الأعصاب الحاسة للألم والخلايا الحساسة للضوء في الشبكية.
نمذجة المرض في أسماك صغيرة
لاستكشاف كيفية تأثير FLVCR1 على الأعصاب الحسية النامية، لجأ الفريق إلى سمك الزرد، الذي تسمح أجنته الشفافة بمشاهدة خلايا الأعصاب مباشرة. خفضوا مستويات النسخة السمكية من الجين، flvcr1a، باستخدام أدوات جينية. أظهرت الأسماك ذات مستويات منخفضة من flvcr1a عددًا أقل من عقيدات الجذور الظهرية، وهي تجمعات عصبية تكتشف اللمس والألم على طول العمود الفقري. سلوكياً، تحركت هذه الأسماك أقل بمبادرة منها وسبحت لمسافات قصيرة فقط عندما لُمس ذيلها برفق، ما يشير إلى استجابة حسية مخففة. وبما أن نماذج الفئران السابقة كانت تموت مبكراً قبل تحليل أعصابها الحسية، توفر أسماك الزرد نظامًا حيًا أولياً يمكن متابعة عيوب الأعصاب والسلوك المرتبطة بـ FLVCR1 فيه بالتفصيل.
تلاقي ثلاث مسارات مضطربة على مصانع الطاقة الخلوية
يقع FLVCR1 في أغشية الخلايا ويدير عدة مواد رئيسية. أشارت أعمال سابقة إلى أدوار في التعامل مع الكولين (مكون لبناء دهون الغشاء)، والهيـم (الصبغة المحتوية على الحديد التي تُشغل العديد من الإنزيمات) وتدفق الكالسيوم بين مقصورات الخلية. جمع العلماء خلايا جلد (خلايا ليفية) من أربعة مرضى يحملون طفرات مختلفة في FLVCR1 وقارنوها بخلايا من أشخاص أصحاء وحاملين بلا أعراض. وجدوا أن خلايا المرضى تحتوي على مستويات أقل من الكولين وأغشية خلوية أكثر سيولة، تغييرات قد تقوض البيئة الدهنية الحساسة التي تحتاجها الميتوكوندريا، العضيات المولدة للطاقة. كما اكتشفوا أن إنزيمًا حاسمًا لصنع الهيـم داخل الميتوكوندريا، ALAS1، كان أقل نشاطًا، رغم أن كمية الهيـم الإجمالية بدت قريبة من الطبيعي. في الوقت نفسه، كانت مواقع الاتصال الفيزيائية بين الشبكة الإندوبلاسمية والميتوكوندريا — حيث يتدفق الكالسيوم عادة إلى الميتوكوندريا — أقصر وأقل تواتراً، وكان دخول الكالسيوم إلى الميتوكوندريا أقل. ثلاث مشكلات — نقص الكولين، تباطؤ إنتاج الهيـم وضعف نقل الكالسيوم — كلها أشارت إلى أداء ميتوكوندري متعطل.
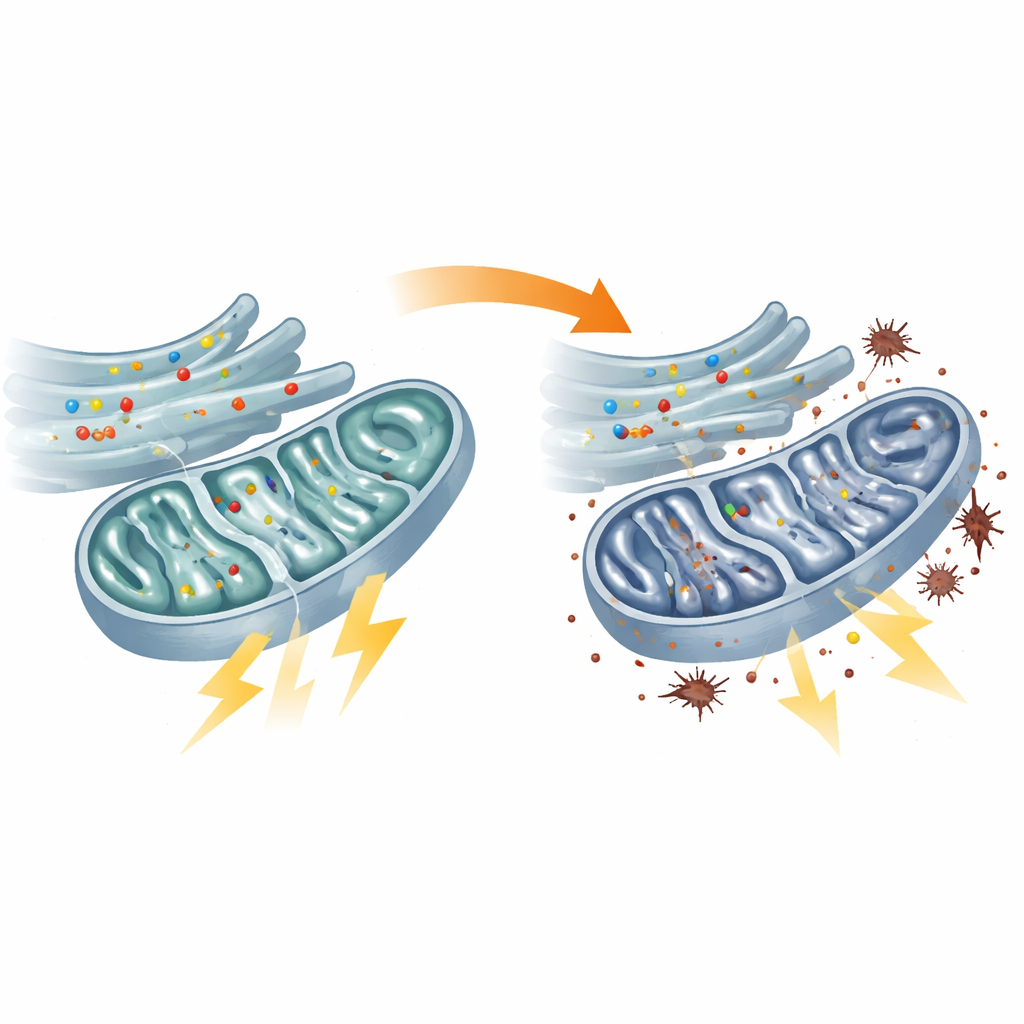
ميتوكندريا جائعة وأنظمة احتياطية مثقلة
أكدت اختبارات مباشرة لتمثيل الطاقة أن ميتوكوندريا خلايا المرضى كانت دون المستوى. مركز معالجة الوقود المعروف بدورة حمض الستريك (TCA) عمل بوتيرة أبطأ، وكان العديد من إنزيماته الأساسية أقل نشاطًا وسلسلة التفاعلات التي تحول الوقود إلى أدينوسين ثلاثي الفوسفات (ATP)، عملت بضعف. نتيجة لذلك، انخفضت مستويات ATP داخل الميتوكوندريا. حاولت الخلايا التعويض بزيادة التحلل السكري، وهو مسار أقل كفاءة لحرق السكر خارج الميتوكوندريا. جاء هذا التحول في استراتيجية الطاقة بتكلفة: تسربت إلكترونات من آليات الميتوكوندريا المجهدة وأدت إلى مستويات أعلى من بيروكسدة الدهون، شكل من أشكال الضرر التأكسدي لأغشية الخلايا. لوحظت عيوب مشابهة في أسماك الزرد ذات انخفاض flvcr1a، مما يربط فشل الميتوكوندريا مباشرة بنموذَج الحيوان للاعتلال العصبي الحسي.
لمحات عن علاجات مستقبلية عبر تعزيز طاقة الخلايا
بشكل مبشر، أمكن تلطيف بعض هذه العيوب في المختبر. عندما زاد الفريق اصطناعيًا دخول الكالسيوم إلى الميتوكوندريا عن طريق زيادة إنتاج بروتين قناة يُدعى MCU في خلايا المرضى، تعافت إنتاجية الطاقة وانخفضت علامات الضرر التأكسدي. كما حسّن تزويد الخلايا بمقدمة للهيـم، حمض 5-أمينوليفولينيك (ALA)، نشاط دورة TCA ووظيفة سلسلة التنفس ومستويات ATP، رغم أن التعرض المطول لـ ALA كان ضارًا في دراسات سابقة. عادى الكولين الزائد سيولة الغشاء وساعد على تقليل تلف الدهون، لكنه حقق مكاسب قصيرة المدى ومتواضعة في إنتاج الطاقة. تقترح تجارب الإنقاذ هذه أن لا مسار وحيد هو المسؤول؛ بل شبكة من اضطرابات الكولين والهيـم وتداول الكالسيوم تدفع الميتوكوندريا إلى ضعف مزمن.
لماذا تهم هذه النتائج المرضى
من خلال تتبع عواقب طفرات FLVCR1 من الجزيئات إلى الخلايا إلى الكائنات الحية كاملة، يقترح هذا العمل أن فشل الطاقة في الميتوكوندريا هو قوة دافعة وراء هذا الشكل من الاعتلال العصبي بفقدان الألم والمشاكل البصرية المصاحبة له. تكون الأعصاب الحسية والمستقبلات الضوئية بحاجة للطاقة بشكل غير عادي لأنها تحافظ على محاور طويلة أو تجدد باستمرار هياكل حساسة للضوء، مما يجعلها عرضة بشكل خاص عندما يتراجع إنتاج الميتوكوندريا. يقدم نموذج أسماك الزرد والخلايا المأخوذة من مرضى الآن ساحات اختبار عملية للعلاجات التي تقوي أيض الميتوكوندريا. وبينما ستتطلب علاجات مثل تناول الكولين، وتعزيز الهيـم المضبوط أو أدوية تزيد من امتصاص الكالسيوم الميتوكوندري تقييماً دقيقاً في نماذج حيوانية وتجارب سريرية، فإن الرسالة المركزية واضحة: إعادة إمداد الخلايا العصبية الضعيفة بالطاقة قد يساعد ذات يوم في حماية الأشخاص المولودين بلا أهم إشارة تحذيرية من صنع الطبيعة — الألم.
الاستشهاد: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
الكلمات المفتاحية: الاعتلال العصبي الحسي, خلل الميتوكوندريا, FLVCR1, عدم الإحساس بالألم, تمثيل طاقة الأعصاب