Clear Sky Science · ar
اضطراب توازن الحديد يسبب تدهور خلايا الشعر في القوقعة وفقدان السمع في الفئران الناقصة Gprasp2
لماذا يهم هذا السمع اليومي
غالبًا ما يُنظر إلى فقدان السمع على أنه نتيجة "تآكل واستخدام" بسيط، لكن لدى كثيرين يكون السبب عيوب جينية خفية. تكشف هذه الدراسة كيف يساعد جين نادر الدراسة، GPRASP2، على حماية خلايا الاستشعار الصوتي الحساسة في الأذن الداخلية من الضرر المدفوع بالحديد. عبر إظهار الكيفية الدقيقة التي ينهار بها توازن الأمور عند غياب هذا الجين، تفتح الدراسة أبوابًا لتشخيصات أكثر دقة وعلاجات مستقبلية لمشاكل السمع الوراثية وربما لاضطرابات المزاج المرتبطة.
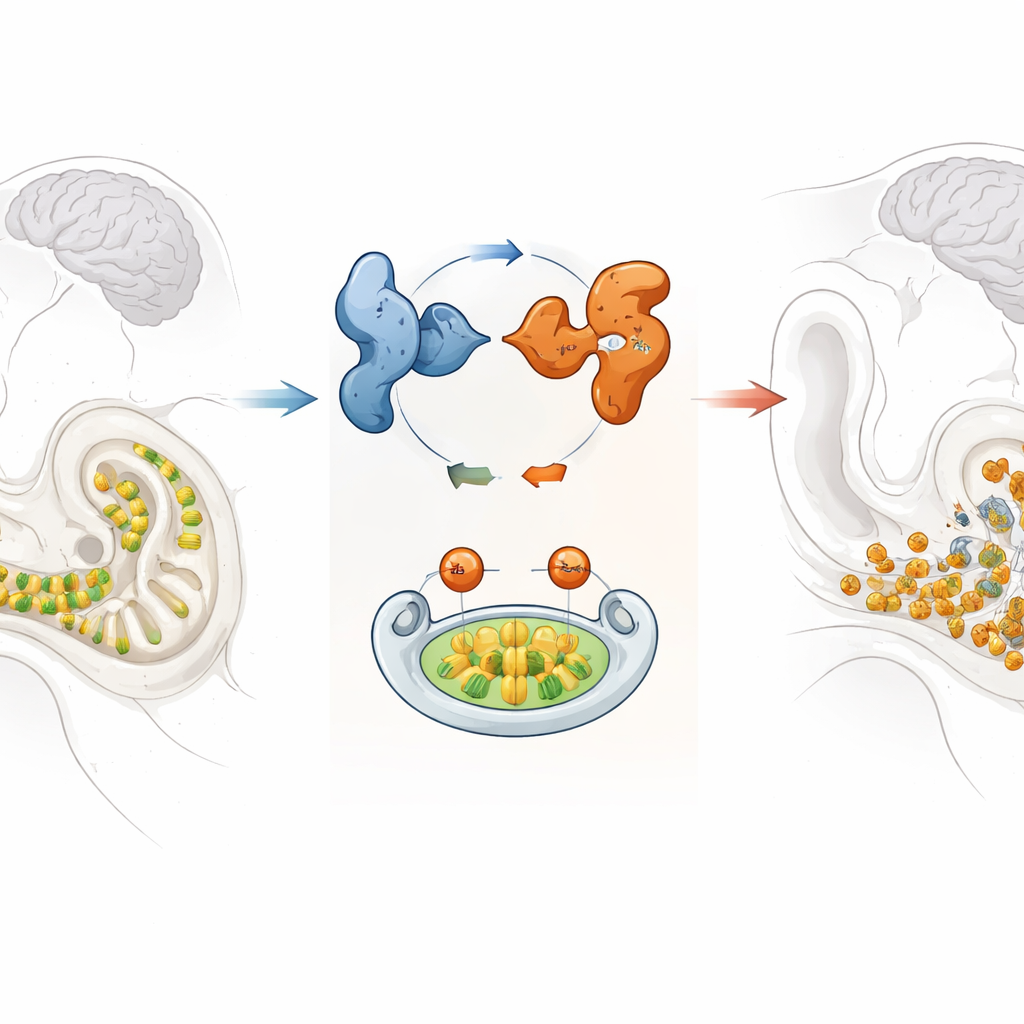
مستشعر صوتي هش في الأذن الداخلية
داخل قوقعة الأذن الملفوفة توجد صفوف من خلايا الشعر التي تحول الاهتزازات الطفيفة إلى إشارات كهربائية يفهمها الدماغ. وبمجرد فقدان هذه الخلايا لا تنمو مجددًا، لذا فإن الحفاظ عليها سليمة أمر حاسم للسمع طوال الحياة. ركز الباحثون على GPRASP2، الجين الذي وُجد سابقًا متغيرًا في عائلة تعاني من فقدان سمع متلازمي مرتبط بالكروموسوم X، أي يطال الذكور بشكل أساسي وقد يصاحبه أعراض إضافية. وعلى الرغم من معرفة وجود GPRASP2 نشطًا في الدماغ والأذن الداخلية، بقي دوره الدقيق في السمع غير واضح.
ماذا يحدث عند غياب الجين
لمحاكاة الحالة البشرية، استخدمت الفريق تحرير الجينات CRISPR لإنتاج فئران تفتقد نسخة عاملة من جين Gprasp2. أظهرت هذه الحيوانات فقدان سمع واضحًا عبر نطاق واسع من الترددات عند فحصها بتسجيلات كهربائية حساسة من العصب السمعي. كانت استجابتها للأصوات العالية المفاجئة مخففة، بينما كانت توازنها ومهاراتها الحركية في الغالب طبيعية، ما يشير إلى مشكلة محددة في السمع بدلاً من اضطراب حركة عام. ومن المثير للاهتمام أن الفئران أظهرت أيضًا سلوكيات شبيهة بالاكتئاب في عدة اختبارات معيارية، مما يوحي بأن هذا الجين يربط بين السمع والمزاج عبر عمله في كل من الأذن والدماغ.
الضرر داخل القوقعة
عند فحص علماء الأذن الداخلية في فئران ناقصة Gprasp2، وجدوا أن العديد من خلايا الشعر الخارجية مفقودة أو غير موضوعة في أماكنها، وغالبًا ما كانت الخلايا المتبقية لديها حزم مشوهة من الإسقاطات الدقيقة التي تعمل عادة كموازيك ضبط. كما لاحظوا تغييرات في الشريان الملتحمي (stria vascularis)، النسيج شديد النشاط الذي يحافظ على السائل والبيئة الكهربائية الخاصة اللازمة للسمع. وعلى المستوى المجهري، كانت مؤشرات موت الخلايا والإجهاد التأكسدي مرتفعة في خلايا الشعر الخارجية والخلايا العصبية القريبة، مما يدل على أن هذه البُنى تتعرض لهجوم شديد من جزيئات تفاعلية وأكثر عرضة للموت.
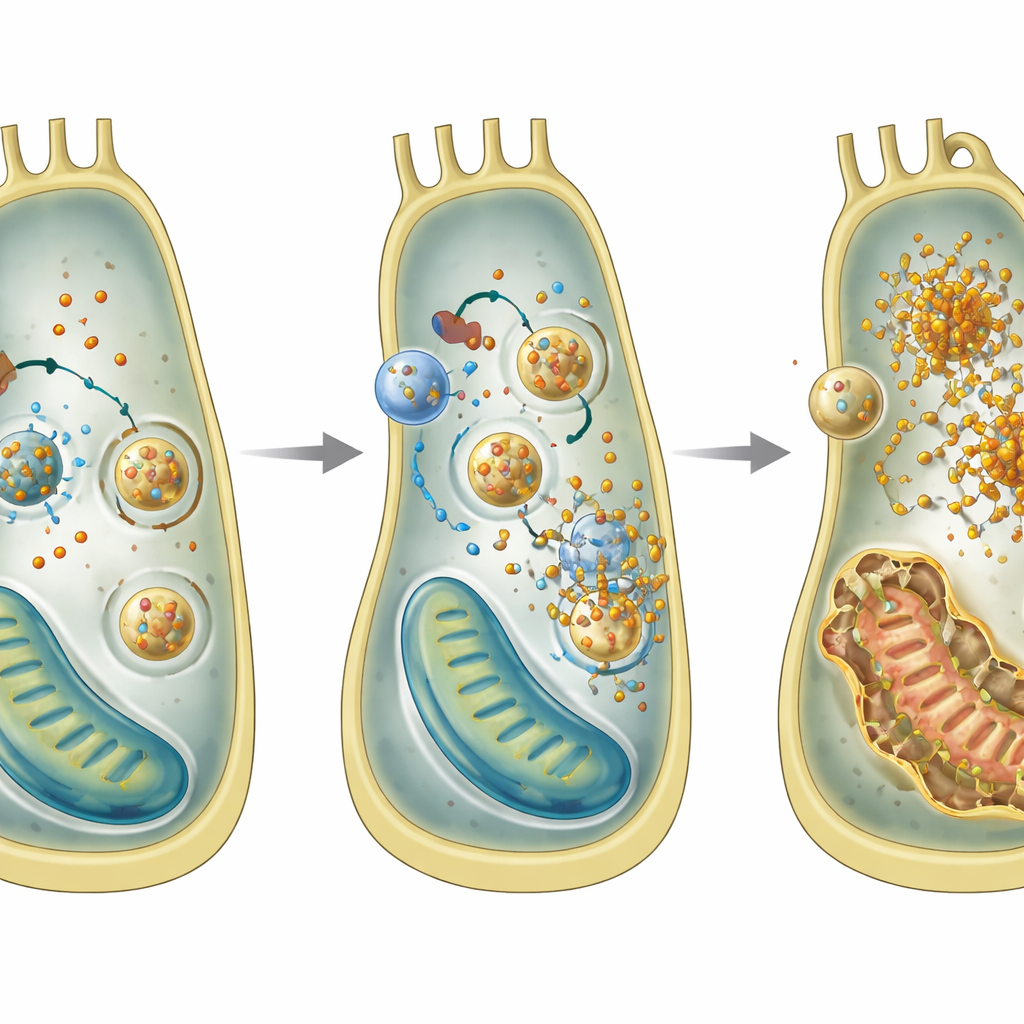
زيادة الحديد وإعادة التدوير المفرطة
بالغوص أعمق، استخدم الفريق سلالة خلوية من الأذن الداخلية لاستكشاف ما يخطئ داخل الخلايا الفردية الخالية من GPRASP2. اكتشفوا نمطًا مميزًا لشكل من أشكال موت الخلايا يسمى الفرَوبتوسِس، الذي يقوده الحديد وتأكسد الدهون. تراكمت في الخلايا الناقصة لـ Gprasp2 كمية أكبر من الحديد الثنائي (Fe2+)، وأنتجت المزيد من الجذور الحرة التفاعلية، وانخفضت مستويات الجلوتاثيون المضاد للأكسدة، وكانت الميتوكوندريات متضررة. أشارت تحليلات الجينات والبروتينات إلى زيادة في الفيريتينوفاجي (ferritinophagy)، وهي عملية تُسلَّم فيها جزيئات تخزين الحديد إلى حجرات إعادة التدوير وتُحلَّل، مطلقةً مزيدًا من الحديد داخل الخلية. أدى حجب هذه الخطوة من إعادة التدوير إلى تقليل تراكم الحديد، مما يدعم فكرة أن الفيريتينوفاجي المفرط مركزي في الضرر.
بروتين شريك رئيسي يضبط الحديد
سأل الباحثون بعد ذلك كيف يتحكم GPRASP2 في آلية إدارة الحديد هذه. عبر رسم خريطة للبروتينات التي تتفاعل مع GPRASP2، حددوا NCAM1، جزيء التصاق خلوي معروف بدوره في التعلم والذاكرة والمزاج. أظهروا أن GPRASP2 يرتبط ماديًا بـ NCAM1، وأن فقدان GPRASP2 يسبب انخفاض مستويات NCAM1 في خلايا الشعر وفي الخلايا السمعية المزرعية. ارتبط انخفاض NCAM1 بزيادة الفيريتينوفاجي وتراكم الحديد. إعادة NCAM1 في خلايا ناقصة Gprasp2 قللت من مستويات الحديد وكبتت منظّمات رئيسية للفيريتينوفاجي، رغم أن الأوتوفاجي العام بقي فعالًا. يشير هذا إلى أن GPRASP2 يضبط مسار إعادة تدوير محدد للحديد عبر NCAM1، بدلًا من تشغيل أو إيقاف نظام إعادة التدوير بأكمله.
ماذا يعني هذا للسمع وما وراءه
بعبارات بسيطة، تظهر هذه الدراسة أن GPRASP2 يعمل كمدير أمان للحديد داخل خلايا شعر القوقعة. عندما يكون GPRASP2 حاضرًا، يتعاون مع NCAM1 لمنع تخزين الحديد من التفريغ المفرط داخل الخلية، محافظًا على الضرر التأكسدي تحت السيطرة. عند تعطّل الجين، يختل تعامل الخلية مع الحديد، وتصدأ الخلايا من الداخل، وتموت خلايا الشعر الحيوية، ما يؤدي إلى فقدان السمع. وبما أن GPRASP2 وNCAM1 يعملان أيضًا في الدماغ، فقد يساعد نفس المسار في تفسير تغيُّرات المزاج التي تُرى لدى بعض المرضى. توفر فهم هذه الآلية المعتمدة على الحديد هدفًا واضحًا للأدوية أو العلاجات الجينية المستقبلية الهادفة للحفاظ على السمع لدى الأشخاص المصابين باضطرابات جينية مرتبطة بـ GPRASP2 أو مشابهة.
الاستشهاد: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
الكلمات المفتاحية: فقدان السمع الوراثي, خلايا شعر القوقعة, توازن الحديد, الفرَوبتوسِس (الموت بالخَرَسَنة الحديدية), GPRASP2