Clear Sky Science · ar
اختيار النماذج في أبحاث العلاجات القاعدية في المراحل ما قبل السريرية
تحويل الجينات إلى أدوية
تُعد علاجات الأحماض النووية نوعاً جديداً من الأدوية التي لا تعمل عن طريق حجب البروتينات كما تفعل معظم الأدوية، بل تتدخل خطوة أبكر على مستوى رسائلنا الجينية. تشرح هذه المراجعة كيف يختار العلماء النماذج المختبرية والحيوانية المناسبة لاختبار هذه الأدوية الموجهة إلى الـRNA قبل وصولها إلى المرضى. قد يهتم القارئ العادي بهذا لأن الاختيارات الذكية للنماذج قد تعني علاجات أسرع وأكثر أماناً وفعالية للأمراض الجينية، بما في ذلك الاضطرابات الطفيلية النادرة وحالات أكثر شيوعاً مثل أمراض القلب.
ما الذي يميز هذه الأدوية الجينية؟
تشمل علاجات الأحماض النووية (NATs) شُحَباً قصيرة تُسمى أوليجونوكليوتيدات مضادة للتعبير (ASOs) و-RNA متداخل صغير (siRNAs). بدلاً من الاعتماد على شكل وكلاء البروتين الكيميائي، تتعرف هذه الأدوية على أهدافها بقواعد الاقتران القاعدي — نفس مطابقة A‑T وG‑C التي تقوم عليها الـDNA. هذا يجعلها قابلة للبرمجة: بمجرد معرفة تسلسل الـRNA الذي تريد تغييره، يمكنك غالباً تصميم العديد من الأدوية المرشحة بسرعة من دون سنوات من الكيمياء التقليدية. الجزء الصعب لم يعد «هل نستطيع صنع مركب نشط؟» بل «كيف نقيس ما إذا كان يعمل فعلاً في سياق بيولوجي واقعي؟» ولأن اختلاف حرف واحد فقط في التسلسل قد يصنع الفارق في النشاط، يصبح اختيار أنظمة الاختبار المناسبة أمراً حاسماً.
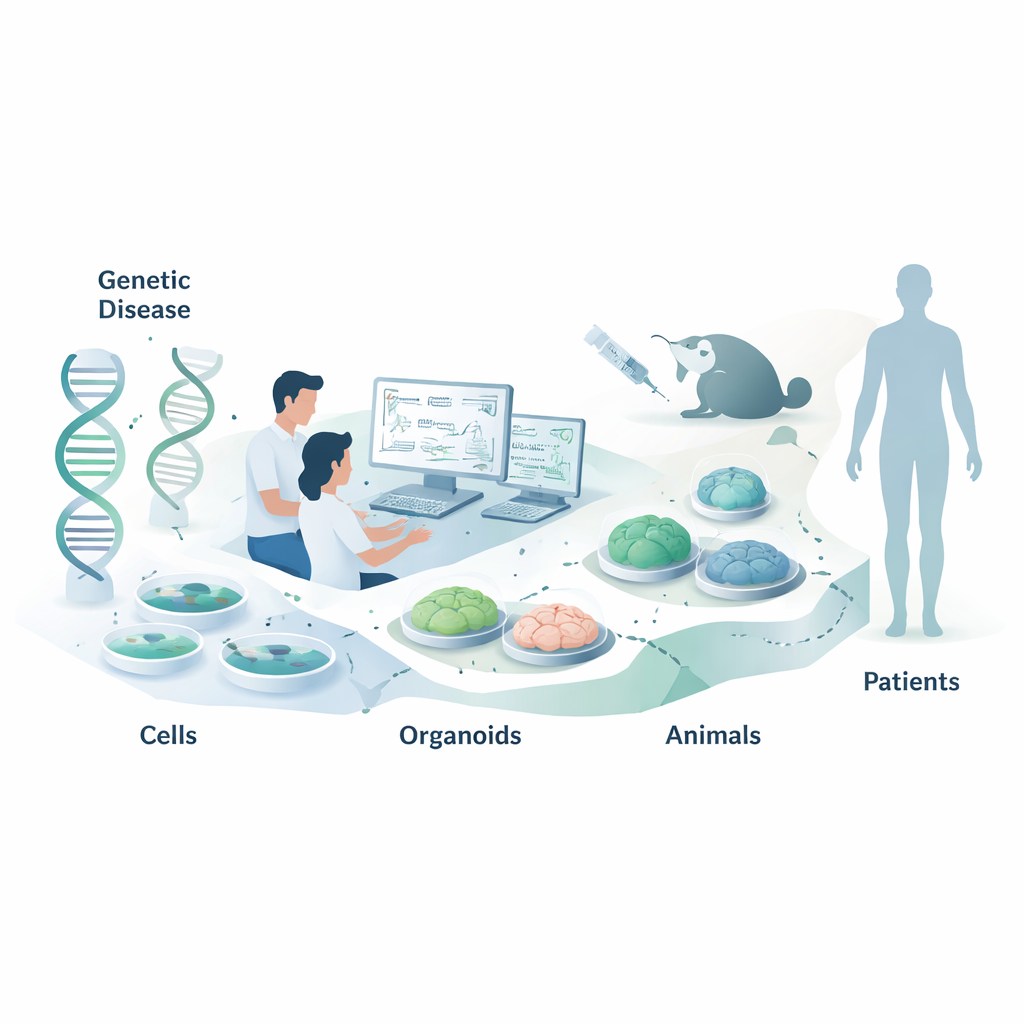
اختبارات الخلايا البسيطة: سريعة لكنها ليست القصة كاملة
المحطة الأولى لمعظم علاجات الأحماض النووية هي طيف من خطوط الخلايا سريعة النمو نسبياً، مثل خلايا HeLa أو HEK293، التي تُعبر عن الـRNA المستهدف بالفعل. يضيف الباحثون مكتبات كبيرة من مرشحات ASO أو siRNA ثم يقيسون مقدار انخفاض الـRNA الهدف وبروتينه باستخدام تقنيات مثل PCR وWestern blot. قد يعملون أيضاً مع خلايا مأخوذة من مرضى، والتي تلتقط خلفية الشخص الجينية الدقيقة وتسمح باختبار أدوية «انتقائية الأليل» التي تُسكت النسخة المعطوبة فقط من الجين. عندما لا يُعبر الجين الطبيعي بسهولة، يُدخل العلماء أحياناً جينات مصغرة صناعية أو بلازميدات مراسل تضيء عندما يُقص الـRNA أو يُركب بشكل صحيح. هذه الأنظمة قوية لمقارنة كثير من التصاميم بسرعة، لكنها قد تفوت تفاصيل مهمة، مثل البنية الطبيعية للـRNA أو المعالجة الخاصة بنوع الخلية، لذلك يجب تأكيد النتائج في سياقات أكثر واقعية.
من الإصلاح الجزيئي إلى سلوك الخلايا الحقيقي
تهدف العديد من علاجات الأحماض النووية ليس فقط إلى تدمير الـRNA المعطوب بل إلى إصلاحه عن طريق تعديل الطي الترابطي (splicing)، العملية التي تربط أجزاء رسالة الجين معاً. يمكن أن تتسبب ASOs المصممة بعناية في تخطي الخلايا لإكسون ضار، أو استعادة قطعة مفقودة، أو منع إدخال «إكسون زائف» يكسر الشفرة. لرؤية ما إذا كانت هذه التغييرات تحسّن وظيفة الخلية فعلاً، يتجاوز الباحثون قياسات بسيطة لمستويات الـRNA والبروتين. في الخلايا المستمدة من المرضى، يختبرون ما إذا عادت نشاطات الإنزيمات، أو ما إذا عاد نقل الأيونات في خلايا الرئة إلى وضعه الطبيعي، أو ما إذا استجابت مسارات الإشارة في الخلايا المناعية بشكل صحيح. وبصورة متزايدة، يستخدمون العضيات ثلاثية الأبعاد — أنسجة مصغرة تُنمى من خلايا جذعية مأخوذة من المرضى — التي يمكنها محاكاة نبضات القلب، أو نشاط شبكات الدماغ، أو سلوكيات معقدة أخرى. هذه النماذج ثلاثية الأبعاد أقرب إلى الأعضاء الحقيقية لكنها أصعب وأبطأ وأكثر تكلفة للتشغيل، لذلك على الفرق موازنة الواقعية مع كمية الاختبارات الممكنة.
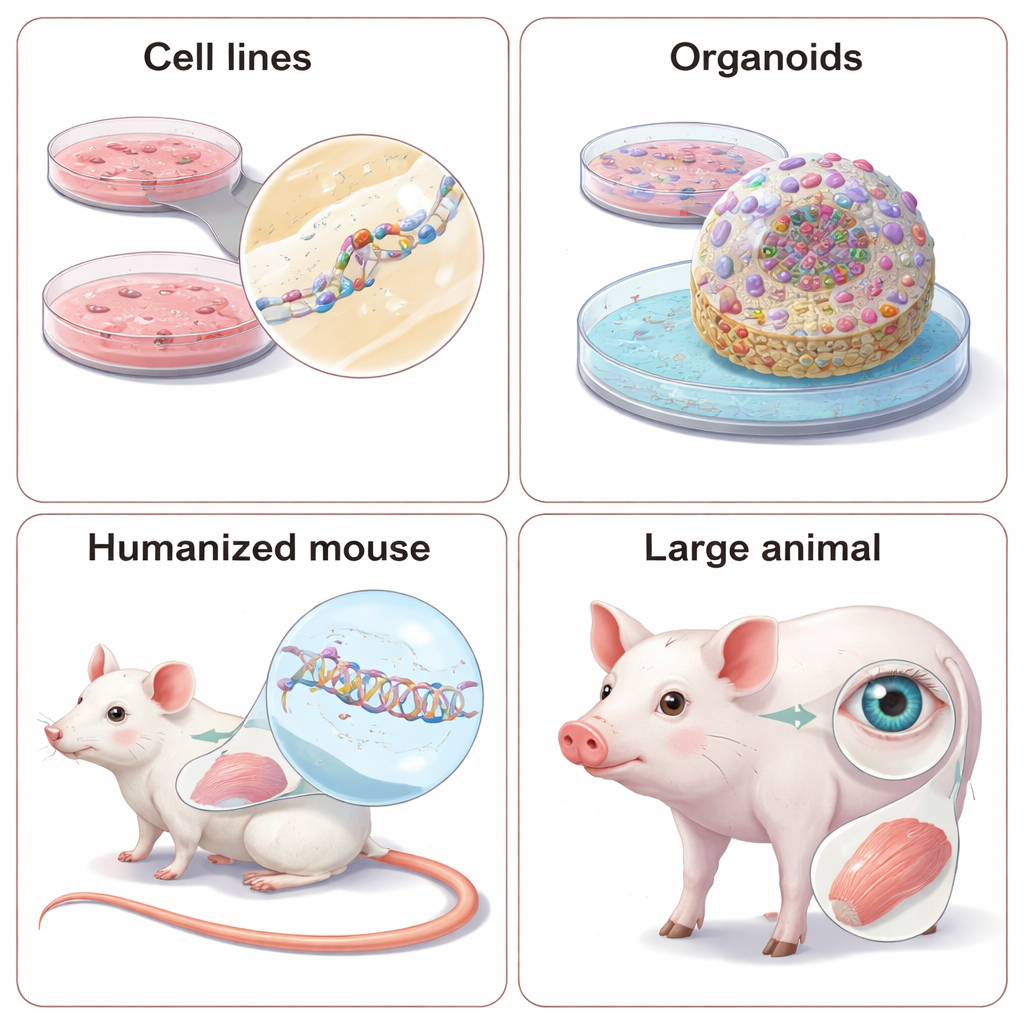
لماذا لا تزال الحيوانات مهمة — وكيف نؤنسنها
بعض سمات المرض، مثل الأيض على مستوى الجسم كله، أو التفاعلات بين الأعضاء، أو السلوك، لا يمكن التقاطها في أطباق زجاجية. لذلك تُختبر علاجات الأحماض النووية في حيوانات حية. وبما أن هذه الأدوية تهتم بالتسلسلات الدقيقة للـRNA، يواجه العلماء خياراً: تصميم أدوية «بديلة» تتوافق مع نسخة الحيوان من الجين، أو إعادة هندسة الحيوان ليحمل تسلسلات بشرية. يمكن أن تكشف ASOs وsiRNAs البديلة ما إذا كان خفض مستوى جين معين يحسن الأعراض في نماذج الفئران المألوفة، لكنها لا تحاكي تماماً الدواء الموجه للبشر. تسمح النماذج المؤنسة — فئران أو حتى خنازير صغيرة تحمل أجزاءً أو نسخاً كاملة من جينات بشرية — باختبار المرشح السريري الحقيقي لكنها تتطلب وقتاً وتكلفة كبيرين، وقد تؤدي اختلافات دقيقة في تنظيم الجينات بين الأنواع إلى مفاجآت. تبرز المراجعة أيضاً الاستخدام المتزايد للحيوانات الكبيرة، خاصة لأمراض العين والعضلات، حيث تشبه التشريح البشري بشكل أوثق.
نظرة إلى الأمام: نماذج أذكى وقليل من التخمين
يخلص المؤلفون إلى أنه لا توجد «أفضل» نموذج وحيد لأدوية الأحماض النووية؛ بل يحتاج كل مشروع إلى مسار مصمم خصيصاً يبدأ باختبارات سريعة وبسيطة ويتقدم نحو أنظمة أكثر تعقيداً وذات صلة بشرية. ومع دفع الجهات التنظيمية والمانحة لتقليل استخدام الحيوانات، من المتوقع أن تتحمل العضيات المتقدمة، وأجهزة الأعضاء على شريحة، والنماذج الحاسوبية جزءاً أكبر من العبء، خصوصاً عند دمجها مع أدوات التعلم الآلي التي تتنبأ بالتسلسلات والكيميائيات الأكثر نجاعة. في النهاية، من خلال فهم نقاط القوة والنقاط العمياء لكل نموذج — ومن خلال تبادل الممارسات الفضلى والبيانات عبر المجال — يمكن للباحثين تحويل الأفكار الجينية القابلة للبرمجة إلى أدوية آمنة وفعالة للمرضى بمزيد من الاعتمادية.
الاستشهاد: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
الكلمات المفتاحية: علاجات الأحماض النووية, أوليجونوكليوتيدات مضادة للتعبير, siRNA, نماذج ما قبل السريرية, العلاج الجيني