Clear Sky Science · ar
Wnt11 يتوسط تفاعل الأرومات والخلايا العضلية الملساء لتعزيز تليّف المثانة العصبي لدى الفئران
عندما تفشل الأعصاب، تندب المثانة
يعاني العديد من الأشخاص المصابين بإصابات الحبل الشوكي أو التصلب المتعدد أو مرض باركنسون من «المثانة العصبية»، حيث تعجز الأعصاب التالفة عن التحكم الصحيح في تخزين وإفراز البول. مع مرور الوقت، يمكن أن يصبح جدار المثانة سميكًا وصلبًا بنسيج شبيه بالندبة، مما يهدد صحة الكلى وجودة الحياة. تكشف هذه الدراسة على الفئران عن الجاني الجزيئي الرئيسي وراء هذا التندب وتقترح سبلًا جديدة لإبطاء الأذية أو حتى منعها.
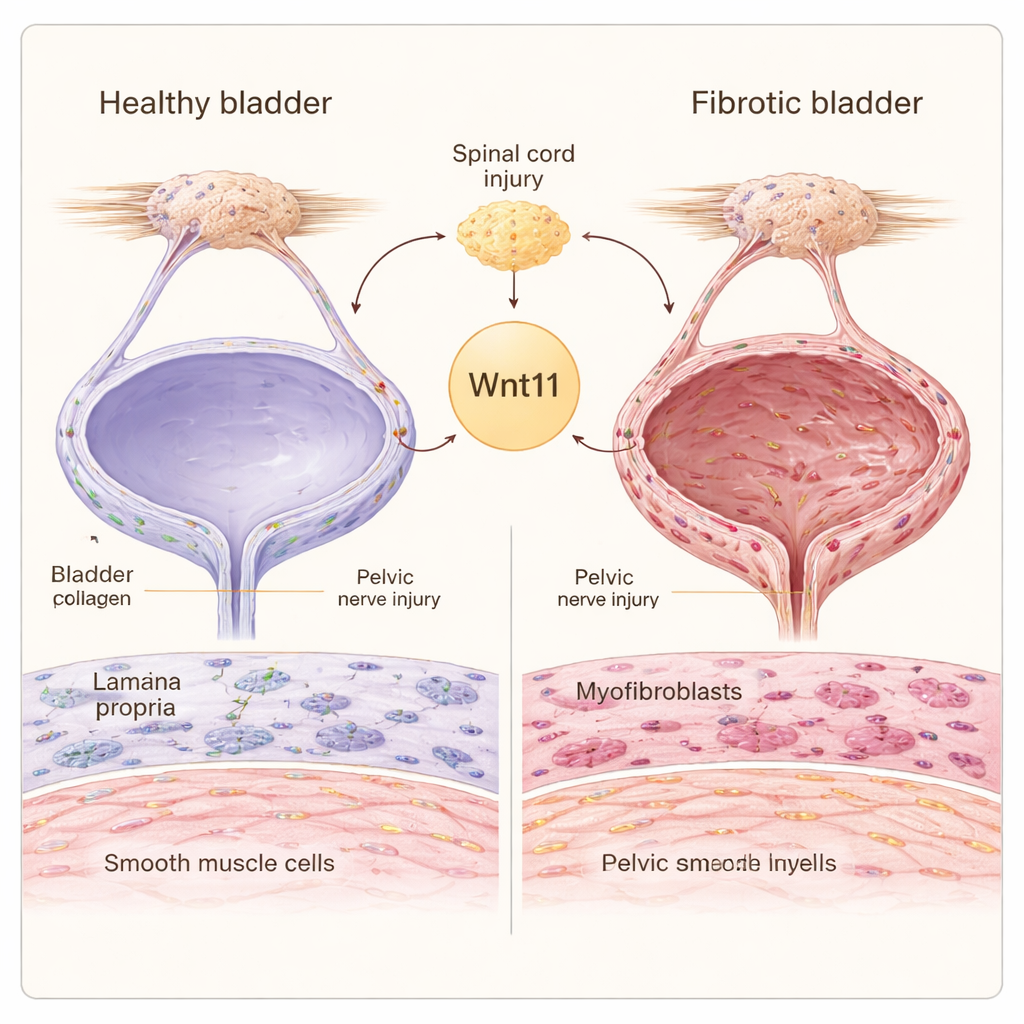
تكلفة خفية لأذية الأعصاب
عندما تُصاب الأعصاب التي تخدم المثانة، سواء في الحبل الشوكي أو قرب الحوض، تضطر العضو للعمل بجهد أكبر للتعامل مع البول. يحتوي جدار المثانة على نوعين رئيسيين من الخلايا الداعمة: الأرومات، التي تصنع مادة السقالة حول الخلايا، والخلايا العضلية الملساء، التي تنقبض لدفع البول إلى الخارج. في المثانة العصبية، يمكن أن تتحول الأرومات إلى «أرومات ليفية» نشطة جدًا تفرز كولاجينًا زائدًا، بينما تتحول الخلايا العضلية الملساء من حالة رشيقة قابضة إلى حالة أكثر ضخامًة ومُصنِّعة. معًا، تضع هذه التغيرات نسيجًا ندبيًا صلبًا يقلل من قدرة المثانة على التمدد والإفراغ.
جزيء إشارى يخرج إلى الواجهة
ركز الباحثون على عائلة من بروتينات التواصل الخلوي تسمى ربطات Wnt، المعروفة بتنظيم نمو الأنسجة والتندب في أعضاء أخرى. عند فحص مثانات فئران ذات أذية عصبية، وجدوا أن أحد الأعضاء، Wnt11، ازداد باستمرار وبشكل قوي في المثانات المتليفة الناجمة عن إصابة الحبل الشوكي أو سحق العصب الحوضي. ارتفعت مستويات Wnt11 في كل من الأرومات والخلايا العضلية الملساء، وارتبطت كمية Wnt11 بشدة ضعف وظيفة المثانة. عندما تعرضت خلايا المثانة الطبيعية في المختبر لعامل آخر محرض للتندب، TGF-β1، زادت أيضًا إنتاجية Wnt11، مما يوحي بوجود حلقة تعزيز متبادلة بين هذين الإشارَتين.
من رسالة كيميائية إلى ندبة دائمة
لاختبار ما إذا كان Wnt11 مجرد مرافق أم دافعًا نشطًا، أضاف الفريق بروتين Wnt11 إضافيًا إلى فئران ذات أذية عصبية وعرقل أيضًا إفراز Wnt بدواء يسمى LGK974. مكّنت إضافة Wnt11 من تضخيم المثانات، وساءت أنماط الضغط أثناء الامتلاء والإفراغ، وتثخنت طبقة العضلات، وازداد ترسب الكولاجين. أما حجب إفراز Wnt فكان له التأثير المعاكس، حيث خفف من مشاكل التبول وقلّل النسيج الندبي. في الخلايا المعزولة، دفع Wnt11 الأرومات نحو حالة الأرومات اللّيفية وميّز الخلايا العضلية الملساء نحو النمط المصنّع المحفز للتليّف. كَشَطُ جين Wnt11 نفسه خفف هذه التغيرات، مما أوضح أن Wnt11 هو مسرّع مركزي لإعادة تشكيل المثانة.
كيف تفسر الخلايا إشارة التليّف
بتعميق البحث، رسمت الدراسة المسار من Wnt11 على سطح الخلية إلى تغييرات جينية في النواة. وُجد أن Wnt11 يرتبط بمستقبل يسمى Vangl2 على الأرومات والخلايا العضلية الملساء في المثانة. هذا الزوج لم يستخدم المسار الكلاسيكي لـWnt الذي يتضمن البروتين β-catenin؛ بل فعّل سلسلة مختلفة تُسمى مسار استقطاب الخلية المستوي (PCP). هنا، يستدعي Wnt11 وVangl2 بروتين موصل يُدعى DVL2، الذي يفعّل بعد ذلك الإنزيم JNK. يقوم JNK بدوره بتنشيط عوامل النسخ c-JUN وNFAT5، واللتان تنتقلان إلى النواة وتساعدان في تشغيل الجينات المعززة للتليّف. تلاقت أيضًا مسار TGF-β1، المعروف كمحرض للتندب، ماديًا ووظيفيًا مع هذا المسار Wnt11–Vangl2–JNK، بحيث يعزز كل من الإشارَتين تأثير الأخرى سواء عند غشاء الخلية أو داخل النواة.
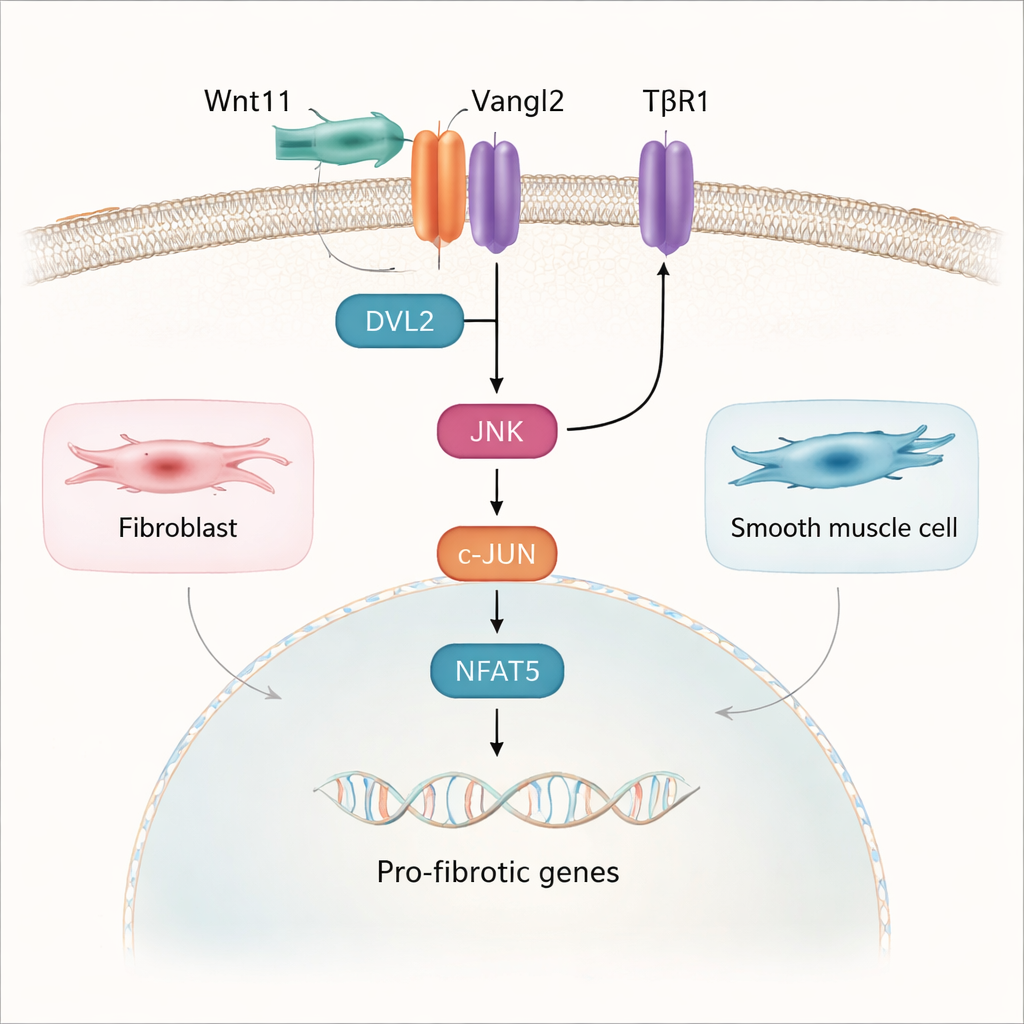
نحو مثانات أنعم وأكثر صحة
نظرًا لتعاون Wnt11 وTGF-β1 في تصلب المثانة، اختبر الفريق أدوية تحجب خطوات رئيسية في كلا المسارين. في الفئران المصابة بالمثانة العصبية، أدى التثبيط المشترك لمستقبل TGF-β المسمى TβR1 وإنزيم JNK إلى أفضل النتائج: مثانات أصغر، جدران عضلية أرق، كولاجين أقل، وتحسّن في تخزين وإفراغ البول مقارنة بالعلاج بدواء واحد فقط. للقراء غير المتخصصين، الخلاصة أن إشارة محددة ناتجة عن إصابة عصبية، Wnt11، تساعد على تحويل الخلايا الداعمة والعضلية الطبيعية إلى خلايا مكوّنة للندبات. إن مقاطعة هذه الإشارة، لا سيما مع حواجز TGF-β التقليدية، قد تشكّل أساس علاجات مستقبلية تهدف ليس فقط لإدارة الأعراض، بل للحفاظ على بنية المثانة ووظيفتها لدى الأشخاص ذوي المثانة العصبية.
الاستشهاد: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
الكلمات المفتاحية: المثانة العصبية, التليّف, Wnt11, الخلايا العضلية الملساء, إشارة TGF-β